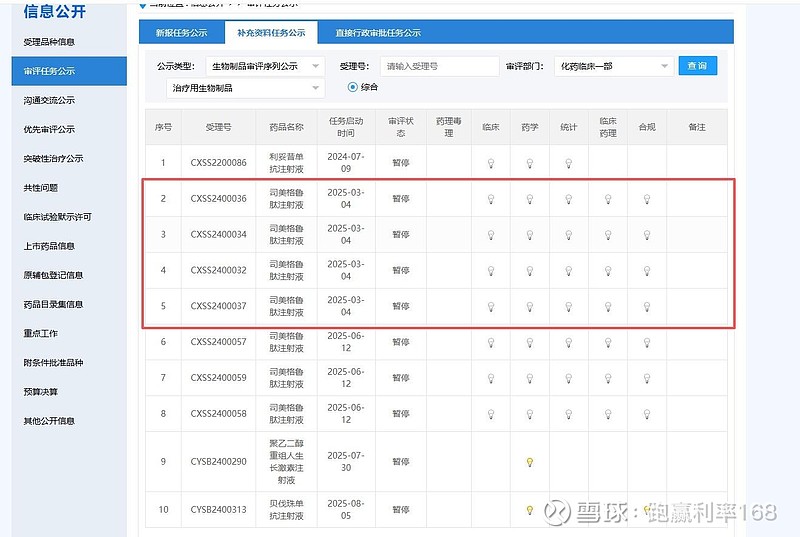
$九源基因(02566)$ 司美格鲁肽专利已于2026年3月20日到期,但国家药审中心九源基因申报的司美格鲁肽一直处于暂停状态。
之前一直认为专利到期了就可以顺利拿到批文,后面查询到中瑞贸易协议第11.11条:
一、缔约双方应依据 TRIPS 协定第 39 条保护未披露信息。
二、对于申请人为获得药品和农用化学品上市审批向主管部门提交的未披露试验数据或其他数据,自批准该上市许可之日起至少 6 年内,缔约双方应禁止其他申请人在药品(包括化学实体和生物制品)和农业化学品上市许可申请中依赖或参考上述未披露试验数据或其他数据。
三、为了避免对涉及脊椎动物的农业化学品进行不必要的重复试验,只要给予第一申请者充分补偿,可以允许他人依赖或参考这些数据。
该条款有个试验数据6年保护期(国内诺和诺德用的是瑞士子公司),诺和诺德的司美在国内是2021年4月上市,如果这样算的话,那国内仿制药企最早只能2027年4月拿到批文。
目前唯一能提前拿到批文的转机应该是2026年5月15日正式生效的最新《中华人民共和国药品管理法实施条例》,该条例第二十二条:
国家对含有新型化学成份的药品以及符合条件的其他药品的上市许可持有人提交的自行取得且未披露的试验数据和其他数据实施保护,任何人不得对该未披露的试验数据和其他数据进行不正当的商业利用。
前款规定的数据的保护期限自药品注册之日起不超过6年。在保护期限内,其他申请人未经药品上市许可持有人同意,使用前款规定的数据申请药品注册的,不予许可;但是,其他申请人提交自行取得数据的除外。
除下列情形外,药品监督管理部门不得披露本条第一款规定的数据:
(一)公共利益需要;
(二)已采取措施确保该类数据不会被不正当地进行商业利用。
本条第一款规定的数据的具体保护办法,由国务院药品监督管理部门制定。
该条例明确指出药品试验数据有6年保护期,但具体保护办法,要单独出台实施办法(大概率实施办法会在2026年5月15日药品管理办法正式生效前落地,否则无法配套)。
根据2025年3月24日国家药监局发布的《药品试验数据保护实施办法》(征求意见稿)第五条:
第五条(创新药相关数据保护) 自创新药首次境内上市许可之日起,给予6年数据保护期。
境外已上市境内未上市的原研药品申请在境内上市的,数据保护期限为6年减去该药品在境内提交上市许可申请被受理之日与该药品境外首次获得上市许可之日的时间差。数据保护期自该药品在境内获得上市许可之日起计算。
该条款规定6年保护期要减掉境外上市时间,诺和诺德的司美格鲁肽最早是2017年12月在美国上市,那么数据保护时间应该到2023年12月。
综述:国内的司美格鲁肽仿制药企最早2026年5月后,最晚2027年4月才能拿到批文。