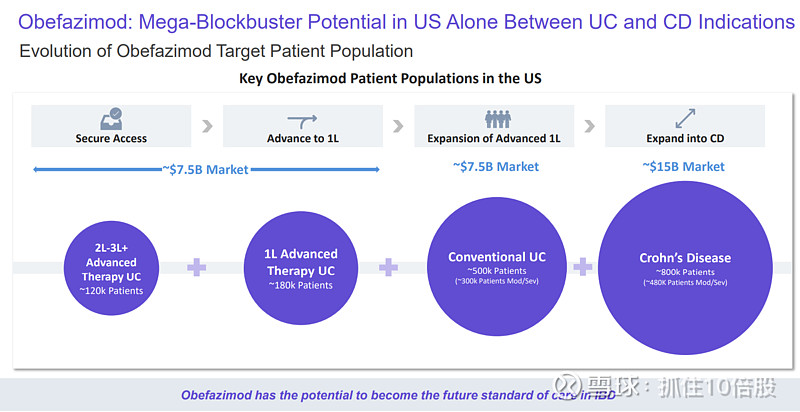
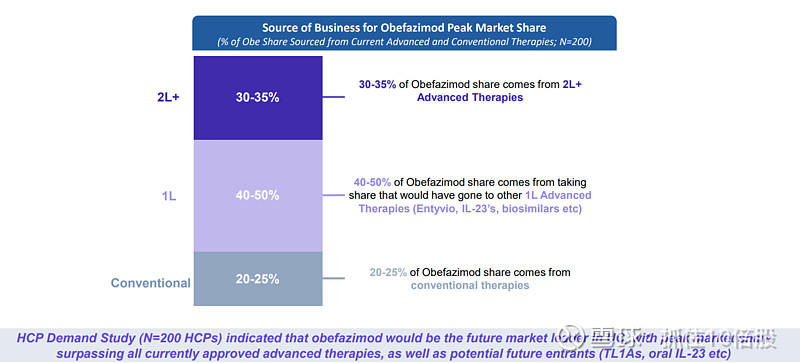
正大丰海5亿美元分子长啥样?
1月29日,纽约,FormationBio和江苏正大丰海药业(CTFH)宣布,FormationBio收购FHND5032的全球权利,FHND5031是一种口服小分子miR-124激动剂,正在开发用于治疗自身免疫性疾病。
根据协议条款,正大丰海将获得KenmareBio的少数股权,外加预付款和额外的开发、监管和商业里程碑,总计高达5亿美元,以及未来潜在销售的特许权使用费。
Abivax的first in class小分子新药obefazimod(ABX464)正处于三期临床。有望以全新机制改写溃结治疗格局。
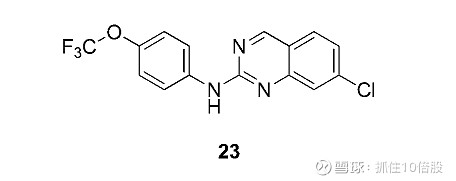
一、丰海专利WO2025045123A1
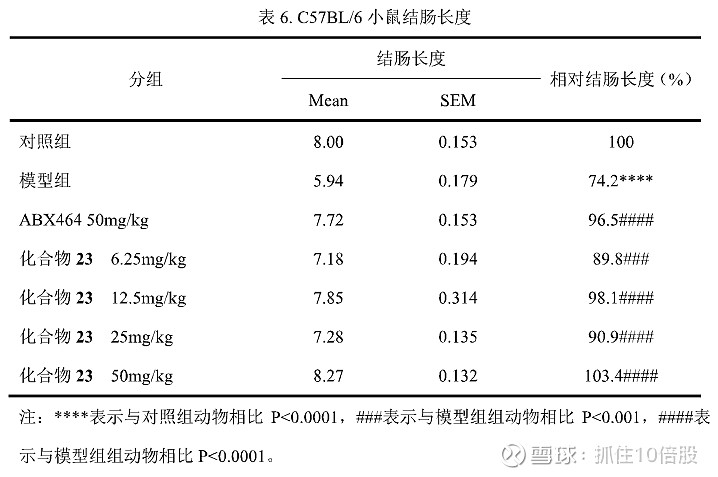
药效
小鼠DSS模型药效和ABX464相当。
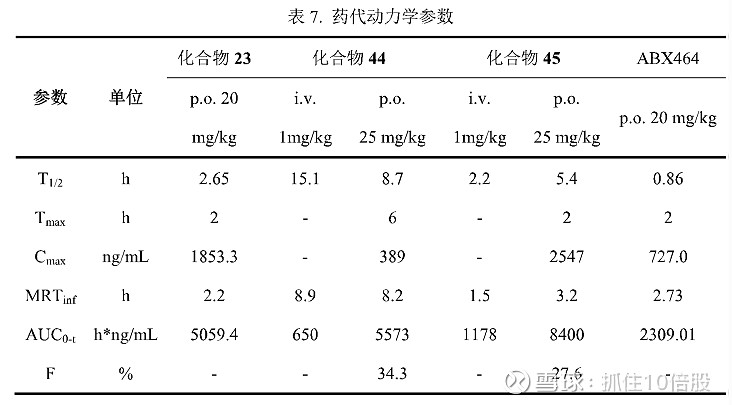
2.药代动力学
同等剂量下,相比于ABX464,化合物23消除半衰期长,系统暴露量(Cna和AUCo高,药代动力学性质良好。
二、国内部分玩家
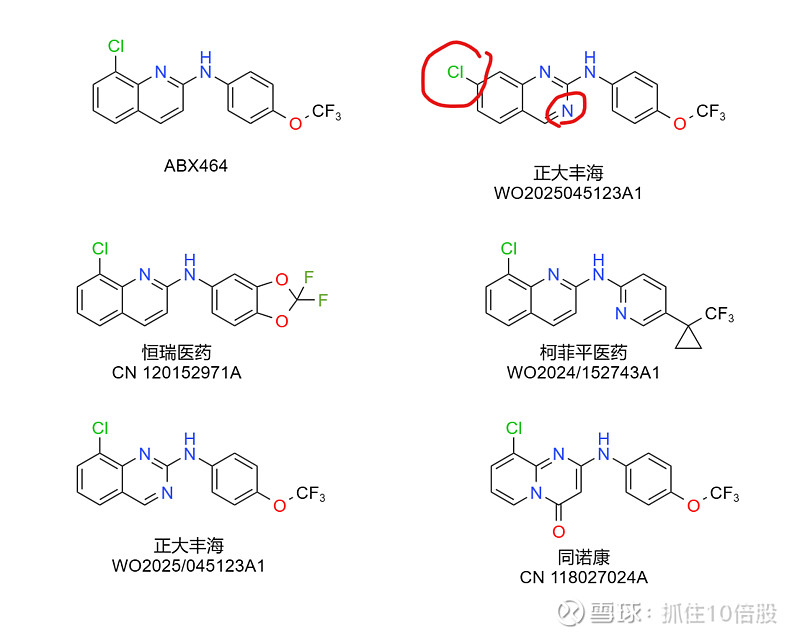
丰海的专利在芳环上加了N原子,Cl取代移了一个位置。结果药代动力学性质优于ABX464。
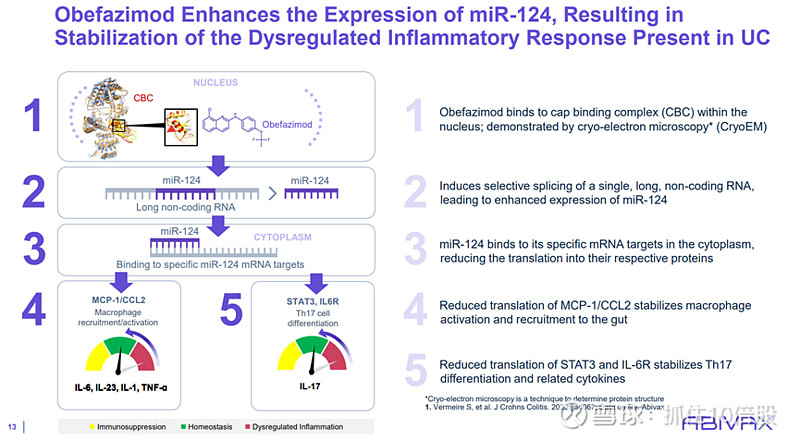
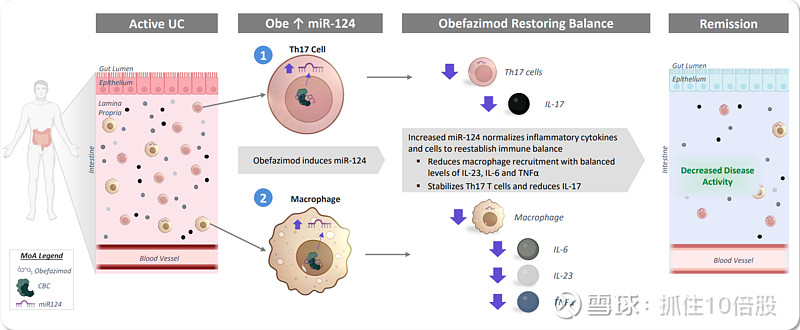
三、RNA剪接调控小分子作用机制
Obefazimod会和帽结合复合物结合,诱导单一长链非编码RNA的选择性剪接,从而增强miR-124的表达。miR-124与细胞质中的特定mRNA靶标结合,抑制其相应蛋白质的翻译。MCP-1/CCL2的翻译减少,从而稳定巨噬细胞的激活和向肠道的募集。STAT3和IL-6R的翻译减少,从而稳定Th17细胞的分化及相关细胞因子。在超过1000种microRNAs中,Obefazimod被发现仅能增强miR-124的表达。在临床前的概念验证中,Obefazimod在DSS引发的结肠炎小鼠模型中有效,这与已知的miR-124特性一致,观察到炎症细胞因子和趋化因子的减少。在临床试验中,溃疡性结肠炎患者血液和结肠组织中miR-124的表达增强。溃疡性结肠炎患者体内炎症细胞因子(如IL-23和IL-17)减少,类风湿关节炎患者体内IL-6也减少。
四、Obefazimod三期临床数据
3期临床设计:2个诱导期,1个维持期试验。主要终点为第8周的临床缓解率。次要终点为维持期第52周的临床缓解率。2025年7月22日报告了诱导期的临床数据。
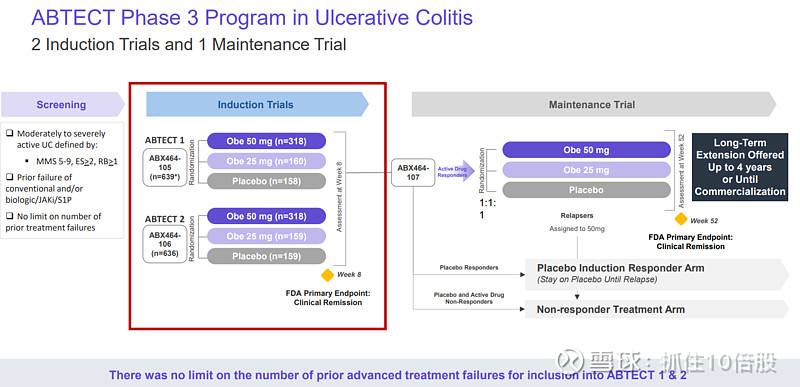
临床结果:
1.诱导期
主要终点:ABTECT-1 和 ABTECT-2 试验的结果表明,Obefazimod在每日一次 50 和25mg剂量方案下,在第 8 周达到了FDA的主要终点-临床缓解。
在 ABTECT-1(研究 105)和 ABTECT-2(研究 106)试验中,每日一次 50 mg剂量的Obefazimod在第 8 周时,经安慰剂校正后的临床缓解率达到了 16.4%(p<0.0001)。25mg剂量,经安慰剂校正后的临床缓解率达到了 13.2%(p<0.0001)
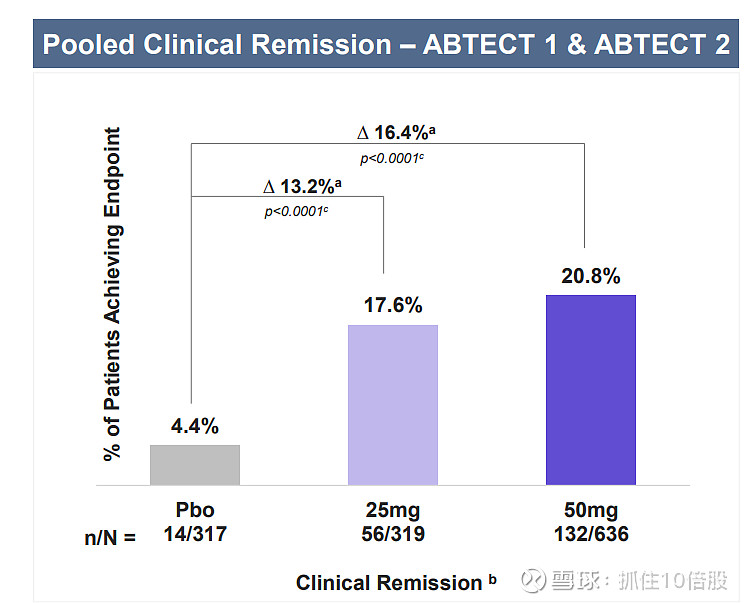
维持期
虽然三期临床维持期数据还未读出。从二期的开放标签数据可以看出相比于上市药物,Obefazimod具有最高的经安慰剂调整后的临床缓解。
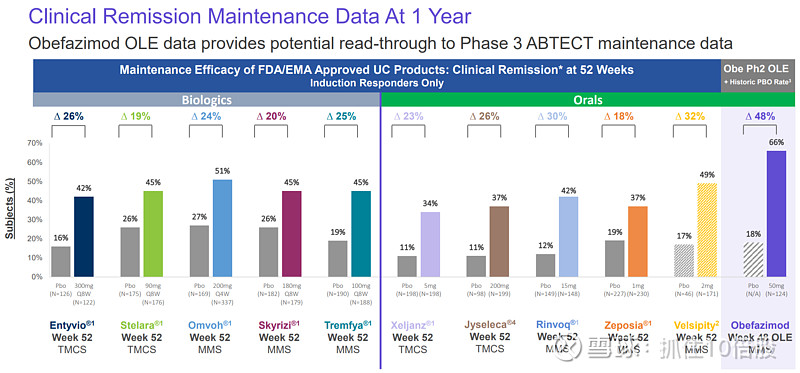
四、Obefazimod价值几何?
仅UC的1L及2-3L+的市场就有75亿美元。未来可扩展到传统用药及CD。