谁会是NSCLC免疫治疗2.0时代的最优解
$康方生物(09926)$ $信达生物(01801)$ $三生制药(01530)$
NSCLC是PD1/PDL1最大的适应症,预计全球的PD1/PDL1销售额的35%左右,全球销售峰值将可能200-300亿美元!绝对是肿瘤免疫治疗的天王山,甚至可以说免疫药物得NSCLC市场者得天下!当初K药也是凭借这个适应症一举打败了FIC的O药,现在康方生物的AK112以及信达生物的IBI363都把这个适应症作为首发或者优先开发的对象!
那么,在肿瘤免疫治疗2.0时代,谁才是下一个真命天子呢?我们尝试结合目前的药理、病理以及现有临床数据进行分析,试图找到答案!
一、免疫治疗1.0时代
我们先来看NSCLC免疫1.0时代王者K药的临床数据:

K药在NSCLC中最核心且奠定其王者地位的临床试验主要有三个:包括KEYNOTE024:PDL1>=50%的NSCLC;KEYNOTE189:EGFR和ALK突变阴性的非鳞NSCLC、及KEYNOTE189。
三个临床试验都有一个非常明显的特征:PFS延长幅度不大,但OS延长幅度很大,延长幅度达到PFS的2-5倍,显示免疫疗法的长拖尾效应!
KEYNOTE024,K药对比化疗,PFS延长2.2个月,但OS大幅延长12.1个月;
KEYNOTE189,K药联合化疗对比化疗,PFS延长4.1个月,但OS大幅延长12.1个月
KEYNOTE407,K药联合化疗对比化疗,PFS延长2.9个月,但OS大幅延长5.5个月
更重要的是5年OS率大幅提升,即使对照组很多后来也交叉使用了K药等,但即使如此,在PDL1高表达的NSCLC,5年生存率高达30%以上,有近1/3的患者获得了长期带瘤生存,而传统化疗在免疫治疗时代之前的经验值是5年生存率不到5%,所以PD1将长生存率提升了4-6倍!而则也是患者及医生对免疫治疗趋之若鹜的主要原因。
因为OS才是肿瘤治疗的黄金标准,K药等PD1就是凭借其对患者生存期的大幅延长,从而成为NSCLC治疗的标准疗法!而要取代K药等第一代IO药物,最重要的是必须在OS上能够打败K药,而不仅仅是PFS!
NSCLC加上其他适应症,预计整体PD1靶点的全球销售峰值将超过800亿美元,谁能打败K药,谁就将成为下一个肿瘤治疗的王者,下一代药物必然伴随用药时间更长且适应症将更加广泛,因此下一代IO药物的全球销售峰值将必然超过1000亿美元!不仅如此,因为以后肿瘤治疗将迈向IO+ADC,谁掌握了下一代IO,谁就更有机会引领下一代的IO+ADC,从而带动ADC药物全球市场份额的上升。所以,下一代IO药物是目前肿瘤治疗、尤其是实体瘤治疗的天王山之战!
二、PD1/VEGF双抗的突破与局限
2.1 VEGF靶点的短板
在PD1单抗大获成功之后,寻找下一个替代升级产品就成为医药行业的重中之重,而将PD1和VEGF两个已经验证过的靶点联合使用就顺理成章,包括罗氏的impower150试验,也包括默沙东进行的著名可乐试验!其结果罗氏之后再没有开过PDL1联合VEGF的NSCLC注册临床试验,而可乐组合则是大面积崩塌!其原因我曾写过文章:AK112:PFS稳了,OS能赢吗
我曾经对PD1/VEGF成为免疫治疗2.0的最优解抱有很大的期望,但连续两次OS翻车使得我对自己原来的判断产生了怀疑。我也曾经说过:如果AK112仅仅是PFS取得阳性结果,OS更差,那么这个药基本上就废了;如果PFS阳性结果,OS非劣或者有改善趋势但没有统计学上的显著优势,那么112国内能成药,但海外难度很大;如果最终PFS和OS双阳性结果,那么将有望在很多适应症上取代PD1成为免疫用药的基础,那将有望成为国际性的大药!
那么,AK112会是哪种情形呢,从目前的数据情况看,第一种情形完全可以排除,因此,AK112至少成药没问题,但OS能不能达到统计学优势呢?这个对于现在已经一千多亿市值的公司而言,已经成为问题的关键了!
我们知道,VEGF靶点的鼻祖是贝伐珠单抗,而贝伐珠单抗在其临床试验中,最大的缺点有两个:其一是很容易产生耐药,肿瘤可通过多种通路快速代偿 VEGF 的抑制(数周至数月内),导致药物疗效迅速衰减,使得PFS的延长幅度普遍不大;其二是没有类似纯免疫疗法的拖尾效应,OS的延长幅度基本上和PFS的延长幅度相当,下表是贝伐珠单抗一些临床试验的PFS和OS数据。
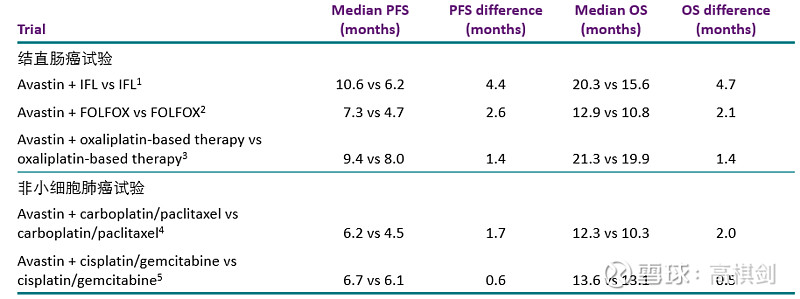
无论是在CRC还是在NSCLC中都是如此,PFS和OS两者相差不超过半个月!尤其是在NSCLC中,延长幅度更加小,无论PFS还是OS的延长幅度都没有超过2个月。
2.2 PD1/VEGF双抗对于PFS的突破
AK112为代表的PD1/VEGF凭借其双富集作用,在PFS上完全起到了1+1>2的效果
两个临床试验的PFS曲线都非常漂亮,HR值都很低,301试验PFS的HR为0.46,而303试验的PFS HR值也仅有0.51,与对照组相比曲线很快分开,4个月PFS率,AK112在301和303试验中分别有90%、80%左右,而对照组对应仅有70%、60%左右,不仅如此,两个临床试验随着时间的推移,整体分开趋势仍非常明显。
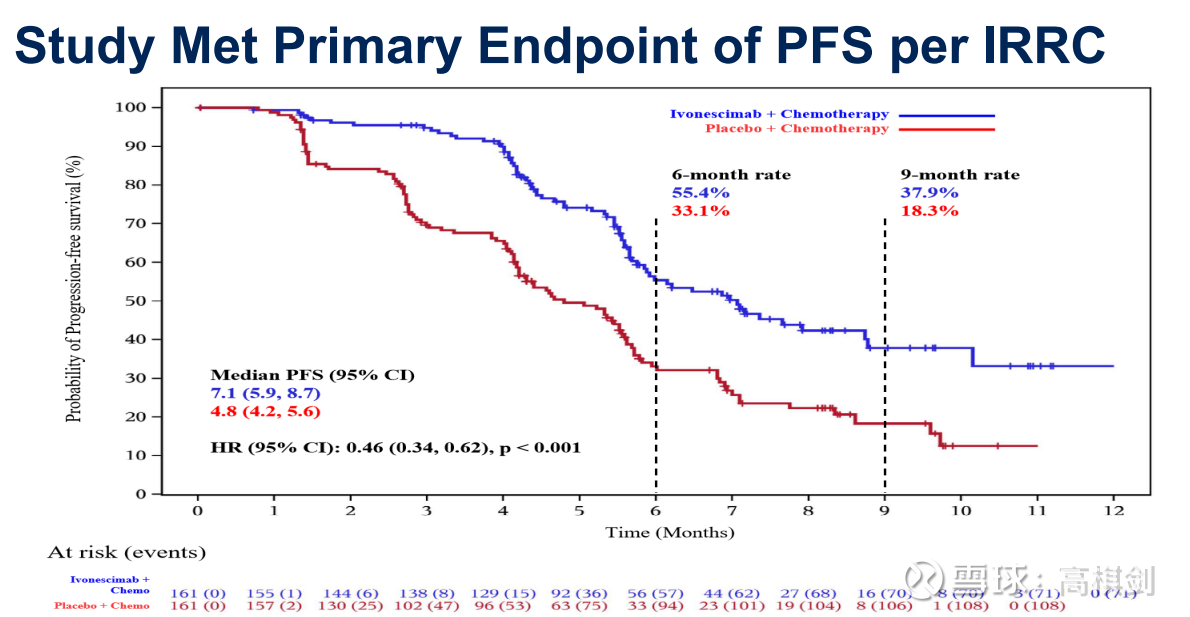
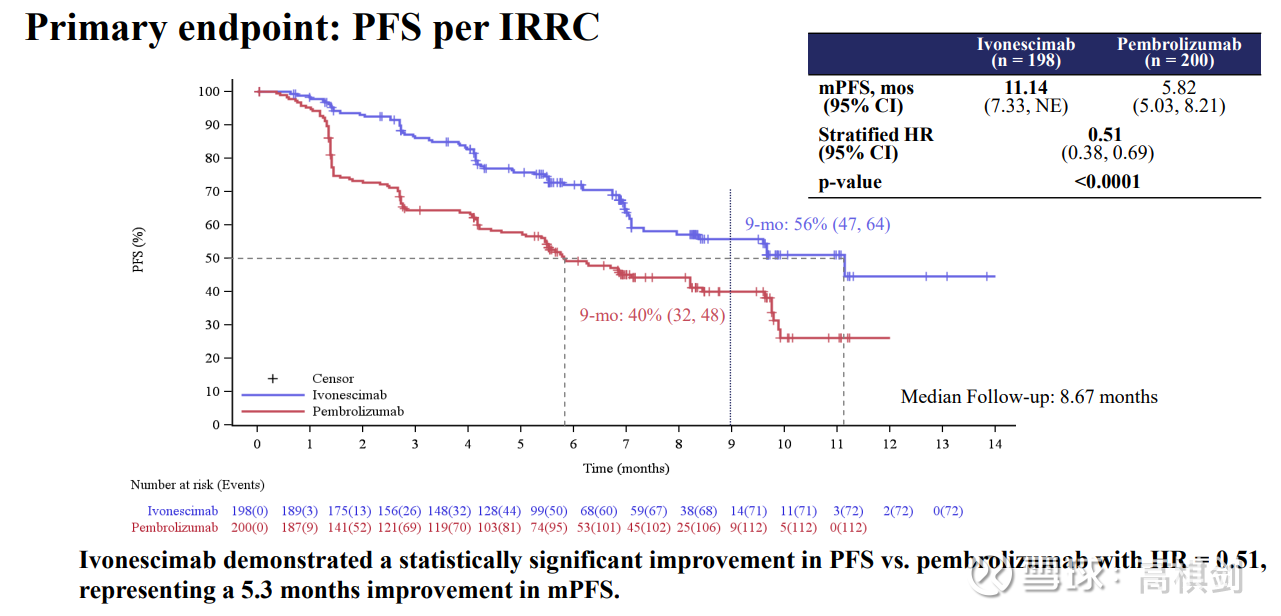
PFS的延长幅度,301试验为2.3个月,而303试验则达到5.1个月。
PD1/VEGF双抗相对于PD1单抗而言,在ORR尤其是PFS方面的确实现了很大的突破,HR值都低至0.5左右,实现了历史性的突破!
2.3 PD1/VEGF双抗的OS局限性
那么问题的核心在于AK112这些试验的OS如何,毕竟我们知道首先OS才是肿瘤治疗尤其是实体瘤治疗的黄金标准,而且K药等PD1的强项就是在很强的拖尾效应带来远超PFS改善幅度的OS大幅延长!
首先出结果的是301试验,mOS在试验整体52%成熟度时,AK112联合化疗对比化疗,OS从14.5个月延长至17.1个月,延长大概2.6月,值得注意的是,OS延长幅度(2.6个月)与其PFS延长幅度(2.3个月)基本相当,其表现与上述贝伐珠单抗的特征一致,完全符合上述VEGF靶点的特征,即基本上没有很强的拖尾效应,值得注意的是这还是头对头化疗(下文还会提到)!
说实话,当初看到这个数据的时候我也是大吃一惊,但后来想,EGFR的TKI经治NSCLC,在经过长时间TKI治疗后,本身T细胞是严重耗竭且浸润不足的,无法实现公司宣称的双重富集作用,所以AK112主要还是当一个减毒版VEGF存在,这个不会是AK112的优势适应症,而这个适应症的OS效应也许也不代表AK112给患者的生存获益能力!
而最能显示AK112对于生存获益程度的适应症是303试验,毕竟针对的是PDL1表达阳性的NSCLC,而NSCLC也是当初贝伐珠单抗的获批适应之一,最能够体现PD1/VEGF双抗的双重富集作用,而且是单药与K药单药的头对头对比,也排除了其他药物的干扰!
其结果在2025年4月27日公布:39%成熟度时期中分析,OS 的HR = 0.777,降低死亡风险22.3 %,在本 次 分 析α分配值僅為0.0001的情况下没有达到统计学显著性,SMMT股价也因此大跌36%。
这个数据在一定程度上是低于我预期的。客观上来说,这次期中α分配值给的很低,所以暂时没有达到统计学优势确实不重要。但HR值高达0.777,即使加大样本量且HR值能够保持不变,其OS即使达到统计学优势也可能仅是堪堪压线。
但关键的是随着时间的推移,303试验的OS逐步成熟后,这个HR值会上升还是会下降呢?这个又成了另一个关键之处!
我们认为随着时间的推移及OS的逐步成熟,HR值预计也将进一步上升,死亡风险下降程度继续缩窄,使得OS获得最终统计学优势将特别富有挑战性性,其原因如下:
2.3.1 301试验的指示性作用:301试验AK112基本没有拖尾效应,而且随着试验数据成熟度上升之后,其HR值反而上升了:
在30%成熟度时,HR0.72,数据其实还可以的:
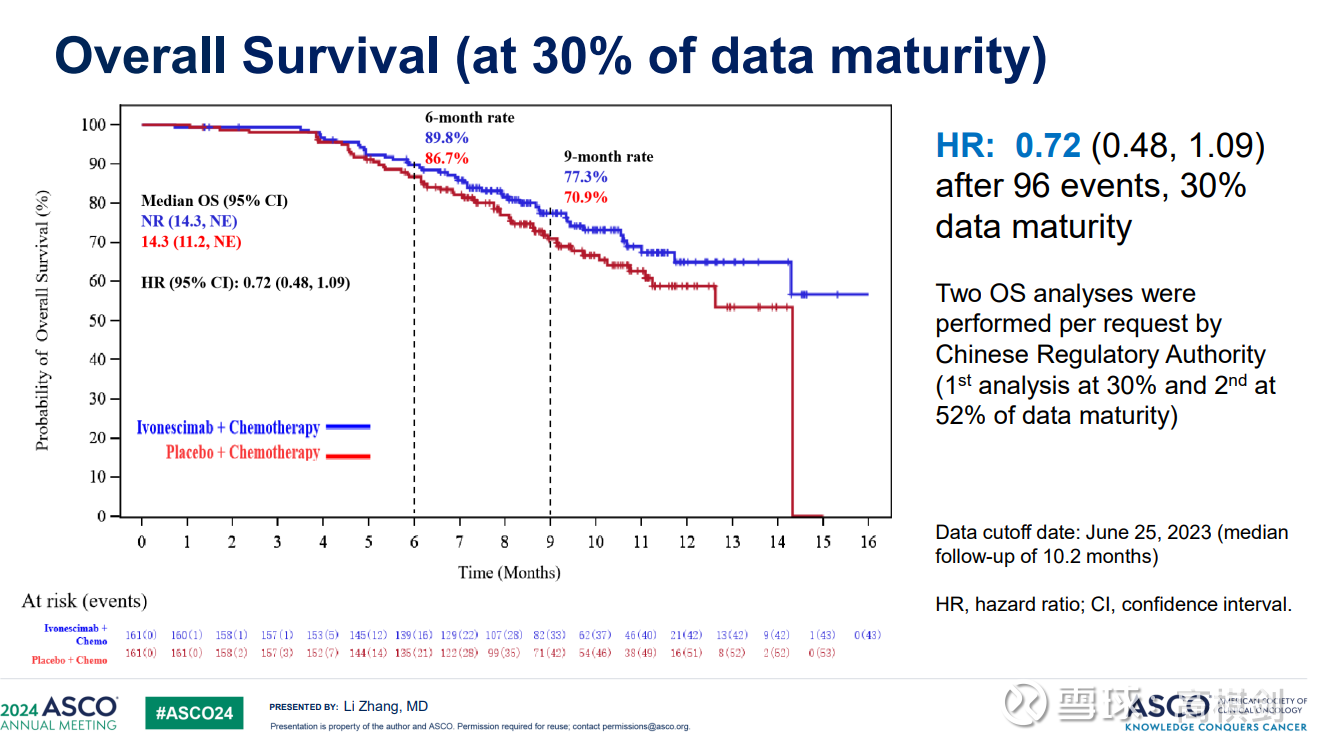
但随着时间的推移,OS的HR值居然上升了,从30%成熟度时的0.72上升到52%成熟度时的0.8!
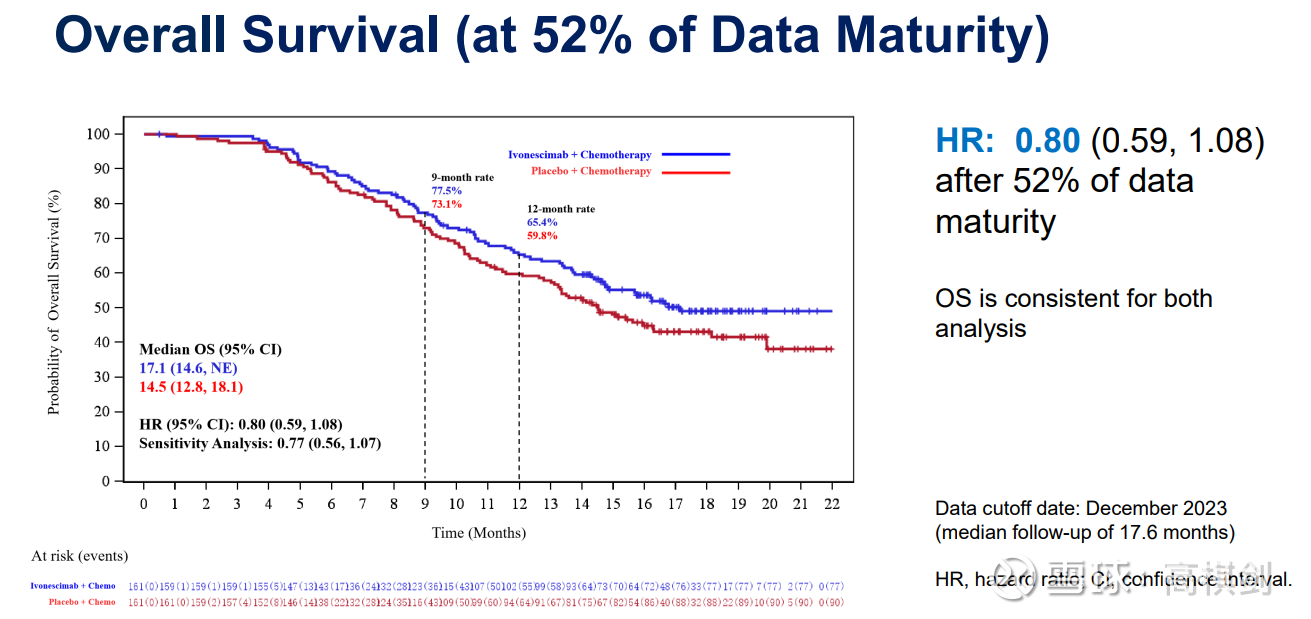
也就是说在30%成熟度时候,AK112+化疗对比化疗,死亡风险下降28%(总样本320,则AK112组死亡40,对照组死亡56),而52%成熟度时,死亡风险下降20%(总样本320,则AK112组死亡74,对照组死亡92),也就是说301试验从30%-52%的成熟度阶段中,AK112组死亡34例,而对照组死亡37例,AK112+化疗在此阶段死亡速率与化疗组相当!
值得注意是是301试验是头对头化疗,而化疗是出了名的没有拖尾效应,301试验中AK112对化疗都没有显示出拖尾效应,而303试验头对头的是具有强拖尾效应的K药,从药理病理上来说,拖尾效应会更加不明显!
2.3.2 AK112组的ORR和DCR明显高过K药组,意味着AK112组在早期死亡患者群体中优势将更加明显
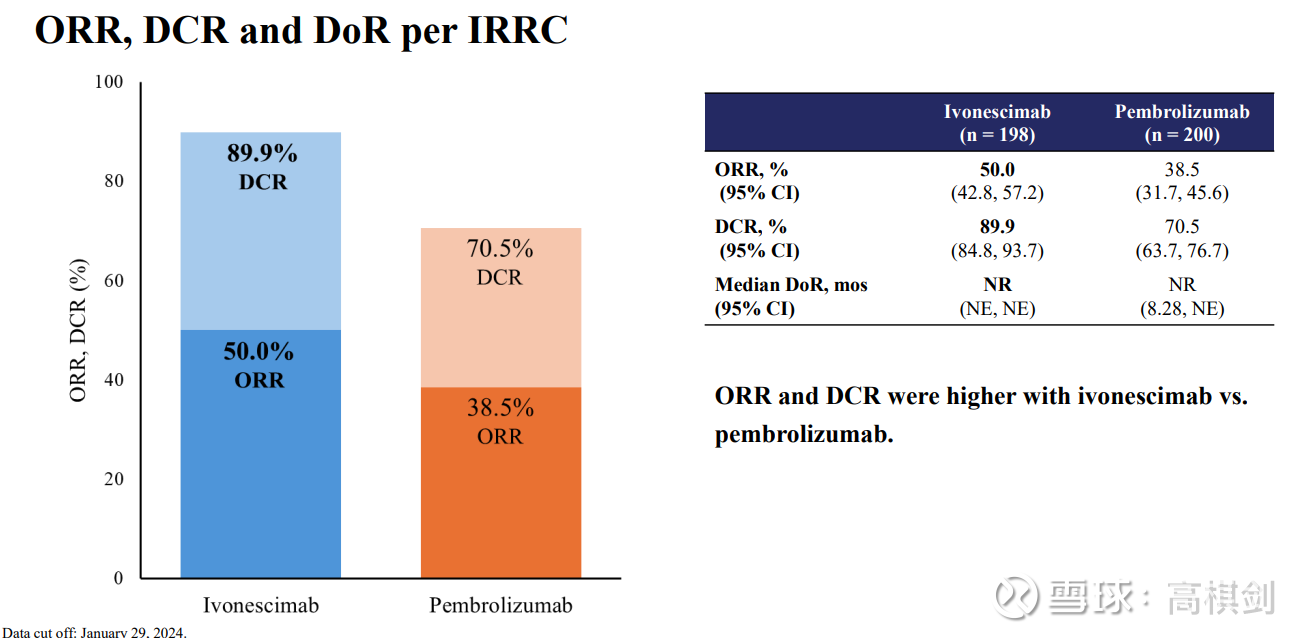
这个和PFS曲线是相对应的,也就是AK112在早期疗效中,缩瘤和疾病控制效果会显著好于K药组,K药组DCR70.5%意味着K药组大概有30%左右的患者,在首次肿瘤评估中即出现肿瘤进展,这部分患者预计生存期会比较短,更加容易出现在早期死亡的患者名单中,而AK112组的DCR接近90%,只有10%左右的患者更容易出现在早期死亡名单中。因此,理论上在OS事件成熟度比较低时,也就是在早期死亡的患者群中,AK112的死亡风险下降程度会明显更高,优势将更加明显,然而即使在这部分群体中,死亡风险也就下降22.3%!而这也是我看到39%成熟度时只有0.777的HR而感到失望的原因。
2.3.3 K药具有很强的拖尾效应,在后期死亡患者群体以及长生存患者群体中,预计将大幅消耗AK112的PFS改善阙值
正如我们在本文第一段分析的那样,K药等PD1单抗,患者一旦有疗效,那么其疗效会非常持久,这个与VEGF及化疗等靶点具有显著的不同。如果我们去看K药的OS曲线,以同样PDL1>=1%的NSCLC的KEYNOTE042为例,我们可以看到K药组的早期死亡速率甚至高于化疗组,但后期患者死亡速率明显下降,OS曲线逐步变得非常平缓。
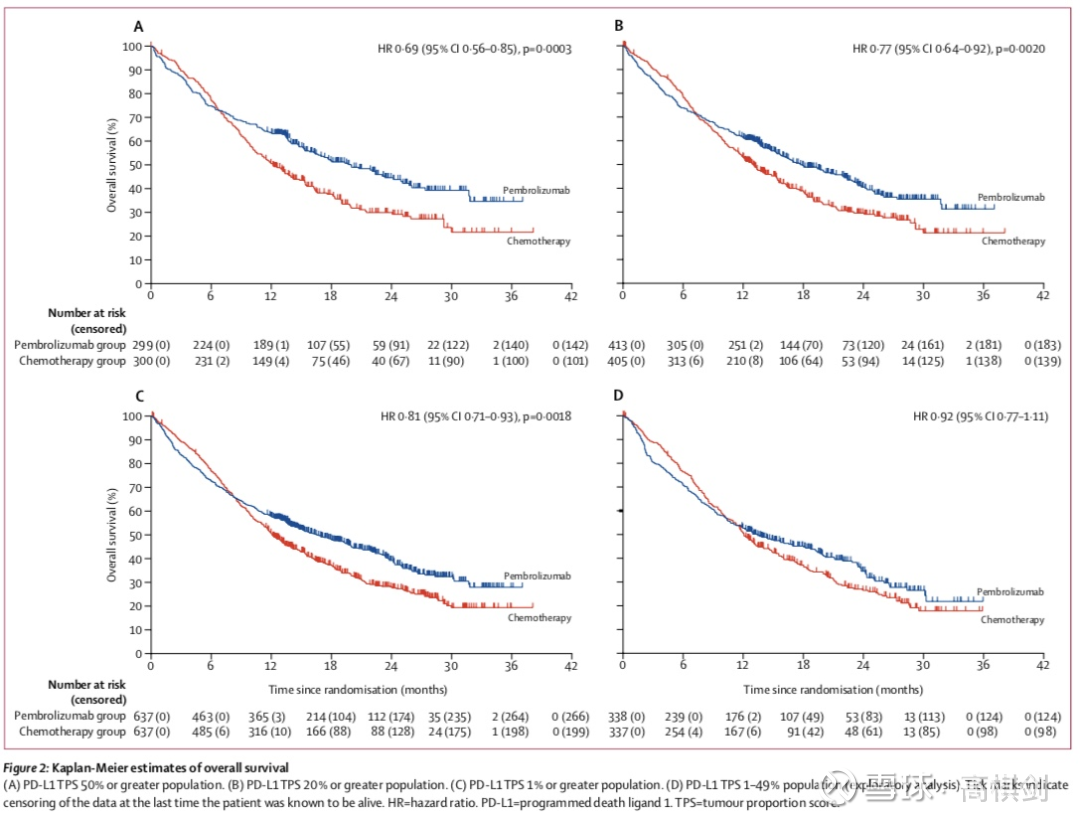
KEYNOTE042的DOR(ORR患者的疾病进展时间)达到27个月左右,而整体样本3年、5年OS率达到25%和17%,中国亚组的生存数据甚至好于海外亚组,对照组长生存获益患者会在临床后期不断消耗AK112组OS的HR值!303试验是头对头K药,K药的这种长拖尾效应意味着随着时间的推移,越晚死亡的患者群体中,AK112带来PFS带来的阙值改善将在生存期改善里越来越不显著,这也比较好理解,同样改善5个月PFS,如果患者生存期为15个月,延长5个月的话是延长了33.3%,而如果患者生存期是30个月的话,延长5个月则仅延长16.7%,两者相差一倍!
而且值得关注的一点是,PD1等单抗最大的特点是长拖尾效应,这些患者大多需要长期使用PD1单抗,而这部分患者长时间使用带有VEGF功能的AK112,会不会对其长生存获益产生影响呢?即使AK112减毒了,但如果毕竟长期使用VEGF会,会不会带来出血等问题从而影响这些长拖尾效应患者的长生存获益呢,虽然这个问题暂时没有结论,但也值得关注。
综合上面的3个论据,我们倾向于认为AK112-303试验OS的HR值随着时间的推移还将继续上升,AK112组在早期死亡患者群体中更有优势,随着时间的推移,在后期死亡患者及长生存获益群体中,优势将更加不明显,如果HR值再上升5个百分点,HR值达到0.82以上,预计就将很难做出统计学优势!
客观上来说,在免疫疗法出来之前,PFS基本上完全可以作为OS的替代指标,绝大多少临床试验在PFS阳性结果后OS都能有阳性结果,但在免疫疗法普及后就不一定了,因为免疫疗法的长拖尾效应会消耗其他药物的PFS阙值,这也是一些ADC等药物在PFS有统计学优势,但OS没有的原因,这也是在信达生物2025年研发日,周彩存教授讲ADC时提到的,ADC对疗效的改善一定程度上被PD1的长拖尾效应对冲掉了,VEGF带来的疗效加成会不会也如此呢。
如果AK112-303的OS改善幅度达到PFS的改善幅度,K药单药在PDL1>=1%的OS大概在20个月左右,如果延长5个月,OSHR值预计会在0.7左右,甚至可能更低,但现在39%的成熟度就已经0.777,我预计303试验最终OS的延长度会较明显得低于PFS的延长度。
AK112-303试验的OS存在很大不确定性,那SMMT海外进行的Hamoni-3呢会如何呢?我们认为肺鳞癌有一定概率可以压线达到OS的统计学优势,但肺腺癌预计不容易,核心是肺腺癌AK112对PFS的改善幅度还没有AK112-303试验大(AK112二期临床试验,非头对头PFS提升肺鳞癌8VS11.1,肺腺癌9VS13.3),而叠加化疗后,患者的生存期将更长(尤其是肺腺癌,OS在国内普遍达到25-30个月),预计会导致HR值可能还不如AK112-303试验。相对而言,因为肺鳞癌生存期短,PFS的改善对OS改善的传导度会更好一些,这个做出统计学优势的概率稍微大一些,但容易出血的肺鳞癌长期VEGF用药累积风险预计也不可忽视。
综上,PD1/VEGF对于NSCLC治疗在PFS取得了比较大的突破,但最终能否做出OS,虽然我们无法得到一定不行的结论,但具有比较大的挑战,容错率非常已经非常低。如果OS达不到统计学优势,那么海外价值就基本没有了,毕竟对于驱动基因阴性的NSCLC而言,已经不是无药可用的适应症,如果没有OS的统计学优势,FDA和欧洲药监局基本上是不会批准的。即使OS达到统计学优势,预计也是堪堪压线,死亡风险下降不到20%,也很难成为标准疗法!所以,我们倾向于认为PD1/VEGF一定程度上提升了PD1单抗的反应率,也延长了PFS,但对于OS的提升则缺乏拖尾效应,可以认为是免疫治疗的1.5版本,没有从根本上解决PD1单抗T细胞耗竭和T细胞浸润不足的缺点。
相对而言,也许基石药业的CS2009(PD1/VEGF/CTLA-4)三抗在OS的表现也许会好一些,毕竟加上CTLA-4后,不排除可以补上PD1/VEGF双抗在OS上的短板。但这还处于临床早期,也没法直接下结论,等待数据验证吧。
三、双免疫检查点双抗也不是答案
这部分我不打算展开讲,简单讲几句,免疫疗法无非是松刹车和踩油门,免疫检查点的作用是松刹车,目前那么多的免疫检查点,只有PD1/PDL1看到了不错的疗效,而CTLA-4其次,有点疗效,但疗效不足且毒性较大,其他如TIGHT、LAG3、CD73甚至包括CD47,在单靶点的单抗上纷纷失败,最典型的如罗氏的TIGHT,刚刚宣布停止所有相关临床试验,并且踢出管线。客观上来说,如果单抗没有额外效果,那么用PD1叠加组成双抗,预计也不会有什么明显效果,所谓我认为康方生物后面一堆双免疫检查点双抗将成药难度将比较大。
多讲几句PD1/CTLA-4双抗,类似双抗康宁杰瑞的KN046已经基本宣告完全失败,硕果仅存的是AK104。AK104在PDL1低表达的实体瘤中,相对PD1单抗,具有一些额外的疗效,尤其是OS的延长,如PD1低表达宫颈癌、胃癌和NSCLC中都是如此,但从其单药后线数据看,额外的疗效也比较一般,2024年ASCO,免疫耐药NSCLC,AK104单元的ORR仅有5-10%,由此可见叠加CTLA-4的双抗,虽有一定额外疗效,但头对头不容易做出统计学优势,所以相对于PD1单抗而言,疗效提升不大,也没有解决PD1单抗T细胞耗竭和T细胞浸润不足的问题。
四、免疫松刹车和踩油门相结合才是最优解(IBI363PD1/IL-2)
之前我们也讲过免疫疗法核心在于松刹车和踩油门,松刹车目前看起来只有PD1有不错疗效,而CTLA-4略有疗效,但免疫检查点只是起到松刹车的功能,对于大多数肿瘤患者而言,动力不足才是根本,T细胞浸润不足以及T细胞耗竭才是PD1低效或者进展的主要原因,所以,解决动力不足才是第二代免疫治疗的根本。这也是北肿郭军教授的观点,如果你车没油了动力不足,你怎么松刹车,车也开不起来!
普遍认为IL-2、IL-12和IL-15是增强免疫细胞扩增和浸润的主要激动剂,但这些激动剂都有半衰期短、用药窗口窄(剂量高了全身性毒性,剂量低了活性不够)、以及靶向性不足等缺点。全球制药届进行了很多尝试,但到目前为止,也仅有信达生物的IBI363完美地解决了这些问题,并且见到了非常好的疗效。具体病理药理分析我这里就不展开了,有兴趣的可以去阅读我以前在雪球上写的文章:
IBI363(四):二线经治及一线PDL1中低表达治疗的未来王者
在这里我仅就IBI363为什么是到目前为止,是数据上表现最好的NSCLC免疫2.0药物!
4.1 IBI363在中位三线IO经治的ORR显著高于K药在一线的数值

3mg组的IBI363在IO经治,中位三线NSCLC患者的ORR显著高于K药单药在一线的临床数据,也高于K药单药在PDL1高表达(TPS>=1%)的数据(KEYNOTE042)
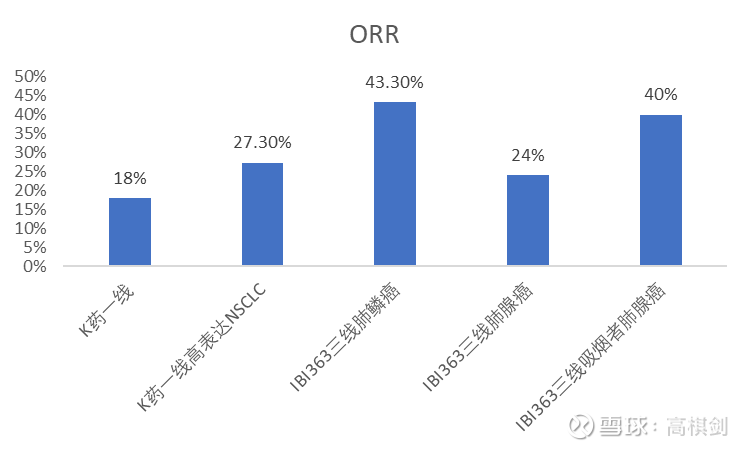
参考我们之前的文章,在后线疗效已经如此之好,推前线只会更好:
这里就不再详细展开了。
4.2 IBI363具有非常强大的拖尾效应
与PD1/VEGF双抗是靶免结合,并且相对PD1单抗不具有额外拖尾效应不同,IBI363是纯粹的免疫疗法,而且是给免疫系统松刹车的同时踩油门并且持续加油的疗法,从目前数据看,延续了免疫疗法的长拖尾效应的特征,而且因为是持续加油,疗效预计将更加持久!
具体到NSCLC的拖尾效应,我们只讲一点,虽然非头对头,但IBI363在其3mg组,单药在IO经治且中位3线的12个月OS率甚至超过了K药在一线IO初治患者且联合化疗的水平!
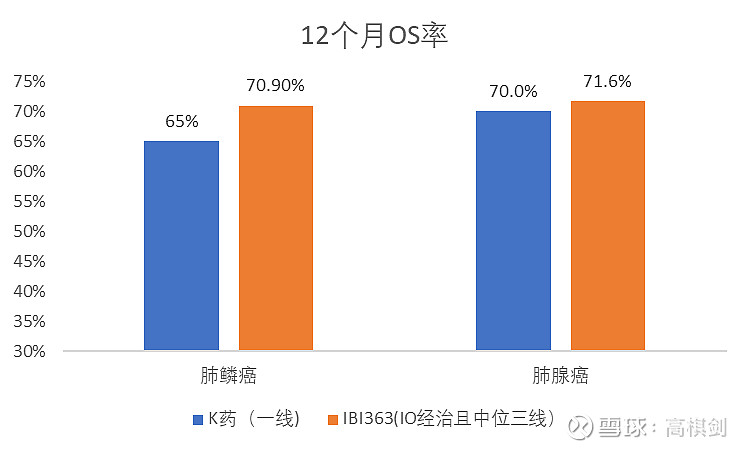
这是什么概念?首先在用药上,K药是联合化疗,而IBI363是单药;其次,K药是初治的一线患者,而IBI363本次入组的是已经用过PD1等免疫治疗,而且是前面中位经过了两线治疗!也就是IBI363在后线单药的疗效已经可以媲美K药在一线联合化疗的疗效。结论:IBI363完全具备往一线推的潜力,OS胜算很大
也有人提到维立志博的LBL-024,PD1/4-1BB双抗的数据不错。我认为IL-2直接扩增效应细胞(CD8⁺ T、NK),可以直接增强免疫细胞浸润并且对冲T细胞耗竭,而4-BB则是延长T细胞的作用时间,减缓T细胞的耗竭。所以从药理上来说,可能LBL-24对于神经内分泌瘤等特殊肿瘤具有比较好的疗效,但对于其他实体瘤预计额外疗效不会太大。
综上:对于NSCLC,K药等第一代免疫存在不足,需要免疫2.0时代来提升疗效;PD1/VEGF一定程度上提升了ORR和PFS,但OS能否达到统计学优势具有很大的不确定性,而且OS提升幅度也非常小,只能说是免疫1.5药物,属于一代药物的改良性药物;而IBI363是目前为止最好的免疫2.0药物,将有望全面取代K药等第一代免疫药物,成为免疫2.0时代的最优解!
声明:以上内容仅供学术探讨,所有分析都是基于现有数据和逻辑,结论具有不确定性,以上内容和结论概不能用于股票买卖之所用!