小核酸药物解析:从技术革命到市场机遇
小核酸药物(寡核苷酸药物)代表着生物医药领域的第三次创新浪潮,紧随小分子药物和抗体药物之后。它们通过直接干预基因表达,从源头调控疾病发生机制,有效突破传统药物的靶点限制。这类药物利用核酸序列(如RNA片段)靶向致病基因的mRNA,实现基因沉默、调控或激活,从而避免了仅作用于下游蛋白质的局限性。依据中心法则(DNA → RNA → 蛋白质),小核酸药物可视为“基因剪刀”,精准“剪断”错误指令,阻止致病蛋白的合成。这一“降维打击”策略,使许多“不可成药”的靶点成为可能,特别是在遗传病、慢性病和癌症等领域。
全球小核酸药物市场正在迎来爆发式增长。根据EvaluatePharma的数据,2023年市场规模约为46亿美元,十年后(2033年)有望飙升至467亿美元,年复合增长率(CAGR)约为25%-26%。这一增长驱动力主要源于技术的不断成熟、监管环境的优化以及临床和商业化的突破。目前已有超过18款小核酸药物获批上市,年度销售额超过10亿美元的“重磅”产品包括Spinraza(诺西那生钠,用于脊髓性肌萎缩症,SMA)和Leqvio(英克司兰,用于降血脂,长效给药)等。
提到该行业“黑暗期”(从1998-2010年),只有零星几款 ASO/aptamer药物产品,很多还被迫撤市。自2016年开始,行业进入快速商业化阶段,批准数量逐年递增,适应症也从罕见遗传病逐步扩展到高血脂、心血管疾病、乙肝、糖尿病,甚至肿瘤和眼科疾病。预计未来,随着技术成熟和市场拓展,行业将迎来更加广阔的发展空间。
核心技术平台:多元共存的治疗体系 小核酸药物并非单一技术,而是涵盖多种互补的平台。下图为不同机制的技术类型及其特点:

递送技术:核酸药物的递送是行业发展的瓶颈之一。当前成熟的技术包括:
GalNAc(N-乙酰半乳糖胺):肝脏靶向“钥匙”,结合ASGPR受体,精准递送siRNA和ASO药物。代表药物包括Leqvio和Patisiran(资料来源:Nature Biotechnology)。
LNP(脂质纳米颗粒):作为“万能快递”,包裹核酸,保护其免受降解,广泛应用于mRNA疫苗和肝外递送(如肿瘤、肌肉)。
未来挑战在于血脑屏障(BBB)突破,方法包括聚焦超声、工程化外泌体、外源性病毒载体等(资料来源:Science Translational Medicine)。
产业链与创新生态
上游:核酸单体、修饰试剂和合成平台。国内企业如键凯科技(修饰核苷酸)、凯莱英(CDMO)等在不断提升自主研发能力,但高端修饰技术仍依赖进口。
中游:新药研发与生产。国内企业如悦康药业、福元医药、石药集团已布局多平台研发,部分已进入临床阶段。
下游:商业化与市场应用。中国市场逐步向肿瘤、慢性病延伸,乙肝和心血管疾病成为主要方向。
未来趋势:从小众到主流
>适应症扩展:逐步覆盖罕见病到常见慢病,未来可能实现多药联合疗法(如小核酸+抗体)。
>靶点升级:除肝脏外,逐步突破血脑屏障和其他组织靶向。
>个性化治疗:利用基因测序实现“N-of-1”定制(如Milasen),未来针对突变亚型的精准药物将成为趋势。
>技术多元化:siRNA、ASO、mRNA等平台共存,推动创新生态系统成熟。
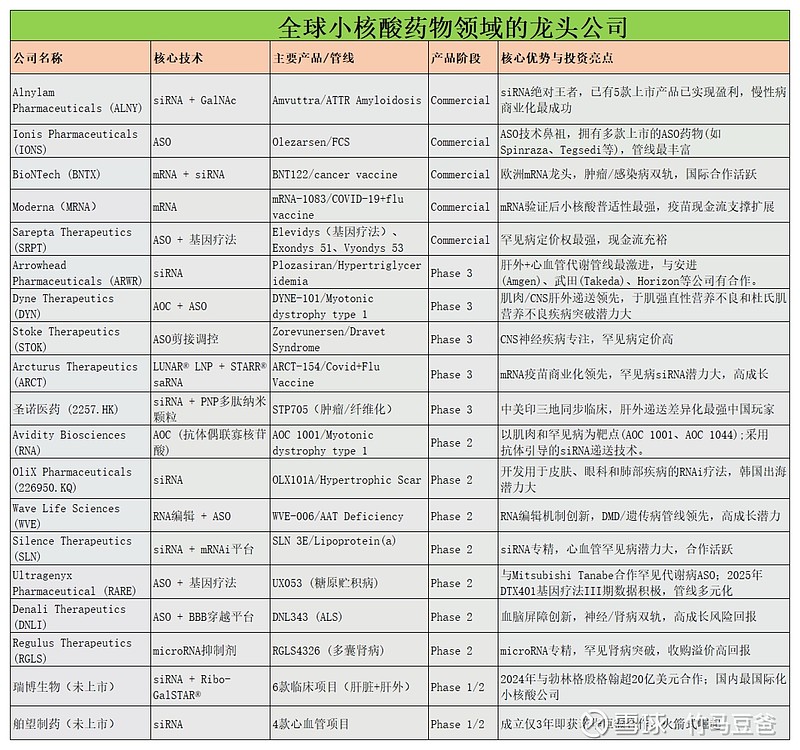
>全球格局:欧美企业领先(Ionis、Alnylam),中国企业快速追赶,逐步实现国际化布局。
总的来看,小核酸药物正引领基因疗法的变革,从基础技术到临床应用不断突破,重塑医药未来。如果你想押注未来十年的生物医药,对于这些小核酸药物领域的龙头公司们,不妨多花点时间盯一盯。