【万邦德002082】原研药MCR环肽开辟糖尿病视网膜病变,突破抗VEGF药物局限进军潜在数百亿新赛道
$万邦德(SZ002082)$ 原研药MCR环肽开辟糖尿病视网膜病变多通路治疗新策略,突破抗VEGF药物局限进军潜在数百亿新赛道
糖尿病视网膜病变(DR)是糖尿病最常见且严重的微血管并发症之一,也是各年龄人群(包括儿童、工作成年人和老年人)主要的致盲原因1。2020年,全球有超过1.03亿人受到糖尿病视网膜病变的影响,预计到2045年这一数字将上升到1.61亿人1。这一延续多年的临床痼疾,正被一项中国原创突破所撼动。近日,据悉万邦德制药集团有限公司(以下简称“万邦德”)自主研发的创新小分子环肽药物(MCR环肽)在糖尿病视网膜病变治疗领域取得临床前重大突破。
一、糖尿病视网膜病变的治疗困境
糖尿病视网膜病变是一种进展性眼部疾病,长期高血糖会导致视网膜微血管损伤,引发视网膜缺血缺氧,进而促进病理性新生血管形成,造成视网膜增殖性病变2。目前,抗VEGF药物和激光光凝术是治疗DR的金标准疗法,但存在需要频繁眼内注射、部分患者应答不佳等问题,亟需新型治疗策略1。
近年来的研究发现,黑皮质素系统(Melanocortin System)在调节炎症反应、促进组织修复和维持内环境稳定方面发挥关键作用3,为DR治疗提供了新思路。
二、万邦德MCR环肽:
对视网膜结构保护效果显著
万邦德研发的MCR环肽在DB/DB糖尿病小鼠模型中表现出显著的视网膜保护作用。
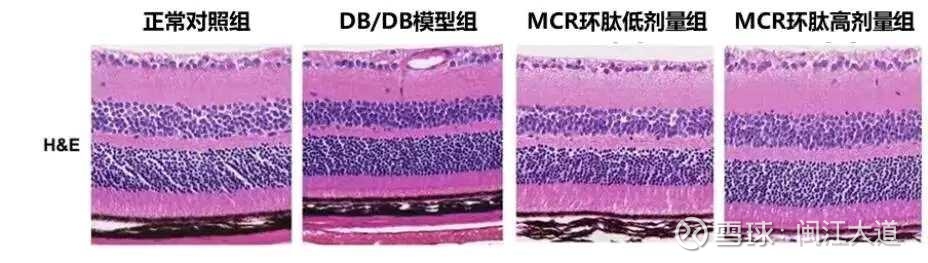
图1. 组织学观察(H&E切片)
实验结果显示,DB/DB模型小鼠的内核层(INL)和外核层(ONL)厚度明显变薄,这是糖尿病引起视网膜变性的典型特征。而经过MCR环肽治疗后,视网膜结构得到明显改善:
1. MCR环肽低剂量组和高剂量组显示剂量依赖性的视网膜结构恢复;
2. MCR环肽高剂量组的ONL厚度恢复接近正常水平。
三、多重机制协同作用
万邦德MCR环肽的核心优势在于其多靶点作用机制。它模拟了内源性黑皮质素(如α- MSH)的生理功能,通过激活眼中的黑皮质素受体,从炎症、血管、屏障和神经等多个关键环节协同发挥作用1, 4。

图2. α-MSH受体在眼睛中的表达和功能 (来源:参考文献5)
强效抗炎与免疫调节
糖尿病视网膜病变本质上是一种慢性低度炎症性疾病。研究证实,激活MCR,特别是MC1R,能够显著抑制核因子κB(NF-κB)等关键促炎信号通路的活化5。这导致多种促炎因子(如TNF-α, IL-1β, IL-6)和趋化因子(如MIP-1α, MIP-2)的表达下调4。更重要的是,MCR激动剂能诱导具有抗炎功能的调节性T细胞(Treg)的生成,并促进抗炎细胞因子IL-10的表达,从而将免疫反应从破坏性的促炎状态转向保护性的抗炎和修复状态4, 5。此外,在糖尿病视网膜病变模型中,MCR激动剂还被证明可以促进巨噬细胞从促炎的M1表型向抗炎、促修复的M2表型极化,这有助于炎症的消退和组织修复4。
抗血管生成与减轻渗漏
除了抑制炎症,MCR激动剂能够直接作用于血管系统。研究表明,激活MC4R可以拮抗视网膜微血管内皮细胞的高通透性5。同时,激动MC1R能显著降低视网膜中血管内皮生长因子(VEGF)的水平,这是驱动病理性新生血管形成和血管渗漏的关键因子4。这种通过调节内源性通路来抑制VEGF的独特机制,与现有的抗VEGF药物形成互补,可能为解决抗VEGF治疗耐药性问题提供新策略。
稳固血-视网膜屏障
血-视网膜屏障的破坏是糖尿病视网膜病变血管渗漏和视网膜水肿的病理基础。MCR激活可显著增加视网膜中紧密连接蛋白(如Occludin)的表达,从而从结构上加固血-视网膜屏障,减少血浆成分的渗漏4。
直接细胞保护与抗凋亡
MCR的细胞保护作用超越了血管和炎症细胞,直接惠及视网膜神经元。α-MSH已被证明能够通过激活MC1R及其下游的Akt/mTOR和Erk1/2 MAPK信号通路,保护视网膜色素上皮细胞免受氧化应激诱导的凋亡5。在缺血/再灌注损伤模型中,MCR激动剂显示出对视网膜神经节细胞的显著保护作用,减少细胞凋亡,这对于防止糖尿病视网膜病变中的神经变性至关重要。
四、前景展望
糖尿病视网膜病变的治疗正处在一个转型期,从单一的VEGF抑制向多靶点、全方位保护的方向发展。万邦德的MCR环肽药物凭借其独特的作用机制和令人鼓舞的临床前数据,有望成为这一领域的重磅产品,为全球数亿DR患者带来新的治疗选择。
文章来源于药时代公众号