普方生物再撕开一条口子



近日,Genmab宣布,FDA已授予其在研ADC药物rinatabart sesutecan(Rina-S)突破性疗法认定,用于治疗在含铂方案及PD-(L)1治疗后仍出现复发或进展的子宫内膜癌(EC)成年患者。
要知道妇科肿瘤领域一向是国内外头部药企布局的重中之重,从HER2到CDK4/6、PARP等靶点均诞生过销售额超几十亿美金的超级重磅炸弹。
对于Genmab来说,Rina-S的销售峰值也预计超过20亿美元,可以算是近两年的重中之重。
需要额外注意的是,该药由普方生物原研,后来Genmab以18亿美元收购了普方生物,才将Rina-S收入囊中。而早在收购半年前,2024年1月,Rina-S就已经被FDA授予快速通道资格。
在普方生物自身的ADC技术平台优势得以验证的基础上,再次用注入Genmab血液里的管线证明实力,在肿瘤领域撕开一条口子。
01
掘金妇科肿瘤

卵巢癌和子宫内膜癌作为常见的妇科恶性肿瘤,全球发病率逐年上升。其中子宫内膜癌的发病率仅次于宫颈癌,居女性生殖系统恶性肿瘤的第二位。2023年,全球子宫内膜癌新增病例数约为40.1万例。
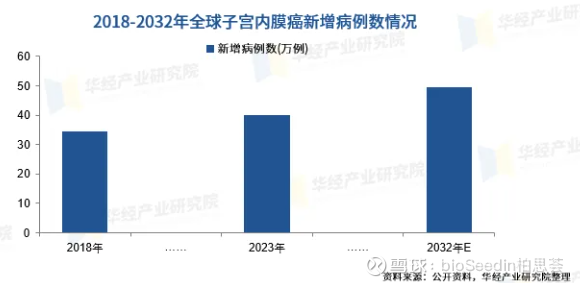
另一边,卵巢癌的发病率也不容乐观,据数据预测,到2030年,全球卵巢癌发病人数将达到37.4万人,中国患者人数将超过6万人。
虽目前铂类药物的应用为以上患者打开了治疗窗口,但是铂耐药复发,并且无基因突变的情况,却没有太好的治疗手段。在此情况下,新时代需要诸如ADC类型的新药进行破局,为妇科肿瘤患者带来全新的希望。由此,FRα靶点ADC应运而生。
FRα作为典型的在肿瘤组织中过表达,但是在正常组织中表达较少的靶点,在上皮性卵巢癌中约为76-96%,在子宫内膜癌约为20-81%;在三阴性乳腺癌中约为35-80%。
2024 年 3 月 22 日,艾伯维宣布FDA已完全批准Elahere用于治疗FRα阳性、铂类耐药的上皮性卵巢癌、输卵管癌或原发性腹膜癌患者。该药物作为全球首款批准用于治疗这种难以治疗恶性肿瘤的药物,是艾伯维于2023年11月30日豪掷101亿美元收购ImmunoGen公司所得核心产品。
而Rina-S目前作为在研管线中进度最快的产品,已进入临床3期阶段。
根据Genmab官方公告来看,此次突破性疗法认定的依据是此前公布的 1/2 期多部分 RAINFOL™-01 试验(临床试验编号:NCT05579366)中子宫内膜癌单药治疗剂量扩展 B2 队列的研究结果。

该试验旨在评估 Rina-S 在实体瘤中的安全性和有效性。在 B2 队列中,共入组 64 例经多线治疗的晚期或复发性子宫内膜癌患者,这些患者均在接受抗 PD-(L) 1 疗法和含铂化疗后疾病进展,且均接受了 Rina-S 治疗。
其中,在22例接受100 mg/m²剂量治疗的患者中,确认的ORR为50.0%,疾病控制率为100%;而在34名接受120 mg/m²剂量治疗的患者中,ORR为47.1%,47.1%的患者获得部分缓解,38.2%的患者疾病获得稳定,疾病控制率为85.3%。
另外在卵巢癌患者中,虽Elahere作为FRα ADC上的FIC已经连续商业化两年,但因为安全性等局限因素商业化未发挥出该靶点的全部潜力,而Rina-S则有潜力在该方面进行突破。
事实上,在SGO 2025大会上公布的Rina-S针对卵巢癌患者最新数据,也切实的为Genmab注入了一针强心剂。
从结果来看,最亮眼的是120mg/m²,Q3W治疗组的疗效——在18名接受治疗的晚期卵巢癌患者中,4例CR(2名确认;2名未确认),8例PR,ORR为66.7%,确认的ORR为55.6%,DCR为88.9%,mDOR尚未达到(中位随访时间48周)。
可见,与Genmab在2024 ESMO上公布的数据(ORR为50%)相比,Rina-S高剂量组的疗效有了进一步提升。并且更值得关注的是,该临床研究并未限定入组患者的FRα表达水平(此前接受过Elahere治疗的患者除外),而FIC药物Elahere则受限于FRα高表达(FRα TPS>75%)患者,因此Rina-S有望面向更多患者。
02
管线进度第一梯队

回看Genmab收购普方生物这笔交易,除了Rina-S外,还使Genmab获得全球范围内拥有三个临床开发候选药物的权利,其中一款则为一种靶向PTK7的ADC PRO1107。
PTK7作为一种存在于细胞表面的受体蛋白,属于受体酪氨酸激酶超家族。它在正常上皮、内皮和造血组织中普遍低水平表达,但在多种上皮癌(结直肠癌、乳腺癌、肺癌、食道癌等)、肉瘤以及血液癌症中过表达。
基于这一特性,使PTK7成为了ADC开发的潜力靶点。
回望之前,PTK7 ADC的开发十分曲折,艾伯维、辉瑞曾一同牵手探索PTK7 ADC Cofetuzumab Pelidotin之路,但后来却先后终止管线开发,原因猜测也是因为疗效表现未达预期且安全性问题突出。
但尽管如此,PTK7靶点因在肿瘤治疗中的潜力,仍吸引着其他药企如礼来等继续投入研发,并在该赛道有不少并购合作案例。
如2024年6月,Day One Biopharmaceuticals宣布,以12亿美元引进中国公司Mabcare Therapeutics与普众发现共同开发的靶向PTK7 ADC新药MTX-13的大中华区外全球权益;而Genmab18亿美元收购普方所得的PRO1107则是另一起PTK7 ADC交易事件。
在以上处于临床阶段的PTK7单抗ADC之外,百奥赛图提前布局了多款双靶点ADC,其中PTK7/B7H3双靶点ADC药物BCG034也在2024年7月授权给IDEAY,此外还有PTK7/EGFR、PTK7/TROP2等两款双靶点ADC处于临床前阶段。
从全球竞争格局来看,包括礼来的LY4175408在内,共有4款PTK7 ADC处于临床阶段,其中进展最快的当属科伦博泰的SKB-518与普方生物的PRO1107,前者已经率先启动2期临床,后者也处于临床1/2期。
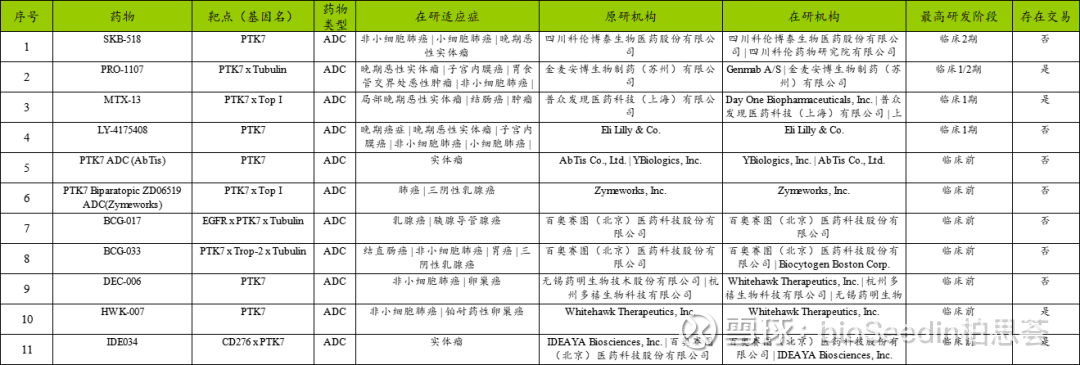
目前在研PTK7 ADC管线
数据源:智慧芽新药数据库
可以见得,处于临床活跃阶段的PTK7 ADC还尚未公布临床数据,但已经有多款药物达成了交易,可见随着技术平台的升级,业内十分看好PTK7 ADC的潜力。
未来1-2年,随着早期临床数据的读出,以及双靶点ADC进入临床,PTK7靶点有望进一步验证其治疗实体瘤的潜力,并可能催生新一轮交易。