js001sc数据解析

写之前本想着几句话说明白,但没想到越写越多,越写越乱,本就不是专业的,还是以能看懂为主。下面开始进入正题。
首先最重要的便是数据,但是数据归数据,也要看从哪个适应症上做出来的数据,就像新能源车的续航,官方标准700公里,实际使用时可能只有400公里,到了冬天可能只有300公里。 但是也要看是多大的电池跑出来的,理论上电池越大续航越远,但是电池大了车子越安全吗?
先看试验结论,数据来源于官方公众号,JS001sc的药物暴露量非劣效于JS001的药物暴露量:两组第一周期实测Ctrough和模型模拟的第一周期AUC0-21day的几何均值比(GMR)分别为1.30(90%CI:0.99-1.70)和0.91(90%CI:0.86-0.95),均达到预设的非劣效标准。
想看懂这组数据,就要了解2个关键名词和他们之间的关系。那就是药物暴露量和谷浓度Ctrough。
这个涉及的是药代动力学中最底层的逻辑。 我们可以把药物在体内的代谢过程,想象成一场水库泄洪与下游灌溉的系统工程。
一、 药物暴露量:“总弹药量” 1. 科学定义: 在药代动力学中,药物暴露量通常用“药时曲线下面积”(AUC, Area Under the Curve)**来衡量。如果在坐标轴上,横轴是时间(t),纵轴是血药浓度(C),那么 AUC 就是这条浓度曲线与横轴所围成的总面积。 临床意义: AUC 代表了在整个给药周期内(比如js001sc的 21 天),真正进入患者全身血液循环的“有效药物总分子数”。 总体来说,AUC 必须达到一个基础阈值,药物才能发挥足够的抗肿瘤作用。 但这个数值也不是越大越好,他也是一个衡量系统性毒性的指标: AUC 越大,意味着肝脏、肾脏以及免疫系统需要代谢和承受的药物总负荷越重。对于单抗类药物,过高的 AUC 往往与严重的全身性免疫相关不良反应。
二、 谷浓度,“底线防御力” 1. 科学定义: 谷浓度是指在连续多次给药的方案中,在下一次给药前那一瞬间,血液中药物浓度的最低点。 2. 临床意义: 对于 PD-1 这种依靠“受体阻断”来起效的免疫药物,谷浓度是维持疗效最核心的生命线。免疫药必须持续结合在 T 细胞表面的 PD-1 受体上,才能防止肿瘤细胞逃逸。如果谷浓度太低,受体结合率就会下降,肿瘤细胞就会在下一次打药前的这段“火力真空期”内疯狂反扑。防守底线: 谷浓度决定了药物在整个周期末尾的“底线压制力”。只要谷浓度维持在有效治疗浓度之上,就能实现 24 小时不间断的全天候免疫激活。
三、 系统博弈:暴露量与谷浓度的关系 这两个指标不是孤立的,它们由给药途径(静脉 IV vs 皮下 SC)和药物的吸收、分布、消除速率共同决定。它们之间存在着一种动态的“妥协与重塑”关系。 1. 静脉输注(IV)的系统特征:高 AUC,低谷浓度,极高且危险的峰值 当静脉打点滴时,药物是 100% 瞬间进入血液的生物利用度 100%。 瞬间会产生一个极其巨大的浓度峰值(C_{max}),这导致 AUC 也很高。但随着血液循环和代谢,浓度在 21 天内呈现指数级衰减。 弊端: 那个巨大的峰值不仅对受体占位毫无额外帮助(因为受体早就饱和了),反而会引发强烈的毒副作用。而在第 21 天时,浓度已经掉到了很低的位置(谷浓度偏低)。 2. 皮下注射(SC)的系统重塑:削峰、平谷、牺牲小部分 AUC 当药物打入皮下脂肪和肌肉之间的间质层时,系统逻辑完全变了。皮下组织就像一个缓释水库储库效应,(就像光伏储能一样),药物大分子必须缓慢地通过淋巴毛细管网渗透进血液。药物在皮下停留的这几天里,会被皮下组织中的蛋白酶降解吞噬掉一部分。这也是为什么君实 JS001sc 的 AUC 是静脉版的 0.91。 消失的那 9%,是在皮下被降解掉的,并没有进入血液。 虽然总药量变少了,但由于皮下组织在 21 天里像个吊瓶一样持续不断、极其缓慢地往血液里滴药,这就完美削平了早期的高危峰值(C_{max} ,并把原本会被快速代谢掉的药物,均匀分配到了整个周期的中后段。 看试验结果: 虽然总体流过的水(AUC)少了 9%,但在第 21 天测水位时(谷浓度),水位反而比静脉注射高出了 30%(1.30)。 不盲目追求过高的 AUC,过高的 AUC 意味着毒性。我认为用 0.91 的 AUC 换取安全性,是极具性价比的系统妥协。 1.30 的谷浓度,相比静脉版还高出了30%的浓度。 所以,二者的关系在皮下制剂的研发中可以概括为:通过控制吸收速率(牺牲一点无效的 AUC 峰值),换取周期末端更强大、更持久的受体饱和度(高谷浓度)。
看完了解释再看它的数据,“90%CI”代表的是 90%置信区间(Confidence Interval)。它后面的那两个数字(比如 0.99-1.70),分别代表了这个区间的下限”和“上限。 这两个数字的“临床大白话”翻译 以 Ctrough(谷浓度)的 GMR 为 1.30(90%CI:0.99-1.70)为例,1.30 是“点估计值”: 也就是这次几十或上百人的临床试验跑出来的一个平均比值。皮下版是静脉版的 1.3 倍。 0.99-1.70 是“真实世界的容错范围”: 统计学的意思是,如果把这个药推向全中国所有的晚期肺癌患者,我们有 90% 的把握,皮下版的真实谷浓度比值,绝对会落在 0.99倍 到 1.70倍 这个区间里兜底。 做皮下(SC)对比静脉(IV)的药代动力学(PK)桥接试验,药监局(FDA/CDE)通常会预设一个非劣效界值,行业里最常用的标准线是 0.8(即 80%)。 药监局通常会盯着你括号里的第一个数字(下限): *通关铁律: 只要你 90%CI 的下限严格大于 0.8,就判定你“非劣效达标”,就会很容易批药了, 翻车标准: 如果你的下限掉到了 0.79,哪怕你的平均值是 1.0,也会被无情拒批,因为存在跌破底线的风险。 谷浓度(Ctrough):1.30(90%CI:0.99-1.70)下限是 0.99。 0.99 远远大于 0.8 的及格线,这说明在最极端、最差的情况下,它的谷浓度也几乎和静脉版(1.0)一模一样,而上限甚至能飙到 1.7 倍。安全垫极其厚实。 暴露量(AUC):0.91(90%CI:0.86-0.95)下限是 0.86。 虽然平均暴露量比静脉版少了9%,但它最差情况下的底线是 0.86,依然稳稳踩在 0.8 的红线之上。总结论:为什么说“均达到预设标准”? 因为这两组数据的下限(0.99 和 0.86)全部大于监管机构要求的底线(0.8)。括号里的数字,其实就是给药监局吃的一颗定心丸,证明这款药在绝大多数患者身上,即使吸收再差,也不会发生“药效断崖式下跌”的情况。
为了更充分的说明,我专门做了一个表格,大家先对比一下已经上市的这几款我认为比较有说服力的单抗皮下制剂药物,有PD1和PDL1。先看一下做三期试验时SCvsIV的剂量问题,我认为不看电池的大小光比较续航实在是耍流氓。。。
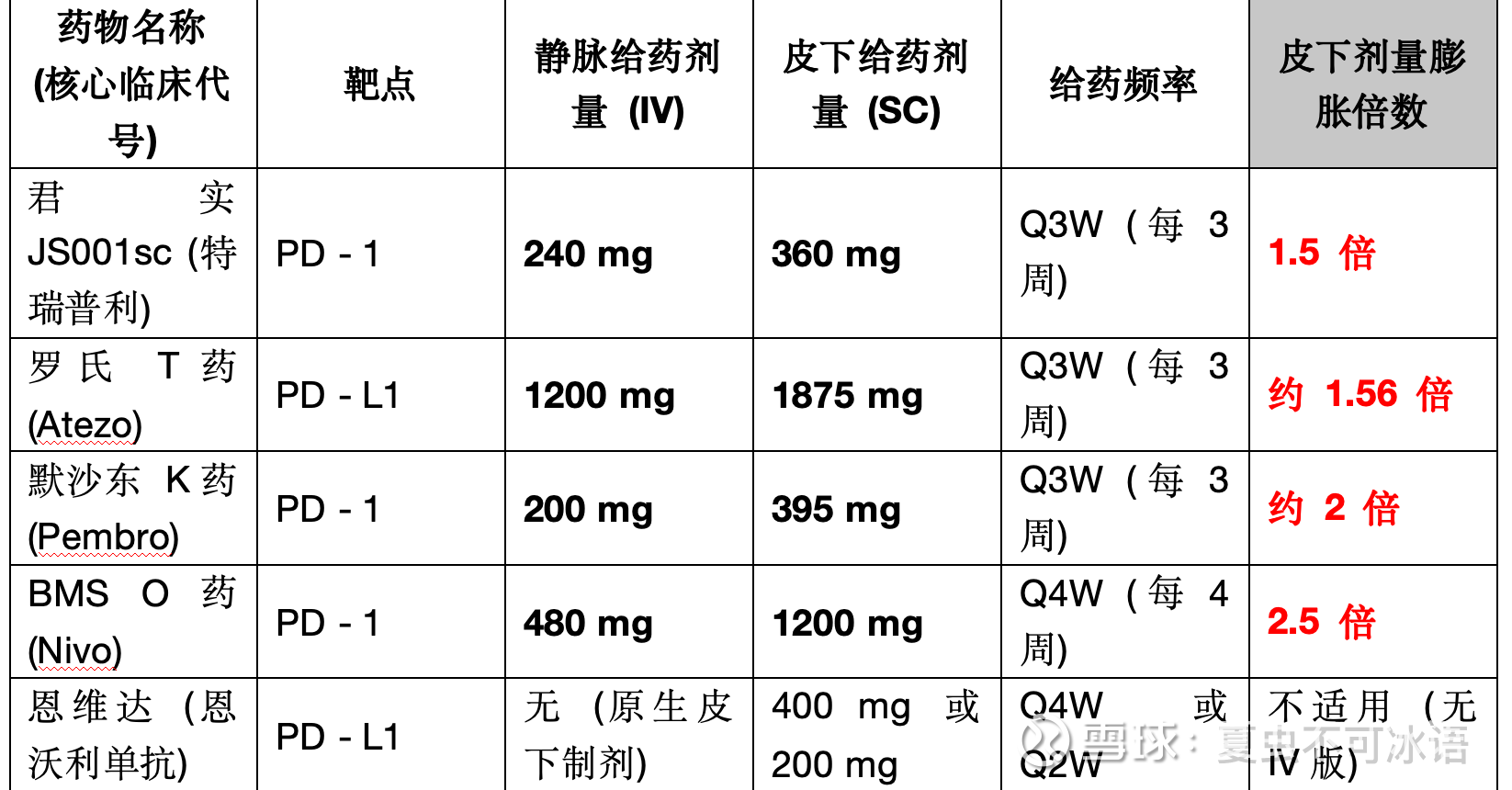
OKT加一个国产的第一个上市恩沃利,非常有说服力了吧。皮下版单次的剂量一定是要超过静脉注射版的,上述也做过说明药物在皮下停留的这几天里,会被皮下组织中的蛋白酶降解吞噬掉一部分。因此,如果不成倍增加剂量,皮下注射的总暴露量(AUC)通常只有静脉注射的 60% - 80%。
但看看上述图中,除了恩沃利在设计初期就是做的皮下制剂,OKT药在3期试验中的剂量,是非常高的,O药的480mg,其实是240mg单次,Q2W,4周就是注射2次,如果算一次的倍数,甚至已经达到了5倍…O药的策略,想降低频率,增加便捷性,就猛猛提升了剂量… 下面要呈现的表格,也可以看到他的数据是很惊人的。K药2倍,T药1.5倍都还好。大家带着这个试验时的剂量,进入下一个环节,对比一下这几款的初步数据。
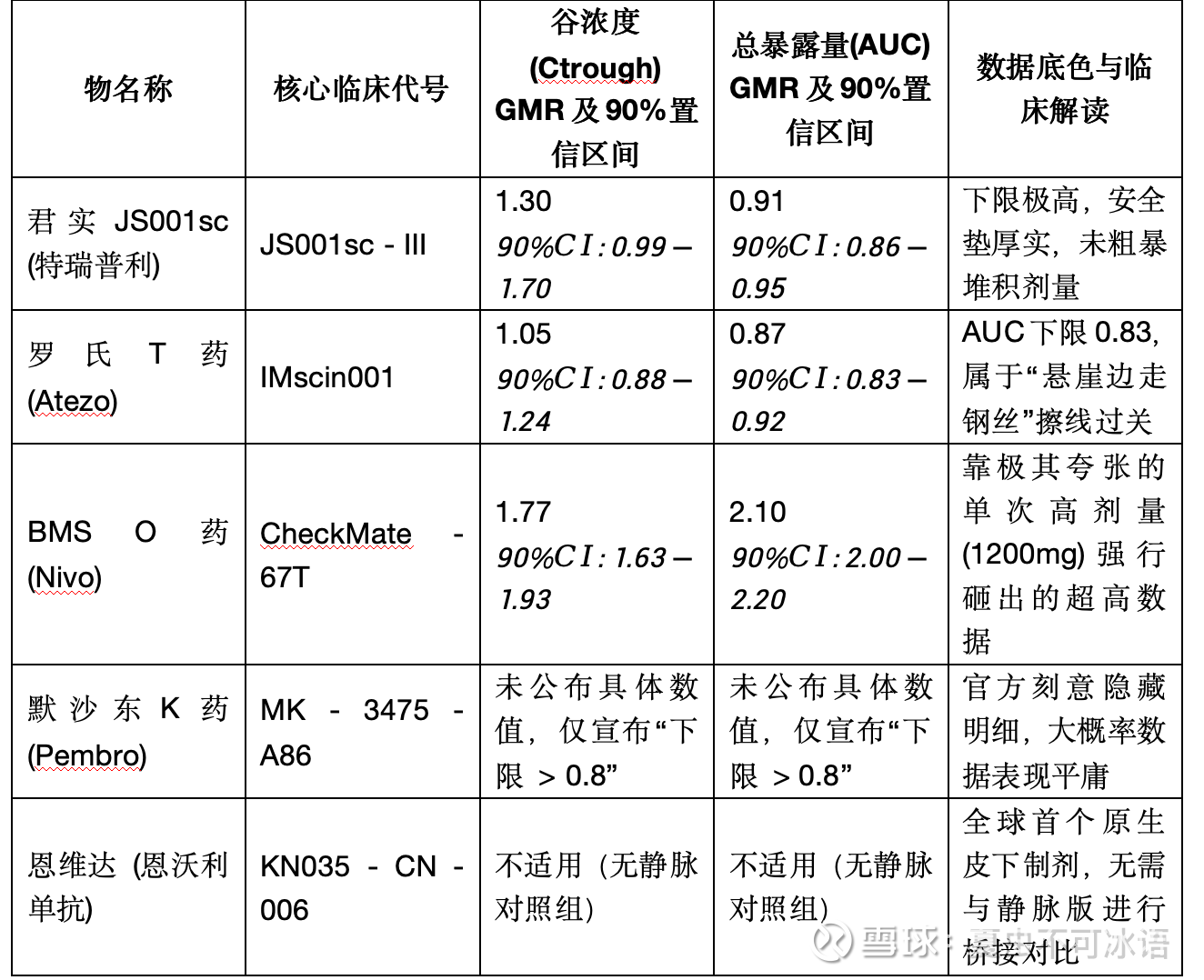
罗氏 T药(Atezo) T药虽然过关了,但极其凶险。它的 AUC 下限掉到了 0.83,距离 0.8 的“拒批死亡线”仅仅一步之遥。稍微再多几个吸收不良的患者,这个数据就可能跌破 0.8 导致几十亿研发打水漂。
BMS O药(Nivo)O药的对照组是 静脉版 3mg/kg(大约240mg),但它皮下版一针直接怼到了惊人的 1200mg 进去(将近5倍的剂量)。靠着这种极其粗暴的剂量堆砌,它硬生生把置信区间砸到了 2.0 以上。代价就是,不管以什么载体作为媒介,一针打进去的蛋白负荷会极大…
默沙东 K药(Pembro)虽然向 FDA 递交了上市申请,但在之前的学术大会上,只用了一句Ctrough 和 AUC 的 90%CI 下限均 >0.8,达成非劣效来概括,至今没有对外公布具体的点估计值和括号里的精确范围。 遮遮掩掩往往意味着数据没有达到“碾压级”的惊艳,大概率也是靠着增加一倍的剂量(395mg)擦着 0.8 的安全线飞过去的。要不然来中国CDE,现在还让提交补充申请了…美国那边上市咱管不了,中国这边我感觉冲这一条,CDE还是非常负责任的,绝对不是故意刁难默沙东。
恩维达(恩沃利单抗)— 不在同一个考场 * 置信区间数据:无。 * 临床大白话解读: 因为恩维达是全球唯一的原生皮下制剂,它从来就没有静脉打点滴的版本。没有静脉版,就没有对照组。不过到现在都没有IV版的,以后估计也不会上了。
对比大致相同剂量的T药和K药,就能知道它的谷浓度超出IV版的30%有多么不容易了,连默沙东都没做成如此优效,君实的工艺不值得一个赞吗。其实,个人感觉K药大概率是被坑了。(先留个悬念,后面在着重说一下)。
最后,这些数据,大家有没有想过,都是从哪些适应症里做出来的呢,毕竟,做通了一个,就一通百通,所有的IV版适应症都可以通过,如果你是药企,如何能保证通过最小的成本,最小的代价,获得最高的成功率?那当然是找一个IV版里最简单的适应症。可君实仍没有这样做。直接上数据。
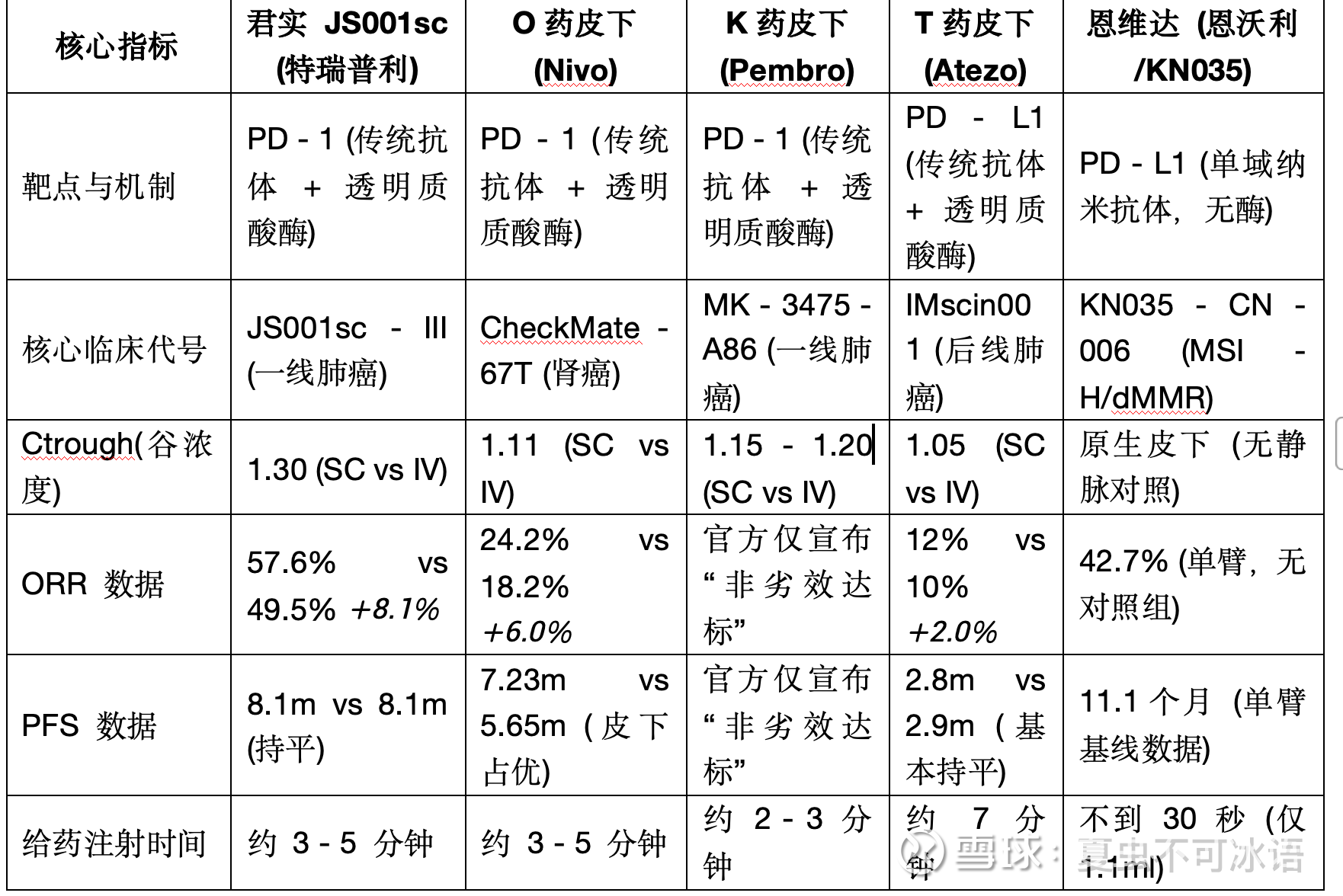
看上图的表格吧,先看适应症栏和ORR(不是主要终点,次要终点,但也能说明很多的问题)的对比吧,如何做好一个CMO?在临床试验的设计里,选哪个适应症来做“皮下vs静脉”的头对头对比,里面其实也藏着极深的算计。这四个药选的适应症,难度其实是有着天壤之别的。【青铜局难度:T药(罗氏)与 O药(BMS)】 这两家为了稳妥,选的是单药治疗”和“后线/低基数”适应症,属于避重就轻。T药皮下:选了“二线及以上非小细胞肺癌(单药)” 难度相比稍低: 都是打过化疗失败的病人,身体底子差,肿瘤负荷大。静脉版T药在这个阶段的有效率(ORR)本来就只有10%左右。逻辑:只要皮下版的ORR能跑到10%-12%,就算非劣效通关了。基数越低,容错率越高,就算稍微差一点,在统计学上也看不出来。 O药皮下:选了“既往接受过治疗的肾细胞癌(单药)” 难度算中等: 肾癌虽然对免疫敏感,但O药在这里也是作为单药使用。没有其他联合药物的干扰,体内的药代动力学(PK)环境相对干净、简单。 地狱级难度:K药(默沙东)与 君实(JS001sc)真正的狠角色,是默沙东和君实(再次吹君实的研发)!他们都选择了肿瘤界最难啃的硬骨头、一线非小细胞肺癌 联合化疗, 为什么说在“一线+化疗”里做皮下注射是绝对的地狱模式?
1.极高基数的“天花板效应”(稍有不慎就翻车) 在一线肺癌里,静脉PD-1加上化疗,ORR(客观缓解率)通常都在45%到60%之间。这已经是极高的天花板了, 痛点: 如果静脉版能做到50%的ORR,你的皮下版哪怕只做到了40%,在统计学上就会立刻被判定为“劣效”,几十亿的研发费直接打水漂。在这么高的基数下,维持住不掉队,已经是很难得了,甚至像君实那样还反超了8.1%,对皮下制剂的吸收效率要求是极其变态的!(K药没公布数据,不知为何,大概率持平或者低一点)
2. 化疗带来的“吸收黑洞”(PK环境极其恶劣) T药和O药是单药,打进皮下后,药物可以舒舒服服地吸收入血。 君实和K药是联合化疗!化疗药大家都知道是啥吧,副作用一大把,(ADC其实也可以理解为PROmax版的化药,不赘述)。化疗药物打进人体后,会引起全身性的血管内皮损伤、体液分布改变,甚至皮下水肿。在这么恶劣的体内环境下,皮下注射的PD-1还能不能稳定地、足量地释放到血液里?这不仅考验药效,更是对皮下制剂底层配方(如透明质酸酶的比例)的终极拷问。君实已经通过了,而且完成的非常好,可以说是全球第一个大大方方公布数据的。
3. 毒副作用的“叠加放大器” 一线病人要同时承受化疗的剧烈毒性和PD-1的免疫反应。如果皮下剂型设计得不好,局部吸收过快导致血药浓度瞬间飙高,极其容易和化疗产生致命的毒性共振。君实敢在这个模式下说出“未发现新的安全性信号,说明它的皮下释放曲线做得极其平滑。 并没让毒性有叠加。
在我的视角里罗氏和BMS像是在“保交楼”,首先保证必须要能安全的获批;而默沙东和君实是挑了IV版里最难的适应症,直接把皮下剂型扔进了最复杂、最残酷的“化疗联合战场”去受死考验!也是最难、容错率最低的适应症! 君实不仅扛住了化疗环境的干扰,还在ORR50%这么高的有效率基数上,硬生生又往上拔高了8个百分点!联合化疗都没有问题,单药肯定就更没有问题了。若再加上剂量的考虑,君实是1.5倍,K药是2倍IV的剂量,君实用更少的剂量做到了比K药更好的效果,考验的是什么呢?(再卖个关子,下面会解答)。BTW,像O药皮下那个剂量,和化疗联用我是不敢想的….,不知道有没有后来上市后的补充数据。(如此大的剂量Orr提升也不是很明显)。所以我认为君实作为国产第一个SC皮下,选择的这个适应症也是非常的有诚意。并没有避重就轻,为了上市而上市,这和18年挑黑色素瘤比上市速度已经有了本质的区别。和新换了邹总当领导我认为也有很大的关系。
再多说一句这个为啥没转为PFS的胜利,在肿瘤界,ORR(客观缓解率)和 PFS(无进展生存期)的脱节,是临床医生和统计学家最经常吵架的地方。君实 JS001sc 的 ORR 暴涨了 8.1%,但中位 PFS 却死死钉在 8.1 个月 vs 8.1 个月,一分都没多。 为什么“打得更狠(ORR高)”,却没能“活得更久(PFS长)”? 核心真相一:ORR 看的是“爆发力”,PFS 看的是“耐药期” ORR 是一个“门槛指标: 按照 RECIST 1.1 标准,只要肿瘤靶病灶的长径总和缩小超过 30%,就算作有效(PR/CR),计入 ORR。高谷浓度带来的“早期红利”: 前面分析过,JS001sc 皮下版拥有 1.30 的极高谷浓度。这意味着在用药早期,它能更迅速、更饱和地封锁住免疫细胞上的 PD-1 受体。这种高压态势,把原本那些肿瘤只缩小了 25%(算作 SD 疾病稳定)的患者,硬生生往前推了一把,推过了 30% 的及格线。这就是那 8.1% ORR 提升的来源。PFS 的铁壁(耐药机制未变): 肿瘤什么时候进展(PFS 终点),取决于肿瘤细胞什么时候进化出获得性耐药(比如 HLA 丢失、JAK/STAT 突变、肿瘤微环境重塑)。皮下剂型只是改变了“送药方式”,并没有改变特瑞普利单抗这个分子的底层药理机制。无论你早期把肿瘤打得缩水了 35% 还是 50%,到了 8 个月左右,肺癌的耐药基因该表达还是会表达,一旦耐药,肿瘤就会复发进展。 大白话总结:皮下版的高浓度让更多病人的肿瘤在早期缩得更小了(赢了 ORR),但并没有改变肿瘤最终产生耐药的时间表(PFS 没变)。 核心真相二:“一线联合化疗”的基石掩盖效应,这个试验是“一线非小细胞肺癌(NSCLC):特瑞普利单抗 + 化疗。前 4-6 个周期的主导权在“化疗”: 在一线治疗的早期,迅速杀灭肿瘤、贡献 ORR 的绝对主力,其实是极其刚猛的铂类化疗药。8 个月中位 PFS 的“天花板”: 对于一线 NSCLC,无论你加什么 PD-1(K药、O药、国产四大),其中位 PFS 普遍就是落在 8 到 9 个月 这个极度拥挤的区间。因为在 8 个月左右,通常是化疗耐药全面爆发的时间点。化疗一旦崩盘,单靠 PD-1 的维持治疗,很难在“中位数”这个指标上把曲线强行拉开。 核心真相三:统计学上的“中位 PFS 欺骗性” , Kaplan-Meier (KM) 生存曲线。 8.1 个月只是“中位数(Median)”: 它只代表了第 50% 那个患者发生进展的时间。它不能代表全貌。免疫治疗真正的胜利在“长尾(Long Tail)”: 评价免疫治疗,更核心的是看 1年 PFS 率、2年 PFS 率。皮下版前期打出了这么高的 ORR,极有可能在后期的 KM 曲线尾部产生更厚实的“长尾效应”。也就是说,虽然中位数没变,但可能活过 2 年没复发的患者比例变多了。这一点,需要等待君实后续公布更长随访时间的 OS(总生存期)和长线 PFS 数据才能下定论。 核心真相四:不要忘了它的初始目的(这是一场非劣效试验) 最关键的底层逻辑是:这是一场为了证明“我跟静脉版一样好”的 PK(药代动力学)桥接试验,不是为了证明“我比静脉版活得更长”的优效试验。 药企在设计试验时,样本量(几百人)和统计学效能(Power)都是冲着“非劣效”去算计的。在这样的试验框架下:PFS 能做到 8.1 vs 8.1(完全持平),在药监局眼里已经是*巨大的成功和完美的闭环。它证明了改变剂型绝对没有牺牲患者的生存利益。统计学上没法(也没必要)强求它转化成中位 PFS 的延长。 虽然 PFS 没有变长,但高 ORR 在真实临床中绝对也有用武之地啊,假如对于一个伴有严重气道阻塞、上腔静脉压迫综合征、或者剧烈骨痛的肺癌患者,他最需要的就是肿瘤立刻、马上能够缩小,以缓解致命的压迫症状。在这个极其凶险的阶段,JS001sc 能多提供 8.1% 的客观缓解概率,这多出来的退缩率,对于改善患者当下的生存质量和挺过危险期,我认为也很有临床价值。
那最后就说说这个药,如何才能安全平稳的在皮下释放吸收的事吧。 因为静脉(IV)版是把药液混在生理盐水里,直接顺着输液管流进大静脉,100% 瞬间入血,根本不存在“释放、渗透、吸收”的物理屏障。 真正的制剂学“地狱”,全在皮下(SC)这短短几分钟、仅仅一两毫升的推注里! 直接切入大分子单抗的底层制剂工艺,看看把一个在血管里跑的药,硬塞到皮下脂肪里,到底要翻过哪几座大山,以及君实的工艺团队到底牛在哪里: 一、 皮下制剂的“三座大山”(主要难点) 把 PD-1 这种几万道尔顿的大分子蛋白打到皮下,面临着极其变态的生理和物理限制:
1. 浓度与黏度的死局(水库太小) 人体皮下组织的间隙极其致密,单次注射的极限容量通常只有 1.5ml 到 2.0ml。超过这个量,皮肤就会鼓起巨大的硬包,甚至因为压力过大导致组织坏死。 为了把 360mg 的特瑞普利单抗塞进这不到 2ml 的水滴里,必须把蛋白浓度浓缩到极高(通常 >150 mg/ml)。
2. 细胞外基质的“铜墙铁壁” 皮下组织里充满了由“透明质酸(玻尿酸)”和胶原蛋白交织成的致密网状结构。大分子蛋白打进去后,就像是被困在了一片极其茂密的原始森林里,根本迈不开腿,没法游向远处的毛细血管和淋巴管。
3. 局部的“巨噬细胞绞肉机” 如果药物在皮下待的时间太长,皮下组织里巡逻的巨噬细胞和蛋白水解酶就会把它当成外来异物,直接就地“吃掉”并降解。这就是为什么皮下注射的生物利用度往往只有 60% 左右的根本原因,很多药还没等入血,就死在皮下了。
二、 制剂如何实现“安全、平稳地释放”? 为了攻克上面这三座大山,药企必须在制剂里加入一个核心武器,并利用一条特殊的通道:
1. 加入“分子开山斧”:重组人透明质酸酶(rHuPH20) 这就是君实、罗氏、BMS 默沙东皮下版里共同添加的那个“酶”。它的作用极其冷血且精准:打针的瞬间,这个酶会立刻把皮下组织里致密的透明质酸网给暂时剪断、降解掉。 原本致密的皮下组织,瞬间被融化出了一个临时大口袋。这就极大降低了注射阻力,病人不会觉得胀痛,黏稠的药液也能迅速摊开。不用担心,人体在 24 到 48 小时内,又会把这些透明质酸重新长出来,恢复如初。
2. 走“淋巴高速”而不是“毛细血管” PD-1 单抗分子太大了,根本钻不进皮下毛细血管那狭窄的孔隙。透明质酸酶开路后,药物真正进入血液的路径是:先缓慢渗透进孔隙更大的“毛细淋巴管”,随着淋巴液回流,最终在颈静脉处汇入全身血液循环。 这个“淋巴回流”的过程极其缓慢,通常需要好几天。这就天然形成了一个极其平稳的缓释效应,完美削平了静脉打点滴时那种危险的浓度尖峰。
三、 君实的数据为什么这么好?它的工艺到底赢在哪? 既然大家都加了透明质酸酶, 君实真正的核心工艺壁垒,最可能的就是藏在极其微观的处方配比里: 1. 找到了“酶与抗体”的最完美切割比例,透明质酸酶加少了,路开得不够宽,抗体药物依然会淤积在皮下被降解;酶加多了,路开得太猛,药物吸收过快,就会导致血液里的初始峰值(Cmax)飙升,引发系统性毒性。 君实应该找到了一个最黄金的比例。这个比例让特瑞普利单抗进入淋巴管的速度,刚好能够对冲掉它在皮下被巨噬细胞吞噬的速度。可以让你它的绝对入血存活率极高,一点药都没浪费。 2. 极高浓度的“热力学维稳工艺” 把 360mg 的抗体浓缩在极小的体积里,最怕的就是蛋白在常温下发生聚集(不仅失效,还会引发严重的免疫原性抗药抗体 ADA)。 目前可以通过极其复杂的缓冲液体系(pH值调控、特定的氨基酸/糖类稳定剂、聚山梨酯表面活性剂的精准添加),在皮下极其复杂的生理盐环境(pH 7.4)下,依然保持了特瑞普利分子的三维结构绝对稳定,不抱团、不沉淀。这是硬核的生化制造底子。 3. 分子天然的等电点(pI)”优势 特瑞普利单抗这个分子本身的表面电荷分布(等电点),可能天然就比 O 药或 K 药更亲和人体皮下的微环境(我记得js207就比所有的双抗要稳定,耐热)。打进去之后,它不容易和皮下组织里带负电的细胞膜死死粘连,从而能够更顺滑地“滑进”淋巴管。
当然上述是我个人的理解,如果有大佬看到了不对的地方,可以批评指正。但其实这个酶剂,也很有说法的。(K药的不明真相原因,以及国产的雄起)
K药!它没有用大家都在用的那种酶,它另起炉灶了,先看行业里的“垄断霸主”:Halozyme 的 rHuPH20 。在我们刚才聊的图表里,罗氏的 T药(Atezo) 和 BMS 的 O药(Nivo),包括强生的达雷妥尤单抗皮下版,用的都是美国一家叫 Halozyme(哈罗赞) 公司的专利技术——重组人透明质酸酶(rHuPH20)。 美国最喜欢的霸王条款: Halozyme 靠着这个酶在皮下制剂领域几乎是绝对垄断。它不仅收极高的专利授权费和销售分成,还经常签“排他性协议”(比如我授权你做PD-1皮下,别人就不能用我的酶做PD-1了,估计是O药的复仇,腹黑一下)。 默沙东(K药)的破局:韩国 Alteogen 的 ALT-B4 。K药是全球当之无愧的肿瘤药“药王”,默沙东当然咽不下“被别人卡脖子收天价保护费”的这口气。 所以,在研发 K药的皮下版(代号 MK-3475A,商品名目前定为 Keytruda Qurex/Qlex)时,默沙东绕开了美国的 Halozyme,秘密找到了韩国的生物技术公司 Alteogen(阿尔泰奥金)。 K药皮下版里面加的酶,正式名称叫:Berahyaluronidase alfa(代号:ALT-B4)。 ALT-B4(韩国酶)和 rHuPH20(美国酶)有什么区别? ALT-B4 也是一种人透明质酸酶的变体,但它是 Alteogen 利用自己的专利平台(Hybrozyme)基因重组改造出来的。物理特性: 韩国这家公司声称,他们改造后的 ALT-B4 比传统的 rHuPH20 热稳定性更好,而且在大规模生产时的蛋白表达量更高。这就意味着它在极高浓度的抗体药液里,不容易失效。 它的氨基酸序列和空间结构跟 Halozyme 的产品有差异,专门为了绕开美国佬的专利壁垒。 (不过现在就因为默沙东用了韩国人的这个酶,现在默沙东正被美国的 Halozyme 按在法庭上疯狂起诉! Halozyme 咬死说韩国的 ALT-B4 侵犯了他们的底层专利,韩国嘛,什么都偷,倒也正常,哈哈)。这场官司现在打得难解难分,但美国 FDA 还是在去年(2025年下半年)顶着压力,把 K药的皮下版给批上市了。因为一旦 K药全盘转成皮下,默沙东每年能省下、或者多赚几百亿美金,他们愿意为了这个花重金打官司。 现在PD1sc版本表面上拼的是数据,但在水面之下,其实是一场“谁能掌握皮下打洞(透明质酸酶)核心科技”的底层肉搏战。君实肯定也用不起啊,光使用费就几千万刀,后面还要15%的分成,君实咋做的呢?
既然 O 药和 T 药用了美国 Halozyme 的酶(被收了天价保护费),K 药用了韩国 Alteogen 的酶(正在被美国人疯狂起诉侵权),那君实的 JS001sc 到底加了什么神秘武器,能巧妙避开这两大雷区? 答案非常硬核:君实用的依然是“重组人透明质酸酶”,但据我了解是用国产的平替,至于具体的供应商名字,药企在正式获批上市前通常将其作为绝对的商业机密严格保密,目前君实官方从未在任何公开材料里点名具体是哪家企业。Halozyme 签过很多排他性协议,国内企业想买都买不到。 目前国内在“重组人透明质酸酶”赛道上走在最前面、且唯一一家已经向国家药监局递交了 NDA(上市申请)的企业,叫上海宝济药业(其核心产品代号 KJ017)。 宝济药业的 KJ017 也是通过重组技术改造的人透明质酸酶,它的出现直接打破了美国 Halozyme 的全球技术垄断。不推股,只是个卖铲子的。大家了解就行了,也在港股通里。这里只想表达,我们国内的东西,同样非常优秀,国内的科学家、工程师,做出来的东西,不比美国人的差。
通过上述,我才敢说,是我以往看到皮下版后,因为惯性的思想,觉得也就是那么回事。没想到数据出来后,如此的优效。超越了外国耳熟能详的名药,不仅是药上的胜利,也是中美药企工艺的成熟度,稳定度,深度甚至是人性上的胜利。作为国产第一个PD1皮下制剂,君实的数据担的起这个头衔。
最后还有恩沃利,恩沃利单抗(恩维达) 它不需要美国 Halozyme 的酶,也不需要韩国 Alteogen 的酶,更不需要国产的替代酶。 为啥它不需要加透明质酸酶? 前面我们说过,君实、O药、K药之所以必须加酶,是因为它们都是传统单克隆抗体(IgG)。这种大分子(分子量约 150 kDa)体型太庞大,就像一辆重型坦克,在皮下组织的“透明质酸森林”里寸步难行,必须靠“酶”这把开山斧在前面开路。 而恩维达(KN035)的真身,是一个单域纳米抗体(Nanobody)体型极小: 康宁杰瑞的科学家把抗体上冗余的部分全部砍掉,只保留了最核心的结合区(并融合了Fc段延长半衰期)。它的分子量只有大约 80 kDa(只有传统抗体的一半左右)。它就像一辆极其灵巧的摩托车,根本不需要砍树开路,自己就能在皮下组织的孔隙里极速穿梭,迅速进入毛细血管和淋巴管入血。 因此,他有非常变态的溶解度: 传统大抗体一旦浓度过高就会黏成“糖浆”甚至沉淀。但纳米抗体天生结构极其稳定,它可以被极其夸张地浓缩。恩维达可以做到在 仅仅 1.1 ml 的极其微小的液体体积里,塞进去 400mg 的高浓度药量,而且依然清澈如水,推注阻力极小,不到 30 秒就能手工推完。(OKTJ都要3 5分钟,主要是黏,得慢慢推)。常温之王: 纳米抗体甚至不需要极其严格的冷链,它在常温下的稳定性极其恐怖,这也是它不需要复杂配方维稳的原因。 康宁杰瑞拥有自主建立的骆驼纳米抗体噬菌体展示文库,这种纳米抗体最早是在骆驼和羊驼的血液里发现的。康宁杰瑞的创始人徐霆博士带领团队,硬是从底层的抗体库筛选开始,一步步打造出了这个全球首个获批的皮下注射 PD-L1。 专利护城河极其深厚。就是适应症少了一点,不过也非常非常的强大!能避开所有专利,独立自主的做出来,还不牛?(恩沃利上市第一个完整年卖了5个亿,我记得电话会王总说28年争取卖10亿001sc制剂,合理。)
越说越多,就这样吧。 挑在今天超级大跌的时候发出来,一个是想说,信心,比黄金更珍贵,国产创新药品质真的不比海外MNC的差,越来越多的事情可以证明,往后应该会更多。我可以很负责任的说这两个过程SC制剂,就是当今最好的皮下制剂。无论从哪个方面来说,都要优于西边。二也不要忘记投资的初心,只要逻辑不变,就继续忽略短期的波动,深挖数据,探询数据后的意义。有时候比持股的过程更有意思。$君实生物(01877)$ $创新药(BK2526)$