成都先导DEL技术加速药物发现新范式革新
在药物发现领域,传统靶点往往局限于具有明确结合口袋的酶或受体,而许多具有重要生物学功能的蛋白(如支架蛋白)因缺乏传统“可成药性”特征而难以靶向。DNA编码化合物库(DNA-encoded library,DEL)技术通过整合高通量筛选与分子条形码技术,实现了对数百亿级化合物库的快速筛选,为攻克“不可成药”靶点提供了革命性工具。近期,Xavier课题组发表在《Cell》上的研究以CARD9蛋白为靶点,展示了DEL技术如何加速药物发现进程,特别是针对传统方法难以触及的“不可成药”靶点。
“不可成药”靶点的局限性
CARD9是一种关键的免疫支架蛋白,通过调控NF-κB信号通路参与炎症反应。其结构主要由卷曲螺旋结构域(CC domains)组成,缺乏传统小分子结合口袋,长期被视为“不可成药”靶点。人类遗传学研究发现,CARD9的截短变异体(CARD9 Δ11)与克罗恩病保护效应相关,这提示靶向CARD9可能具有治疗潜力。然而,卷曲螺旋结构域缺乏明确结合口袋,如何针对这种结构特殊的蛋白开发抑制剂成为巨大挑战。
利用成都先导DEL技术
实现高效初始筛选
本研究采用成都先导(HitGen)自有的DEL库(共计224亿个分子),对全长CARD9及其截短蛋白进行筛选(图1A、B)。这一高通量策略成功识别出以苯并咪唑为核心结构的化合物系列。关键突破在于:
超高通量筛选能力:DEL技术完成了传统高通量筛选难以企及的百亿级化合物库筛选
特定结合位点发现:无需预先了解靶点结构特征,直接识别出CARD9 CC-1结构域的结合位点(图1C)
结构验证:通过X射线晶体学证实苯并咪唑类化合物与CARD9二聚体界面的特异性结合,首次揭示了CC结构域存在可成药性口袋(图2A、B、C)
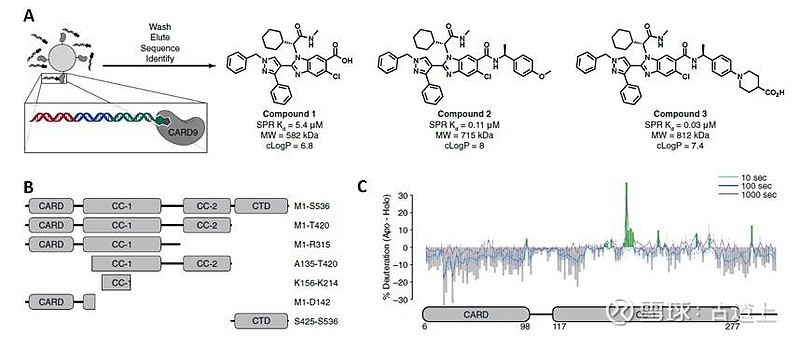
图1:(A)CARD9 DEL筛选流程,以及通过DEL筛选得到的结合子的结构。(B)CARD9用于DEL筛选的全长蛋白以及其他截短蛋白。(C)HDX-MS(氢-氘交换质谱)。数据代表了在化合物1存在下,CARD9蛋白中氢-氘交换减少的区域。
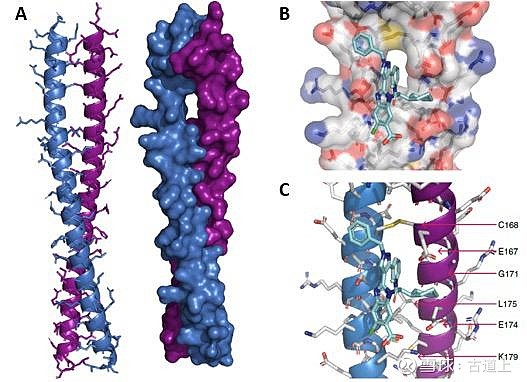
图2:化合物1和CARD9K156-K214的X-ray共晶结构。(A)CARD9K156-K214的X-ray单晶结构。(B)化合物1和CARD9K156-K214的X-ray共晶结构。(C)化合物1和CARD9K156-K214重要氨基酸残基的相互作用。
从“结合子”到“功能抑制剂”
的转化
初始苯并咪唑类化合物仅能结合CARD9但无功能活性,DEL技术为其后续转化提供了关键基础:
DEL衍生探针的二次筛选:基于DEL发现的苯并咪唑结构,设计TR-FRET置换筛选探针,对80万化合物库进行高通量筛选(图3A)
发现全新化学骨架:成功鉴定出苯并二氮 类化合物(图3B),化合物6同时结合CC-1和CC-2两个结构域(图3C)
细胞水平验证:化合物6在人树突状细胞中选择性抑制Dectin-1/CARD9通路,显著降低IL-1β、IL-6和TNF等炎症因子分泌(图3D)
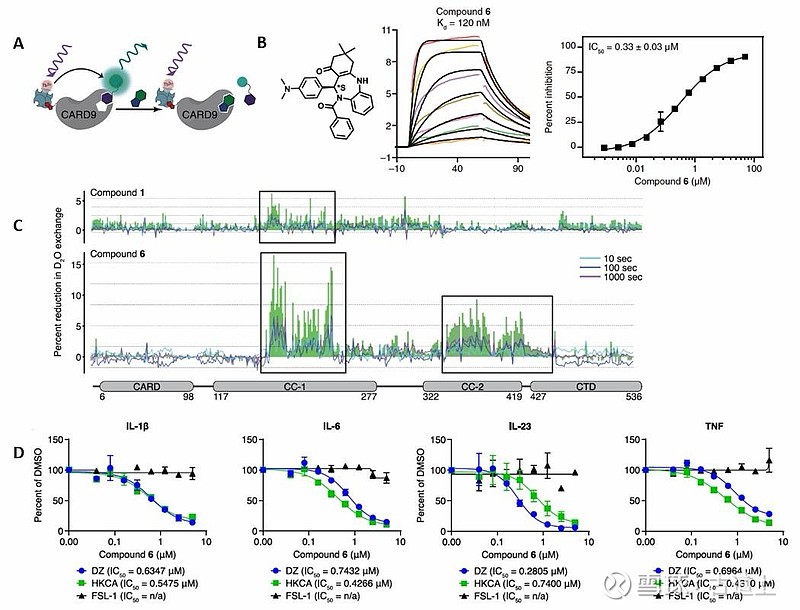
图3:苯并二氮 类化合物的发现与验证。(A)TR-FRET试验的原理图。(B)化合物6的SPR结果与TR-FRET抑制曲线。(C)CARD9M1-S536与化合物1或6的HDX-MS图。(D)化合物6对MDDCs细胞因子分泌的抑制作用。原代人单核细胞来源的树突状细胞(MDDCs)用两种不同的真菌来源的Dectin-1激动剂(DZ和HKCA)或TLR2/6激动剂FSL-1进行刺激。
结论
靶向CARD9卷曲螺旋结构域的抑制剂的发现历程诠释了DEL技术在现代药物发现中的核心价值:DEL不仅突破了传统“可成药性”概念的限制,更通过超高通量筛选与结构导向优化,将“不可成药”靶点转化为可靶向的治疗机会。这一“结合子优先”的策略为其他难成药靶点(如其他CARD家族蛋白、支架蛋白复合物等)的药物开发提供了可复制的范式。随着DEL技术与人类遗传学分析、AI辅助设计、结构生物学等技术的深度融合,未来药物发现将更高效地攻克传统方法难以触及的疾病靶点,为炎症类疾病等重大健康挑战提供创新解决方案。
DEL技术在药物发现中的
范式革新价值
遗传学指导的精准靶向:结合人类遗传学发现,CARD9的截短变异体(CARD9 Δ11)与克罗恩病保护效应相关,而DEL技术可以筛选精准靶向与疾病相关的截短蛋白/突变蛋白的结合子
突破传统靶点认知:首次证明CARD9的CC结构域存在可成药位点,为靶向其他支架蛋白提供新思路
建立“结合子-功能化”新范式:证明即使初始结合子无功能活性,也可通过DEL结合子衍生探针,结合高通量筛选快速转化为功能抑制剂
1. Rahman, J. S., Wang, J. D., Guo, S. D., Graham, D. B., Hu, K., Venables, J. D., ... & Xavier, R. J. (2026). Human genetics guides the discovery of CARD9 inhibitors with anti-inflammatory activity. Cell. 网页链接