瑞博生物(6938.HK)抢滩小核酸慢病蓝海,自研+BD双轮驱动
原创 西南医药杜向阳 西南医药杜向阳
2026年3月9日 10:09 上海投资要点
推荐逻辑:1)小核酸市场高速增长,26 年催化密集,公司作为 siRNA 领域的开拓者之一,自研+BD 双轮驱动有望充分受益赛道增长与靶点催化;2)公司肝靶向核心技术平台接连达成 2 项重磅合作,具备持续造血能力,预计每年有能力提交 2-4 个 IND,肝外递送持续突破;3)公司布局多个小核酸慢病大病种,核心品种 RBD4059 具备 FIC 潜力,高血脂、乙肝、肾病全面布局、空间广阔。
siRNA 小核酸开拓者之一,自研+BD 双轮驱动。公司成立于 2007 年,基于核心技术平台已创建全球最大的 siRNA 药物管线之一,处于临床阶段自研药物涉及心血管、代谢类、肾脏、肝脏疾病的 7 种适应症,其中 4 款处于二期临床试验。公司对外合作合计交易价值超 60 亿美元,包括基于核心技术平台分别与 BI、Madrigal 达成合作共同开发 MASH小核酸创新疗法,及就 RBD7022 与齐鲁制药展开合作。siRNA 药物占小核酸市场近半份额,递送技术为研发关键。全球小核酸药物市场从 2019年的 27 亿美元增长到 2024 年的 57 亿美元(CAGR 16.2%),其中 siRNA 药物占比由 2019年约 7%增长至 2024 年的 44%,有望持续增长。小核酸药物研发平台优势明显,公司首创肝靶向 RiboGalSTAR™平台接连与 BI、Madrigal 达成两项合作,合计交易价值超 60 亿美元,预计未来有能力每年提交 2-4 个 IND;公司前沿布局肝外递送技术,已在肾脏、CNS 等多领域展现疗法优势。核心品种 RBD4059 有望成为全球首款获批治疗血栓性疾病药物。全球每年约 1/4 的人死于血栓栓塞引发的疾病,2024 年全球抗血栓药物市场 593 亿美元,其中约 55%-60%可能成为 FXI siRNA 疗法目标市场。RBD4059 于 si-RNA 赛道进度最快,用于血栓性疾病的 2a 期试验目前处于安全性随访期,计划 26 年启动 2b 期试验拓展适应症。临床 1 期数据显示,600mg 剂量组的 FXI 活性下降 91.6%,药效可持续观察至终点的第 169 天。抢滩小核酸慢病蓝海,管线布局具备潜力。1)RBD5044(APOC3 siRNA):2024 年全球调脂药物市场 240 亿美元,HTG 适应症进度最快的为普乐司兰(3 期),其次为瑞博生物 RBD5044,正在瑞典开展用于混合型血脂异常的 2 期试验,且已获 NMPA 2 期临床默示许可。2)RBD1016(HBV-X siRNA):2024 年全球抗 HBV 药物市场 209 亿美元,现有研究显示 siRNA 药物针对 CHB 表现出更优的功能性治愈,RBD1016 用于乙肝的 2 期全球 MRCT 已于 2025 年 10 月完成,用于丁肝的 2 期于瑞典进行中。3)此外公司还在肾病领域布局了 C5、C3 靶点的临床早期管线。盈利预测与投资建议:公司管线布局全面,小核酸慢病赛道市场广大。预计 2025-2027 年收入分别为184.1/266.2/358.2 百万元,分别同比+29.1%/+44.6%/+34.6%,首次覆盖,建议关注。风险提示:集采政策风险、竞争加剧风险、新品研发进度不及预期风险、海外市场进度不及预期风险。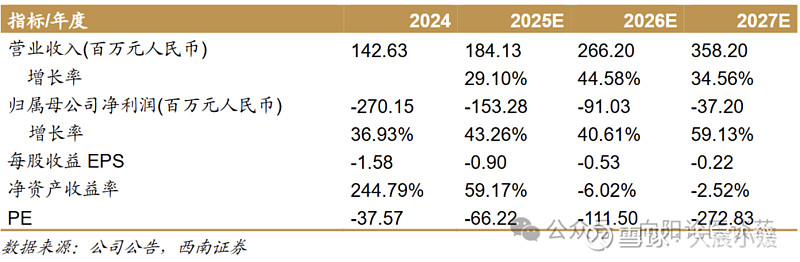
1
公司概况:siRNA 小核酸开拓者之一,聚焦多个慢病大病种
siRNA 小核酸领域的开拓者之一,布局血栓、高血脂、乙肝、肾病等多种慢性病。公司成立于 2007 年,是 siRNA 小核酸领域的开拓者之一。基于核心技术平台,公司已经创建全球最大的 siRNA 药物管线之一,有多款自研药物资产处于临床试验,涉及心血管、代谢类、肾脏和肝脏疾病的七种适应症,其中四款处于 2 期临床试验中,包括核心产品 RBD4059、重要产品 RBD5044 和 RBD1016,此外还布局了 20 余个临床前项目。积极拓展外部合作,交易价值合计超过 60 亿美元。2023 年 12 月,公司与勃林格殷格翰达成合作,基于公司拥有自知识产权且已通过临床验证的GalNAc递送技术的RiboGalSTAR™平台,共同开发治疗非酒精性或代谢功能障碍相关脂肪性肝炎(NASH/MASH)的小核酸创新疗法,总交易价值超 20 亿美元(首付款 2500 万欧元)。同月,瑞博生物与齐鲁制药达成合作,授权后者在中国内地、香港及澳门开展 RBD7022(治疗高胆固醇血症)的开 发、生产和商业化权利 , 合作总额超7亿元人民币 。 2026 年 2 月公司再次基于RiboGalSTAR™平台与 Madrigal达成44亿美元全球独家许可协议(首付款 6000 万美元),携手开发六款针对 MASH 创新 siRNA 疗法。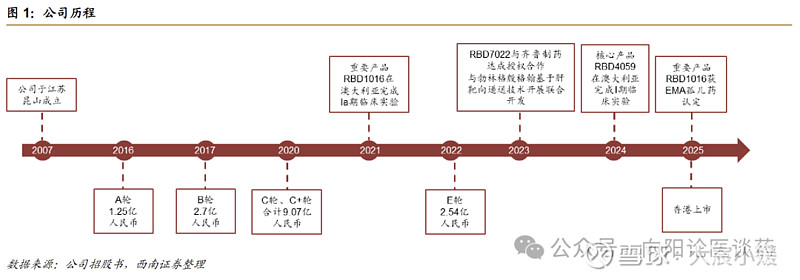
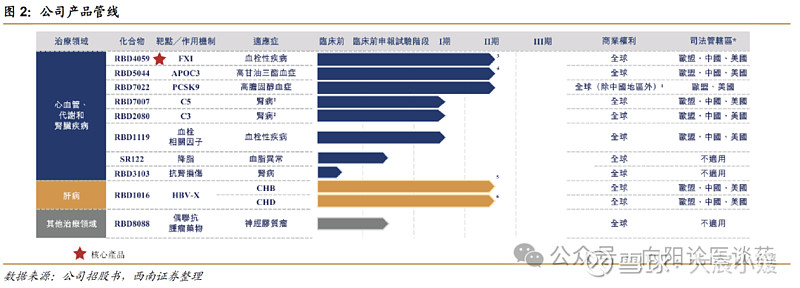 1.1 前瞻布局 siRNA,肝内外递送平台构建护城河小核酸市场星光正盛,siRNA 药物占比近半。全球小核酸药物市场从 2019 年的 27亿美元增长到 2024 年的 57 亿美元,CAGR 16.2%。在技术持续进步、上市批准及临床验证不断增加的推动下,预计全球小核酸药物市场将加速增长,于 2029 年及 2034 年将分别达到 206亿美元及 549 亿美元,2024-2029 年 CAGR 为 29.4%,2029-2034 年 CAGR 为 21.6%。siRNA药物占比由 2019 年约 7%增长至 2024 年的 44%,有望在未来十年占据更大市场份额。
1.1 前瞻布局 siRNA,肝内外递送平台构建护城河小核酸市场星光正盛,siRNA 药物占比近半。全球小核酸药物市场从 2019 年的 27亿美元增长到 2024 年的 57 亿美元,CAGR 16.2%。在技术持续进步、上市批准及临床验证不断增加的推动下,预计全球小核酸药物市场将加速增长,于 2029 年及 2034 年将分别达到 206亿美元及 549 亿美元,2024-2029 年 CAGR 为 29.4%,2029-2034 年 CAGR 为 21.6%。siRNA药物占比由 2019 年约 7%增长至 2024 年的 44%,有望在未来十年占据更大市场份额。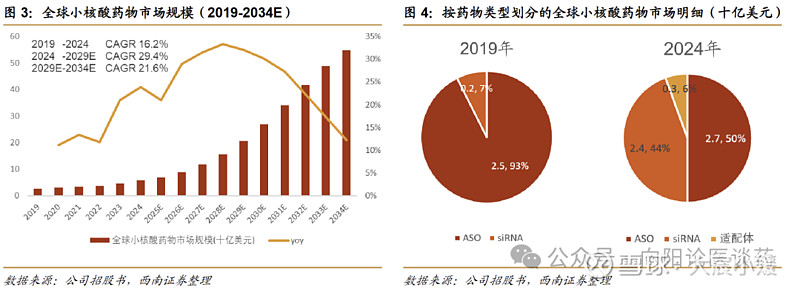
以 siRNA 为代表的小核酸药物兼具长效性与低耐药性,且研发成功率相对较高、研发平台优势明显。
1)从作用机制看,小核酸药物作用于基因表达上游,通过干预 mRNA 翻译效率,特异性沉默疾病基因表达,不易产生耐药性,且疗效持久,可实现半年以上给药频次,显著提升患者依从性;
2)从研发路径看,针对已知基因设计药物比解析复杂蛋白质结构更具确定性,目前已获批小核酸药物临床试验周期多为 5-6 年,短于传统药物研发周期,且成功率相对更高。此外小核酸药物研发效率高度依赖技术平台,例如 Alnylam 凭借其高效平台,从临床 1 期到 3 期研发成功率(POS)达 66.7%,远超创新药整体 5.7%的平均水平。
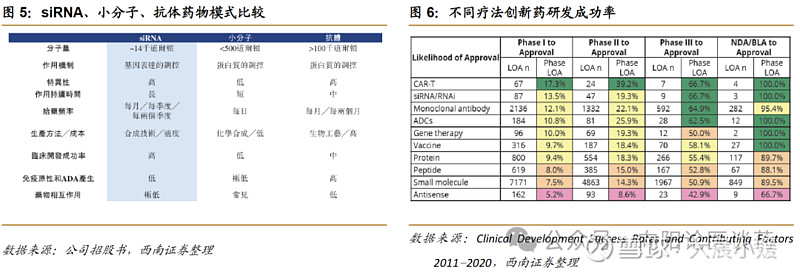
公司已形成以递送技术为核心、修饰技术协同的全技术链研发平台。靶向递送与化学修饰技术是 siRNA 药物成功的最关键技术,肝脏递送技术是目前主流递送方式,而肝外递送代表小核酸疗法的下一个前沿领域。公司已建立自主研发的技术平台,涵盖从药物递送、化学修饰、多靶点药物设计到模型引导的药物开发与生产。具体来看:
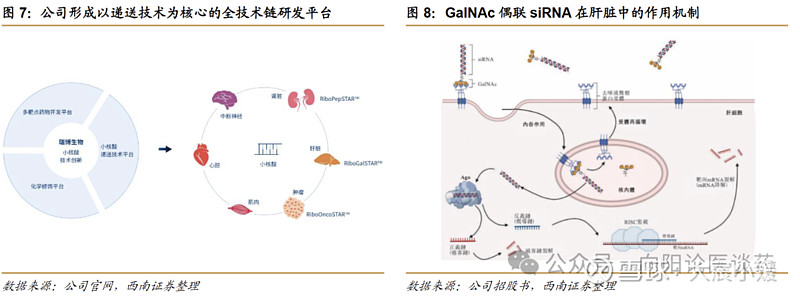
1) 首创肝靶向 RiboGalSTAR™平台,预计有能力每年提交 2-4 个 IND:公司拥有自主知识产权且已通过临床验证的 GalNAc 递送技术的 RiboGalSTAR™平台,成功突破了国外GalNac 偶联技术的专利壁垒,使其成为全球最有效率的 GalNAc 递送技术之一。该平台已将 7 个项目推进至临床阶段,预计 2027 年底前将有 3-4 款药物 IND,未来有能力每年提交 2-4 个 IND。该平台已在包括中国、欧洲和美国在内的主要司法管辖区获得专利授权,与勃林格殷格翰合作亦使其成为唯一一个中国开发并已向 MNC 对外许可的 RNAi 技术平台。
2) 前沿布局肝外递送技术,多领域展现优于现有疗法的显著药效:公司正在开发一系列靶向实体瘤、肾脏、CNS 和脂肪细胞及肌肉等代谢组织的肝外递送技术。包括利用缀合递送技术的肿瘤靶向平台 RiboOncoSTAR™(目前拥有一款临床前神经胶质瘤候选药物),以及靶向其他关键组织和器官的 RiboPepSTAR™平台,目前已在肾脏、中枢神经系统递送应用上在多种疾病模型观察到优于现有疗法的药效。
化学修饰方面,公司自主研发的 RSC(瑞博稳定化修饰平台)平台是一项基于对 siRNA降解机制、序列活性、脱靶规律及长效性的系统研究的迭代式 siRNA 化学修饰技术平台,已在美国、加拿大、澳大利亚等主要市场受专利保护。RSC 平台与 RiboGalSTARTM 递送技术协同作用,已通过 RBD4059 及其它临床阶段管线展现出良好的安全性和持久的疗效。
1.2 股权结构清晰,管理团队实力雄厚
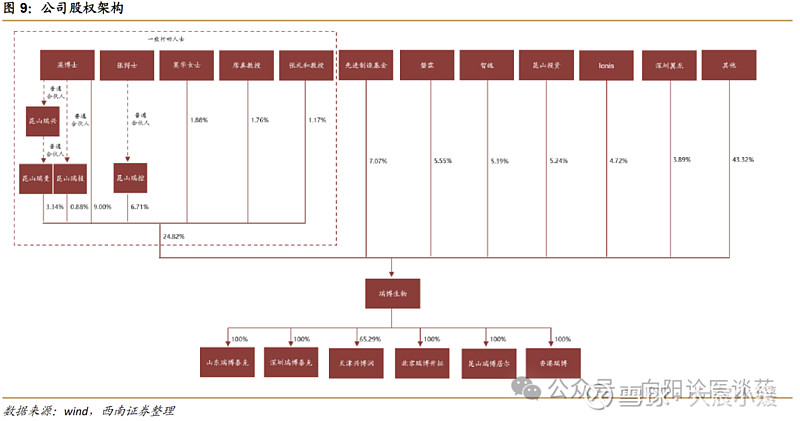
梁子才博士通过关联一致行动人实现实际控制,股权结构清晰。公司上市前经历了 5 轮融资,融资总金额超 15 亿元,包括君联资本、磐霖资本、中金资本系、高瓴资本系等专业投资机构。截至 2026 年 1 月,公司董事长、执行董事兼总裁梁子才博士持股 9.00%,梁博士及其关联的一致行动人合计持股 24.82%,为公司最大控制股东,公司前十大股东包括先进制造基金(7.07%)、磐霖(5.55%)、智魄(5.39%)、昆山投资(5.24%)、Ionis(4.72%)、深圳翼龙(3.89%)等。
涵盖核酸研发与转化全流程的高技术研发与管理团队。公司董事长、首席执行官梁子才博士曾任北京大学分子医学研究所长聘教授,瑞典卡罗琳斯卡医学院研究室主任、副教授,深耕小核酸研究领域 20 余年,曾牵头国家高技术发展计划下的中国首个重大 siRNA 研究项目,为多个国家级研究计划做出贡献。联席首席执行官、全球研发总裁、首席医学官甘黎明博士曾任阿斯利康心血管、肾脏以及代谢类疾病的全球临床开发负责人及全球副总裁,主导阿斯利康核酸药物领域的多项重大合作,拥有阿斯利康 20 年的研发、运营及管理背景。此外,公司还拥有来自中国、美国、瑞典、法国、荷兰的七位心血管、肝脏和肾脏疾病领域的世界级专家组成的强大的科学顾问委员会。

1.3 持续研发投入,融资充沛现金流较稳定
公司暂无商业化产品,主要收入来自与齐鲁制药及勃林格殷格翰的合作首付款及里程碑付款。得益于许可及合作协议,公司 2024 年和 2025H1 营收分别为人民币 1.43 亿元和 1.04亿元,截至 2026 年 1 月累计收到来自齐鲁制药关于 RBD7022 的首付款及里程碑收入 7000万元、来自勃林格殷格翰的合作协议首付款及里程碑付款共计 3500 万欧元。2025H1 公司扣非归母净利润-8811.8 万元,同比减亏 35.9%,主要由于与勃林格殷格翰的合作实现临床前里程碑。
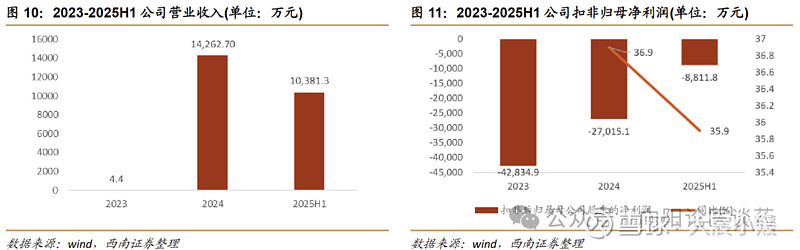
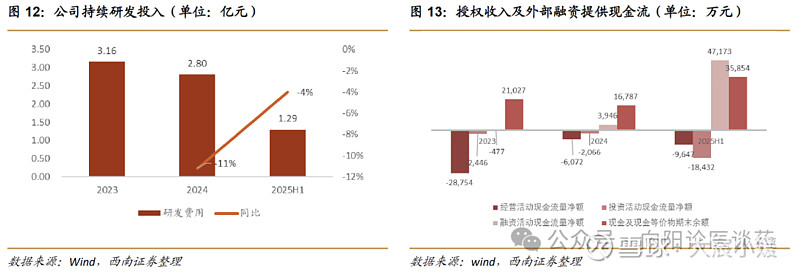
公司持续研发投入,授权收入及外部融资提供现金流。2023 年至 2024 年,研发费用分别为 31,576 万元、28,037 万元,2025H1 研发费用 12,914 万元,同比-4%。现金流方面,目前主要依赖外部融资及授权收入提供现金流,2025 年上半年融资活动现金流净流入 4.72 亿元。
2
心血管、代谢及肾脏疾病
2.1 RBD4059:全球首款用于血栓性疾病的临床阶段siRNA药物
FXI因子仅位于内源性凝血通路上游,抑制FXI有望在抗凝血同时降低出血风险。FXI是一种在血液凝固或止血过程中起关键作用的蛋白质。靶向FXI疗法通过选择性靶向上游的内源性通路,保留正常止血所必需的外源性途径,能够在实现有效血栓预防的同时降低出血风险,相对现有抗凝剂具有关键优势:目前的抗凝剂以凝血酶或Xa因子等下游因子为靶点,会同时影响内源性与外源性途径的功能,增加出血风险。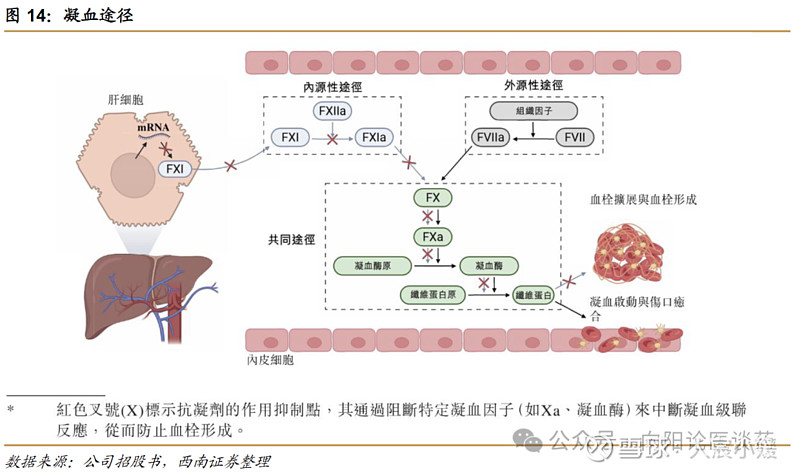
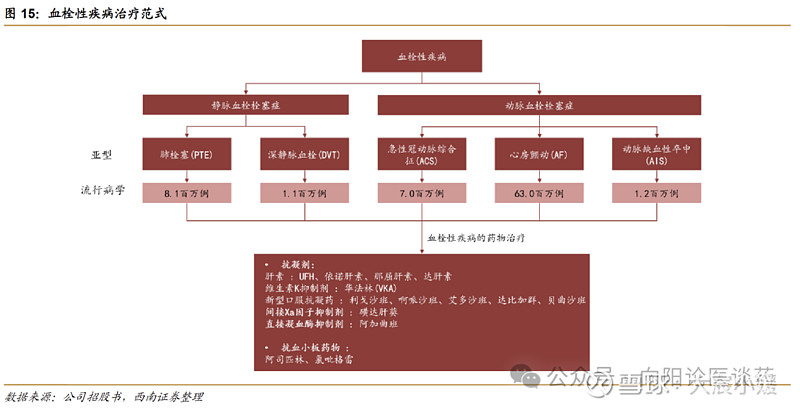
血栓性疾病已成为全球主要死亡原因之一,全球每年约 1/4 的人死于血栓栓塞引发的疾病。血栓形成是血管内限制血液流动的血凝块,主要包括 1)静脉血栓栓塞症(VTE):肺血栓栓塞症(PTE)和深静脉血栓形成(DVT);2)动脉血栓栓塞性疾病:包括急性冠状动脉综合征(ACS)、房颤、动脉缺血发作、脑卒中等。2024 年全球血栓性疾病的发病人数为 2670万人(欧盟 480 万人/中国 700 万人);预计 2034 年将达到 2910 万人(欧盟 760 万人/中国1240 万人)。
2024 年全球抗血栓药物市场 593 亿美元,其中 55%-60%为靶向 FXI 的 siRNA 疗法的目标市场。目前血栓性疾病的主要药物治疗方案为抗凝剂(包括华法林、肝素、直接口服抗凝剂DOAC)。根据弗若斯特沙利文,全球抗血栓药物市场规模从 2019 年的 376 亿美元增长至2024 年的 593 亿美元,CAGR 为 9.5%,预计 2029/2034 年将达到 874/1226 亿美元,其中约 55%-60%可能成为靶向 FXI 的 siRNA 疗法的目标市场(即需要接受长期慢性抗凝治疗的患者群体)。
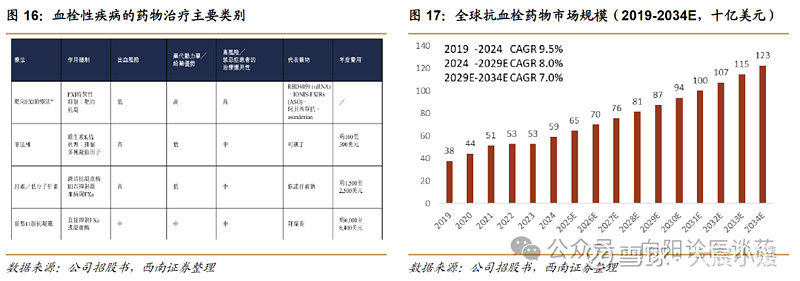
目前尚无靶向 FXI 疗法获批,小核酸赛道中 RBD4059 进度领先。FXI/FXIa 抑制剂按药物形式可分为单抗、小分子、ASO 与 siRNA 四大类。全球范围内共 5 款靶向 FXI/FXIa 创新药进入 3 期临床,包括诺华/Anthos 的 abelacimab(FXI 单抗)、再生元 REGN7508(FXI 单抗)、拜耳 asundexian(FXIa 小分子抑制剂)和 BMS/强生的 milvexian(FXIa 小分子抑制剂)。抑制肝脏 FXI mRNA 表达的小核酸疗法主要包括 Ionis 的 fesomersen (ASO)和瑞博生物 RBD4059,其中 RBD4059 在 FXI-siRNA 中进度最快,目前处于 2 期临床,有望成为全球首款获批用于治疗血栓性疾病的 siRNA 药物。
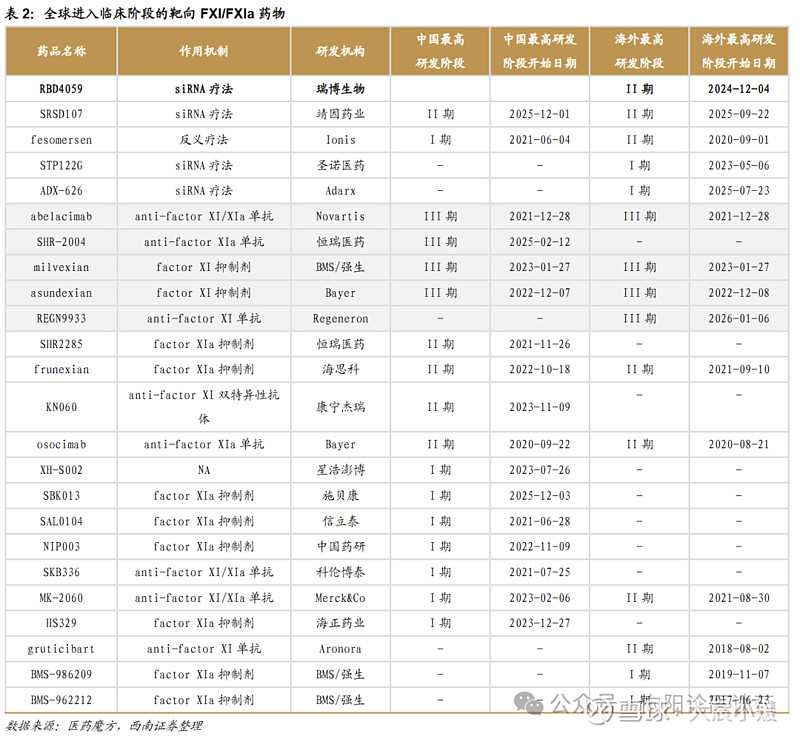
公司核心产品 RBD4059 在 FXI-siRNA 进度最快,且相对其他靶向 FXI 药物具有优势。RBD4059 是公司 FXI 靶向 GalNAc-siRNA,用于治疗和预防动脉粥样硬化性心血管疾病(ASCVD)相关的血栓形成,和其他与异常凝血块形成相关的疾病,例如心房颤动、癌症相关的血栓形成和静脉血栓栓塞。通过选择性沉默肝细胞中的 FXI 基因,RBD4059 能够显著降低血液中 FXI 的表达水平,有望在有效预防病理性血栓形成的同时保留正常止血功能。相对需要每日给药的小分子药物,RBD4059 触发 siRNA 干扰机制可提供每 3-6 个月一次的低频次给药方案,实现 FXI 的持续下调同时提升患者依从性;与抗体等蛋白质类药物相比,RBD4059的化学合成工艺与肝靶向递送系统,大幅降低了产生免疫反应及抗药抗体(ADA)的风险。
公司优先选择监管路径高效的区域加速上市进度。RBD4059 于 2024 年 10 月在澳大利亚完成了健康受试者中的 1 期试验;并于 2024 年 8 月在瑞典启动了针对高危冠状动脉疾病患者的 2a 期临床试验,目前该试验处于安全性随访期。公司计划于 2026 年启动其 2b 期临床试验以进一步拓展新适应症,相关试验结果将用于支持该药物后续进入 3 期临床试验,加速全球上市进程。
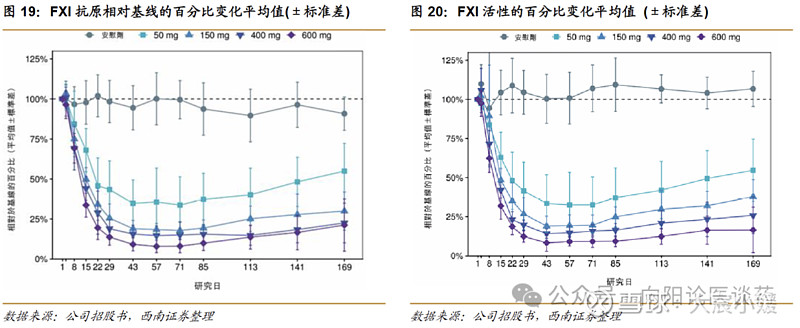
RBD4059 显示广泛的 FXI 抑制水平,可满足各种血栓栓塞适应症可能需要的疗效阈值。在 1 期临床试验中,RBD4059 显示出强劲疗效:50mg、150mg、400mg 及 600mg 队列中,FXI 活性相对于基线的平均最大百分比降幅分别为 67.5%、81.0%、85.8%及 91.6%,药效可持续至试验终点的第 169 天。
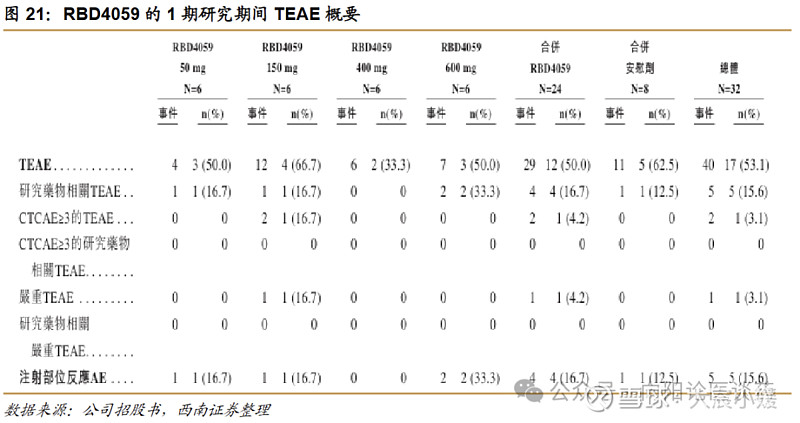
RBD4059 具有良好安全性,相比标准治疗降低出血风险。出血风险是传统抗凝剂的普遍问题。在 RBD4059 的 1 期临床试验中,报告 TEAE 仅为注射部位反应,占比 16.7%;未观察到 Gr≥3 TEAE 或药物相关 SAE。值得注意的是,即使 FXI 抑制水平超过 90%,也未出现出血风险增加的迹象。正在开展的 2a 期试验中,截至数据截止日期(2025 年 8 月 27 日),仅报告 2 例轻度出血事件(1 例痔疮出血、1 例结膜下出血),均未进行特殊医疗干预。
2.2 RBD5044:靶向 APOC3 治疗 HTG 的潜在同类最佳 siRNA
APOC3 在脂质代谢中起关键作用,其水平升高会显著增加心血管疾病发病风险。APOC3是一种主要由肝细胞表达的糖蛋白,通过以下机制推动甘油三酯水平上升,进而显著增加心血管疾病发病风险:1)抑制脂蛋白脂肪酶(LPL)活性,阻碍乳糜微粒的分解,而脂蛋白脂肪酶是清除血液中甘油三酯(TG)所必需的核心酶;2)抑制富含甘油三酯脂蛋白残余物的肝脏清除;3)刺激肝脏分泌更多极低密度脂蛋白(VLDL),加剧脂质负担。因此,阻断 APOC3 成为调控甘油三酯的关键突破口,APOC3 可作为降低血脂异常和心血管疾病风险的新兴治疗靶点。
RBD5044 被设计为靶向肝脏中的 APOC3 mRNA。作为一款经 GalNAc 偶联及化学修饰的 siRNA,RBD5044 能够有效抵达肝细胞,并被肝细胞选择性摄取。一旦进入细胞,RBD5044便会激活 RNA 干扰机制,进而导致 APOC3mRNA 发生降解。通过降低 APOC3 的表达水平,RBD5044 可减轻对脂蛋白脂肪酶等脂质代谢关键酶的抑制作用,同时在一定程度上缓解对肝脂肪酶的抑制,从而实现血液中脂质的有效清除。
在全球范围内,成人血脂异常的患病率约为 40%,每年影响约 30 亿人,其中 HTG(高甘油三酯血症)约占所有病例 25%。根据弗若斯特沙利文,2024 年全球约有 8.456 亿人患有HTG(其中欧盟 1.743 亿人/中国 2.173 亿人),预计 2034 年这一数字将达到 9.139 亿人(欧盟 1.72 亿人/中国 2.199 亿人)。
血脂异常的庞大患者群体对调脂药物有巨大临床需求,现有 HTG 疗法存在局限。全球调脂药物市场规模从 2019 年的 189 亿美元增长至 2024 年 240 亿美元(CAGR 4.9%),预计2029 年/2034 年将分别达到 353 亿美元/416 亿美元(2024-2029 CAGR 8% 2029-2034 CAGR3.4%)。HTG 现有疗法存在局限,体现在疗效有限、需要每日服药,以及显著副作用,比如肝毒性、肌病、胃肠功能紊乱及胰腺炎风险。与以低密度脂蛋白胆固醇为重点的标准治疗相比,APOC3 靶向疗法能更有效、更有针对性地控制与甘油三酯和残余胆固醇有关的心血管风险。临床最先进的候选药物包括 Ionis 的 olezarsen,这是一种用于治疗重度 HTG 的支持 NDA 的ASO 候选药物。
从在研管线看,目前仅有三款靶向 APOC3 小核酸药物获批上市,其中普乐司兰是首个获批的 AOPC3-siRNA,用于降低家族性乳糜微粒血症综合征(FCS)成人患者的甘油三酯水平。截至 2026 年 1 月,有 6 款靶向 APOC3 治疗 HTG 的 siRNA 候选药物处于临床阶段,HTG 适应症进度最快的为普乐司兰(III期),其次为瑞博生物 RBD5044,已于 2025 年 1 月在瑞典启动针对混合性血脂异常的 2 期试验;2026 年 1 月 22 日获 NMPA II期临床默示许可。
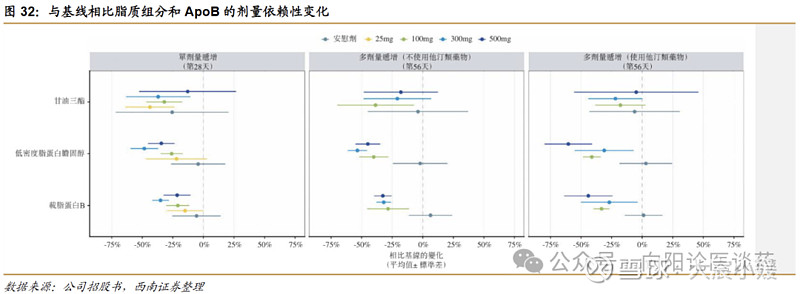
RBD5044 显示充分验证的降脂潜力与长效性,安全性表现优异。2025ESC 公布 RBD5044在澳大利亚开展的健康受试者 1 期临床试验结果。有效性方面,单次注射 RBD5044 可使APOC3 最高降低 84%,同时使甘油三酯(TG)最高降低 70%;且在为期六个月的随访中,甘油三酯水平始终维持在基线水平的 50%以下。此外,受试者的整体血脂状况也显著改善,包括残余胆固醇最高降低 70%、ApoB 最高降低 20%,同时高密度脂蛋白胆固醇(HDL)最高升高 40%。RBD5044 的给药频率可低至每三个月一次,这一特性能显著提升患者对治疗方案的依从性。
安全性方面,1 期多次剂量递增研究中,RBD5044 与安慰剂组 TEAE 分别为 61.1%(11/18)和 50%(3/6),其中 TRAE 分别为 2 例、1 例,所有 TRAE 均为 1 级。RBD5044 组中,与研究药物相关的 TEAE 包括:150mg 剂量队列出现的注射部位疼痛(1/6,16.7%)、90mg 剂量队列出现的丙氨酸转氨酶升高(2/6,33.3%)。此外,在 1 期最高剂量 150 毫克下也未出现剂量限制性毒性,为该产品拓宽临床治疗窗、实现强效降脂提供有力支撑。
2.3 RBD7022:靶向 PCSK9 治疗高胆固醇血症的 siRNA
PCSK9 在调节体内胆固醇水平方面起关键作用。PCSK9(前蛋白转化酶枯草溶菌素 9)是一种酶,在调节体内胆固醇——尤其是通常被称为“LDL-C”或“坏胆固醇”的低密度脂蛋白(LDL)胆固醇水平方面,发挥关键作用。PCSK9 会与肝细胞上的 LDL 受体结合,导致 LDL受体发生降解。这一过程会降低肝脏从血液中清除“坏胆固醇”的能力。
从药物机制看,RBD7022 是一款 GalNAc 偶联 siRNA,用于靶向并抑制 PCSK9 的表达。RBD7022 可特异性靶向肝细胞中的 PCSK9mRNA,通过 RNA 干扰机制有效减少 PCSK9 蛋白的生成。PCSK9 水平的降低,会减少 LDL 受体的降解,使肝细胞表面可利用的 LDL 受体数量大幅增加。这种受体数量的提升,增强了肝脏从血液中清除 LDL-C 的能力,进而降低 LDL及整体胆固醇水平。这一作用机制使 RBD7022成为高胆固醇血症患者的治疗选择,旨在降低与高胆固醇水平相关的心血管疾病风险。
从流行病学看,高胆固醇血症(HC)是最常见的高脂血症类型,约占全球血脂异常病例的 27.4%。HC 被认为是心血管疾病的重要风险因素,且常与其他代谢紊乱相关。根据弗若斯特沙利文的数据,在早发性心血管疾病患者中,约 33.8%至 44.3%患有 HC。2024 年全球高胆固醇血症患者约为 9.35 亿人,预计到 2034 年这一数字将达到 10.10 亿人。
对比目前治疗手段与 PCSK9i 疗法,他汀类药物(LDL 胆固醇降幅通常为 20%-50%)与依折麦布(减少肠道对胆固醇的吸收,降幅为 15%-20%)仅约三分之一的患者能达到目标 LDL-C 水平。PCSK9 抑制剂对 LDL 胆固醇作用降幅可达 50%至 70%,且靶向 PCSK9 的 siRNA药物作用持续时间更长,在初始给药后仅需每年注射两次,可显著提升患者的治疗依从性与用药便利性。
从竞争格局看,截至 2026 年 1 月初,全球仅一款靶向 PCSK9 的 siRNA 药物 Inclisiran获批用于治疗 HC,在研管线中共 6 款用于治疗 HC 的 siRNA 候选药物正在临床开发阶段。RBD7022 为全球第二个进入临床开发的靶向 PCSK9 的 siRNA,于 2023 年 12 月授权大中华权益给齐鲁制药后进展迅速,2026 年 3 月将启动 3 期临床试验。RBD5044 和 RBD7022 在血脂异常治疗领域中可作为机制互补的单药疗法,二者联用则有潜力通过同时降低过高的甘油三酯和胆固醇水平,实现更好的血脂管理效果。
RBD7022 具有与 Inclisiran 相当的 LDL-C 降低效果与良好安全性表现。2025 年 ESC年会上公布了在中国开展的 RBD7022 的 1 期临床试验结果,进一步验证了该药物的强效与长效作用——其 LDL-C 降低效果与 Inclisiran 相当,且具备每六个月给药一次的潜力。以 PCSK9水平作为靶点结合的生物标志物,无论患者是否正在接受他汀类药物治疗,RBD7022 均可使其 PCSK9 水平最大降幅达 75%,且在六个月的随访期内,该抑制水平始终得以维持。RBD7022在 LDL 轻度升高的受试者中展现出良好的安全性与耐受性,且这一特性不受受试者是否接受他汀类药物治疗的影响。
3
肝病领域
3.1 RBD1016:实现 CHB 功能性治愈的未来联合疗法的骨干药物、CDH 差异化 siRNA 候选药物
慢性乙型肝炎(CHB)是由乙型肝炎病毒(HBV)持续感染引起的一种长期肝病,其特点是乙肝表面抗原(HBsAg)在血清中持续存在至少六个月。流行病学:据公司招股书,欧盟和中国 2024 年 CHB 患者分别为 810 万人和 6760 万人;药物市场:全球抗 HBV 药物市场规模从 2019 年 161 亿美元增长至 2024 年 209 亿美元(CAGR 5.4%),预计2029 年/2034 年将分别达到 450 亿美元/778 亿美元,2024-2029 年 CAGR16.5%。
从现有疗法看,CHB 主要治疗手段为应用核苷(酸)类似物(NAs)和长效干扰素进行抗病毒治疗,一线首选药物为恩替卡韦、替诺福韦(NAs)。1)NAs 需长期甚至无限期用药,仅1%-5%的 CHB 患者能实现功能性治愈。2)干扰素可获得更高的 HBsAg 清除率,但为注射给药,治疗持续时间有限,与 NAs 相比副作用更大。
CHB 治疗候选产品包括:1)小核酸疗法,如 GSK 与 Ionis 合作开发的 ASO 药物bepirovirsen,已于 2026 年 1 月 7 日公布关键性 3 期试验积极结果,计划 26Q1 全球申报;2)衣壳调节剂,如广生堂的 GST-HG141 已获得突破性疗法认定,2025 年 7 月进入 3 期临床,且在 2025 年 4 月获批与 GST-HG131(靶向 PAPD5/7 的乙肝表面抗原抑制剂)的联合方案。3)目前正在探索小核酸药物与衣壳调节剂的联合用药方案。
从 siRNA 竞争格局看,目前尚无抗 HBVsiRNA 药物获批治疗 CHB,全球共 7 款同类候选药物处于临床 2 期及以上阶段。
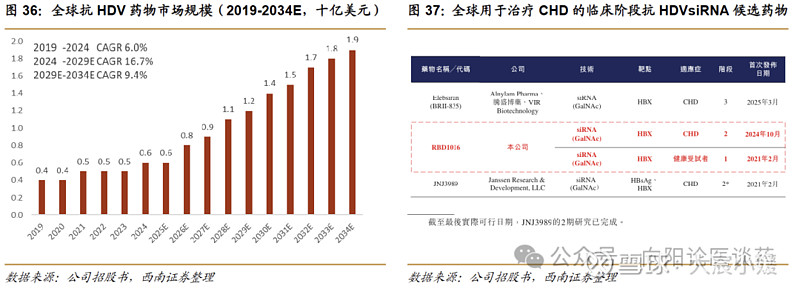
慢性丁型肝炎(CHD)是一种肝脏的重复感染,由丁型肝炎病毒(HDV)引起。HDV 需依赖乙型肝炎病毒完成复制与感染,且合并感染后会加速肝脏病变。流行病学:截至 2024 年,全球 CHD 患者达 1230 万人,其中欧盟 10 万人,中国 200 万人。药物市场:全球抗 HDV 药物市场规模从 2019 年的 4 亿美元增长至 2024 年的 6 亿美元(CAGR 6.0%);预计 2029 年/2034 年将分别增至 12 亿美元/19 亿美元,2024 年至 2029 年 CAGR 为 16.7%。
从现有疗法看,1)全球普遍推荐 PegIFN-α,其具有显著副作用;2)NTCP 抑制剂bulevirtide 已于欧盟获批用于该适应症,但对 HBsAg 的效果有限;3)恩替卡韦或替诺福韦等NAs 被推荐用于控制一些不符合 PegIFN-α治疗条件的患者的 HBV 复制,但它们在降低HBsAg 或 HBV RNA 水平方面没有疗效。
从在研管线看,当前代表性候选产品包括 BlueJay 的单抗 brelovitug,目前正在开展全球性关键临床试验。抗 HBV siRNA 药物可抑制 HBsAg 水平,目前尚无任何 siRNA 药物获批用于治疗 CHB,全球有 3 种用于治疗 CHD 的 siRNA 药物处于临床阶段。
RBD1016 由 siRNA 单元和 GalNAc 递送单元组成,具有高度的肝靶向特异性。其中的活性 siRNA 靶向 HBV 的 X 基因保守区域,通过 RNA 干扰机制降解全部四种 HBV mRNA。这一过程不仅能够阻止 HBVDNA 复制,还能长期显著降低 HBsAg、HBeAg 等病毒蛋白的水平,从而产生强效、持久的抗 HBV 作用。
针对 CHB,公司于 2023 年 8 月、10 月分别在瑞典和香港启动 RBD1016 的 2 期试验,目前正在最终完善该试验的数据分析。RBD1016 亦于 2024 年 10 月获得国家药监局 IND 批准,公司计划启动联合治疗试验并纳入中国临床研究中心。针对 CHD,RBD1016 已于 2024年 8 月在瑞典启动IIa 期试验(未单独开展Ib 期),预计于 2026 年底前完成该试验。
RBD1016 对于 CHB 患者显示剂量依赖性反应和良好的安全性与耐受性。在香港开展的CHB 患者Ib 期临床试验中显示出初步的抗 HBV 效果,单次给药后 HBsAg 持续降低:在接受单剂量 0.3mg/kg、1mg/kg、3mg/kg、6mg/kg 及安慰剂治疗的受试者中,血清 HBsAg 相对基线的平均最大降幅分别为 0.48(第 85 天)、0.75(第 85 天)、0.97(第 113 天)、1.29(第 113 天)和 0.00log₁₀IU/ml。安全性方面,TEAE 发生率 68.8%(22/32),其中最常见(发生率≥5%)的 TEAE 为注射部位反应。大多数患者(24/32,75.0%)出现的是 1-2 级 AE,仅 1 例患者出现与治疗无关的 4 级肌酸激酶水平升高和 3 级天冬氨酸氨基转移酶升高。
4
盈利预测与估值
关键假设:
公司已与国际知名药企勃林格殷格翰建立战略合作伙伴关系,获得合共最高 23.6 亿欧元的里程碑付款;同时与国内知名药企齐鲁制药合作,授予其在中国大陆、香港和澳门开发、生产和商业化 RBD7022 的独家权利。截至招股书发布,2025 年公司已累计收到 BI 支付的首付款 2500 万欧元及里程碑付款 1000 万欧元、齐鲁制药支付的首付款 4000 万元及里程碑付款3000 万元。
与 BI 合作相关里程碑事件包括但不限于:各靶点对应的体内概念验证及其他临床前里程碑;各靶点相关首款产品临床试验启动;各靶点相关首款产品在特定司法管辖区首次获得监管批准以及首次达到多个规定的年度净销售额门槛。目前 BI 合作协议下有两个项目正在进行中,且 25 年 1 月已触发首个临床前里程碑 1000 万欧元,预计 2027 年再次触发。
与齐鲁制药合作相关里程碑事件包括但不限于:在中国内地完成 RBD7022 的 1、2、3 期临床试验及在中国内地实现商业化、达到规定销售额净门槛。RBD7022 已于 2025 年 5 月完成 2 期临床所有受试者入组,有望于 26 年底前触发第二笔里程碑付款;
2026 年 2 月公司与 Madrigal 达成 44 亿美元全球独家许可协议,联合开发六款 MASH 创新 siRNA 疗法,首付款 6000 万美元,参考与 BI 合作进度,预计 2027 年触发首个临床前里程碑。
考虑公司暂未实现商业化,预计 2025-2027 年收入主要由合作收入构成。基于以上假设,我们预计公司2025-2027年收入分别为184.1/266.2/358.2 百万元,分别同 比+29.1%/+44.6%/+34.6%。
5
风险提示
研发进展不及预期风险,竞争格局恶化风险,医药行业政策变动风险。
风险提示:集采政策风险、竞争加剧风险、新品研发进度不及预期风险、海外市场进度不及预期风险证券研究报告:瑞博生物(6938.HK)抢滩小核酸慢病蓝海,“自研+BD”双轮驱动对外发布时间:2026年3月3日报告发布机构:西南证券股份有限公司(已获中国证监会许可的证券投资咨询业务资格)