ELCC:BioNTech更新PD-L1/VEGF双抗多项肺癌临床数据
原创 UmabsDB UmabsDB
2026年3月19日 07:022026年欧洲肺癌大会(ELCC)将于2026年3月25日至28日在丹麦哥本哈根召开,近日相关会议摘要集已正式发布。

这其中BioNTech将更新PD-L1/VEGF双抗药物pumitamig,联合EC化疗,在广泛期一线小细胞肺癌的二期临床结果。

背景:一线免疫治疗联合化疗后,广泛期小细胞肺癌(ES-SCLC)的预后仍然很差。pumitamig(BNT327/BMS986545)是一种在研的双特异性抗体,旨在靶向肿瘤及其微环境(TME)中的PD-L1和VEGF-A。通过与肿瘤细胞上的PD-L1结合,pumitamig旨在恢复效应T细胞的功能,并将VEGF-A中和作用定位在TME内。
两项pumitamig联合化疗治疗一线ES-SCLC患者的II期研究报告显示,该方案在中国和全球人群中均具有令人鼓舞的疗效(Heymach等,NACLC 2025;Cheng等,ELCC 2025)。
方法:本研究为一项在中国开展的开放标签、单臂、多中心研究。年龄≥18岁、ECOG PS评分0-1分、经组织学或细胞学确诊为小细胞肺癌(SCLC)且未接受过广泛期小细胞肺癌(ES-SCLC)全身治疗的患者,接受pumitamig联合铂类-依托泊苷(4个周期)治疗,随后继续使用pumitamig治疗直至疾病进展或出现不可耐受的毒性反应,本次ELCC将报告成熟的总生存期(OS)数据。
结果:截至2025年10月18日,共纳入50例患者(中位年龄59岁,范围46-75岁;80%为ECOG 1分;66%为吸烟者),其中48例可评估疗效(≥1次肿瘤评估)。
中位随访时间为16.8个月(95% CI:11.3-20.8),中位治疗持续时间为26.5周(95% CI:18.1-37.1),目前仍有2例患者在接受治疗。
其中确认的客观缓解率 (ORR) 为 82.0%,中位缓解持续时间为 5.5 个月(95% CI:4.2—6.9)。疾病控制率为 94.0%。
中位无进展生存期 (PFS) 为 6.9 个月(95% CI:5.1—8.2);中位总生存期 (OS) 为 16.9 个月(95% CI:14.3—20.5);12 个月 OS 率为 72.0%(95% CI:57.4%—82.4%)。客观响应率和OS都相对于去年ELCC期间报告的数据具有提升。
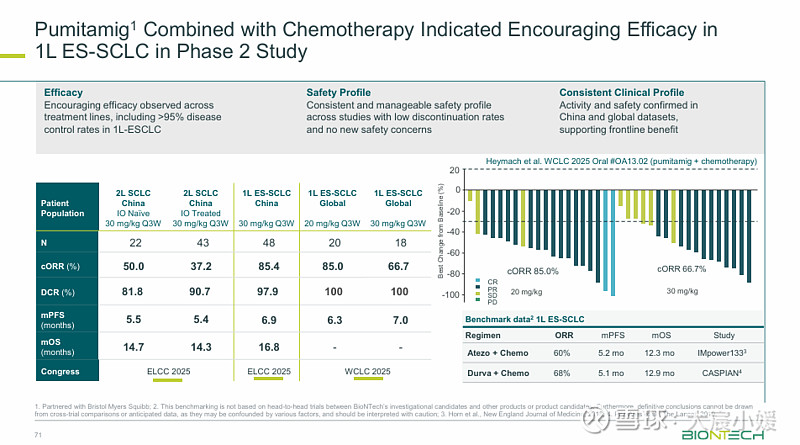
安全性方面,所有患者均出现 ≥1 例与pumitamig或化疗相关的治疗期间出现的不良事件 (TEAE),其中 43 例 (86%) 出现 ≥3 级治疗相关 TEAE。最常见的 TEAE 为中性粒细胞计数减少 (92%)、贫血 (88%)、白细胞计数减少 (80%) 和血小板计数减少 (66%)。
免疫相关不良事件发生率为 26% (13/50),其中 8% (4/50) 的患者发生 ≥3 级不良事件。未发生导致死亡的治疗相关治疗期间出现的不良事件。4 例患者 (8%) 因pumitamig相关治疗期间出现的不良事件而停止治疗。
结论:一线pumitamig联合铂类化疗方案在本 II 期试验中显示出令人鼓舞的疗效,且在广泛期小细胞肺癌 (ES-SCLC) 患者中具有可接受的耐受性,目前正在 ROSETTA Lung-01 全球 III 期试验 (NCT06712355) 中进行进一步评估,也有可能也是pumitamig的首发适应症之一。
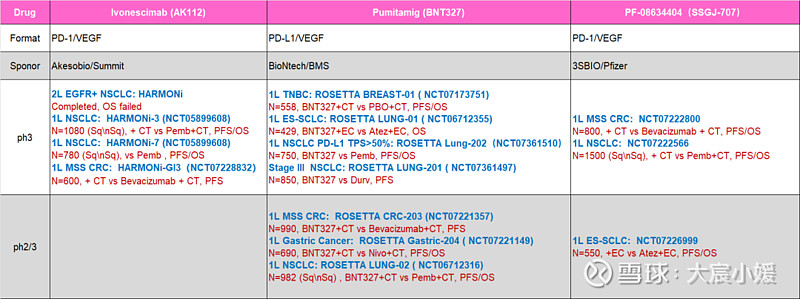 除了小细胞肺癌,BioNTech还再次更新了PD-L1/VEGF双抗药物pumitamig单药,治疗PD-L1阳性的非小细胞肺癌临床结果。
除了小细胞肺癌,BioNTech还再次更新了PD-L1/VEGF双抗药物pumitamig单药,治疗PD-L1阳性的非小细胞肺癌临床结果。
背景:pumitamig(BNT327/BMS986545)是一种在研双特异性抗体,旨在靶向肿瘤及其微环境中的PD-L1和VEGF-A,在晚期非小细胞肺癌(NSCLC)中显示出令人鼓舞的疗效和良好的安全性(ASCO 2024摘要#8533)。本次ELCC研究者将报告正在进行的pumitamig治疗晚期NSCLC患者的最新结果,包括对鳞状细胞癌(SQ)患者的亚组分析。
方法:本Ib/IIa期临床试验纳入了既往未接受治疗的PD-L1阳性晚期非鳞状细胞癌(NSQ;EGFR/ALK野生型)和鳞状细胞癌患者。患者接受pumitamig 20 mg/kg,每两周一次,直至出现不可耐受的毒性、疾病进展或患者撤回知情同意。
肿瘤反应在第一年每6周评估一次,之后每12周评估一次。主要终点为客观缓解率(ORR);其他疗效终点和安全性终点为次要终点。
结果:截至2025年12月22日,共纳入17例非鳞状非小细胞肺癌(NSQ NSCLC)患者和13例鳞状非小细胞肺癌(SQ NSCLC)患者。
在NSQ NSCLC患者中(中位随访时间为16.0个月),未经确认的客观缓解率(uORR)为47.1%,中位无进展生存期(PFS)总体为13.6个月,和2024年ASCO会议报道一致。本次进一步公布亚组数据,PD-L1表达≤49%的患者为12.2个月,PD-L1表达≥50%的患者为17.9个月。
在SQ NSCLC患者的数据为首次报道,中位随访时间为8.8个月,uORR为61.5%;PFS数据尚未成熟。整体上,在非鳞状细胞癌(NSQ)和鳞状细胞癌(SQ)中,均观察到了PD-L1表达水平各异的疗效。
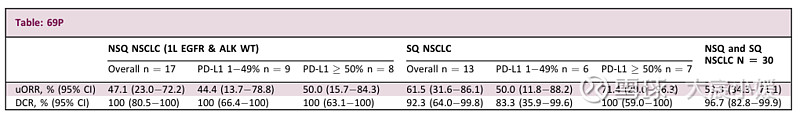
安全性方面,在30例NSCLC患者(NSQ和SQ)中,40.0%报告了≥3级的治疗相关不良事件(TRAE),33.3%报告了≥3级的免疫相关不良事件(irAE),其中6.7%的患者出现≥3级的免疫相关不良事件。
13.3%的患者因TRAE而停止治疗。无TEAE导致死亡。NSQ和SQ NSCLC的安全性特征相似。
结论:pumitamig 在PD-L1表达水平各异的晚期NSCLC患者中显示出初步的抗肿瘤活性,且安全性可接受,包括SQ细胞癌。
pumitamig 联合化疗治疗非小细胞肺癌患者的疗效正在多项全球性研究中进行深入探讨,包括 ROSETTA Lung-02 (NCT06712316) 和BNT327-07 (NCT06841055)。
此外,BioNTech还再次更新了PD-L1/VEGF双抗药物pumitamig单药,治疗EGFR突变的非小细胞肺癌的二期临床结果。
背景:pumitamig(BNT327/BMS986545)是一种在研的双特异性抗体,旨在靶向肿瘤及其微环境中的PD-L1和VEGF-A。在既往接受过治疗的EGFR突变型非小细胞肺癌(NSCLC)患者中,pumitamig联合化疗已显示出令人鼓舞的抗肿瘤活性。
本次ELCC会议,研究者将介绍了一项正在进行的单臂II期临床研究的无进展生存期(PFS)和总生存期(OS)数据,该研究评估了pumitamig联合化疗治疗在接受标准EGFR-TKI治疗后进展的EGFR突变型晚期NSCLC患者的疗效。
方法:患者接受4个周期的pumitamig联合卡铂和培美曲塞治疗,然后接受普米他米联合培美曲塞维持治疗。客观缓解率(ORR)和无进展生存期(PFS)为主要终点;总生存期(OS)和安全性为次要终点。 PD-L1表达分析采用免疫组化法,并根据肿瘤比例评分分为阴性(<1%)、低表达(1%—49%)或高表达(≥50%)。
结果:截至2025年10月18日,共纳入64例患者。中位年龄为59岁,89.1%的患者ECOG PS评分为1分。所有患者均可评估安全性、疗效和PD-L1表达。
中位随访时间为20.4个月,整体客观响应率达到59.4%,中位无进展生存期(PFS)为9.6个月,12个月PFS率为42.4%;中位总生存期(OS)未达到,12个月OS率为79.7%。在所有PD-L1表达水平下均观察到疗效。
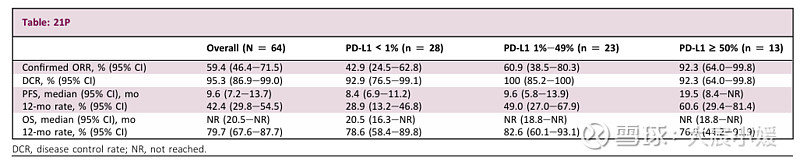 相比于2024年ESMO会议中报道的数据,本次PD<1%的亚组客观响应率略有提升,中和高组均此前数据一致。
相比于2024年ESMO会议中报道的数据,本次PD<1%的亚组客观响应率略有提升,中和高组均此前数据一致。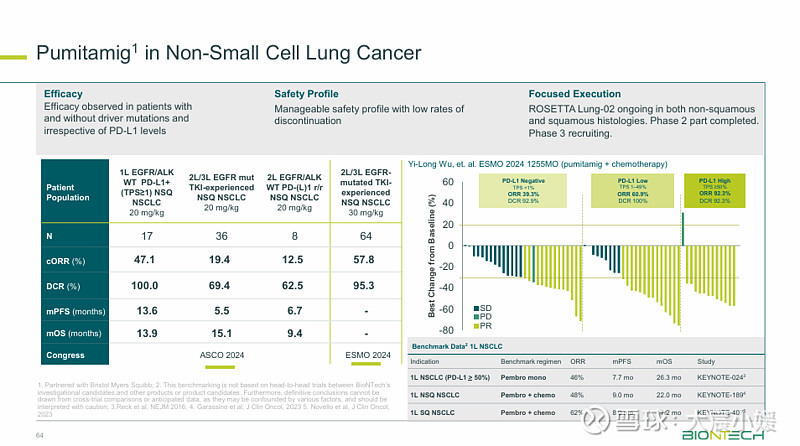
安全性方面,所有患者均报告了治疗相关不良事件(TRAE,与任何药物相关),其中 68.8% (44/64) 的患者出现 ≥3 级不良事件。主要 TRAE 包括血液学不良事件、转氨酶升高和蛋白尿。TRAE 导致 12 例患者停止治疗,1 例患者因肺炎死亡。31.3% (20/64) 的患者出现任何级别的免疫相关不良事件(irAE),7.8% (5/64) 的患者出现 ≥3 级 irAE。
结论:pumitamig联合化疗在 PD-L1 水平(包括 PD-L1 <1%)下均显示出令人鼓舞的无进展生存期 (PFS) 和总生存期 (OS),其安全性与既往报道一致,适用于接受 EGFR-TKI 治疗后进展的 EGFR 突变型非小细胞肺癌 (NSCLC) 患者。PD-L1高表达的患者获益最大。
虽然pumitamig联合化疗在EGFR突变的非小细胞肺癌中展现了积极的数据,但基于基于当前的其它疗法的研发格局,其或不再进行更多的探索,目前也没有启动相关三期临床试验