半年一次,哮喘新药获批上市
近日,NMPA正式批准葛兰素史克开发的德莫奇单抗(商品名:易适来)上市,用于成人和12岁及以上青少年重度嗜酸性粒细胞性哮喘的维持治疗。
德莫奇单抗是GSK开发的新一代抗白介素-5(IL-5)单克隆抗体,其独特之处在于兼具高结合亲和力与延长的半衰期,可实现每年仅需两次给药(每半年一次)。作为IL-5靶向生物制剂的迭代产品,它直接作用于嗜酸性粒细胞发育的关键细胞因子,从源头抑制2型炎症——这正是导致哮喘急性发作与病情进展的核心病理机制。
该药的获批用于重度哮喘的治疗是基于SWIFT-1和SWIFT-2两项Ⅲ期临床试验的研究数据。
结果显示,与安慰剂联合标准治疗相比,德莫奇单抗治疗组患者的年化哮喘急性发作率分别降低58%(SWIFT-1)和48%(SWIFT-2)。更具临床意义的是,汇总分析显示,需要住院治疗或急诊就诊的严重急性发作风险降低了72%,德莫奇单抗组的年化严重发作率仅为0.02,而安慰剂组为0.09。
安全性方面,德莫奇单抗表现良好,不良事件发生率和严重程度与安慰剂组相似,未出现与研究治疗相关的死亡或严重不良事件。
哮喘是中国重大公共卫生负担之一,约有4600万成年人受其困扰,其中约6%属于重度哮喘患者。这类患者即便接受标准治疗,仍面临更高的住院风险和潜在的致命性发作可能。数据显示,中国约15%的哮喘患者在过去12个月内经历过需要住院的急性发作。
德莫奇单抗的获批为这一庞大患者群体带来了全新的治疗选择。作为中国首款且目前唯一一款用于治疗嗜酸性表型重度哮喘的超长效生物制剂,其半年一针的给药方案不仅有助于提高患者依从性,更有望彻底改变现有治疗模式,减轻疾病管理负担。
除哮喘适应症外,GSK还在积极拓展德莫奇单抗的治疗边界。目前,该药针对嗜酸性肉芽肿性多血管炎(EGPA)、高嗜酸性粒细胞综合征(HES)以及慢阻肺(COPD)的III期临床试验也在进行中。
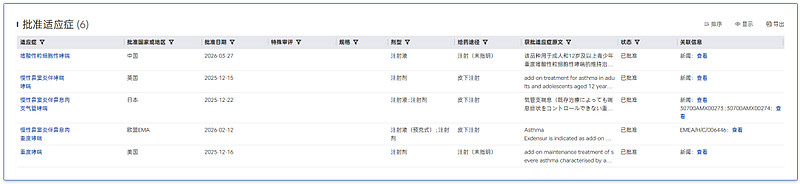
德莫奇单抗已获批适应症
图片来源:药智数据-全球药物分析系统
结语:德莫奇单抗在华获批,既是GSK呼吸产品管线的重要里程碑,也是中国哮喘治疗领域迈向精准化、长效化管理的标志性事件。随着这款超长效生物制剂的临床应用,中国数百万重度哮喘患者有望迎来少打针、少发作的全新治疗时代。
参考来源:
1.药智数据-全球药物分析系统
2.网页链接
声明:本内容仅用作医药行业信息传播,不代表药智网立场。