拨康视云一近视新药撤回临床试验申请,上市不到9个月股价已跌去八成
上市不到9个月的拨康视云,其新药临床试验出现了变数。
3月19日,拨康视云-B(02592)发布公告,公司于2024年1月就CBT-009眼用乳液(一种以半氟化烷烃(“半氟化烷烃”)为基础的阿托品滴眼液,用于治疗青少年近视)可能在中国等地进行安慰剂对照多地区临床试验(“多地区临床试验”)一事,与药审中心举行了新药临床试验申请前咨询会议。基于当时的沟通情况,集团于2025年12月正式提交了新药临床试验申请,并于2026年1月获得受理。
在提交新药临床试验申请后,药审中心批准了一款可比药品在中国上市。经后续与药审中心沟通后,公司相信由于各区域监管要求不同,将中国纳入多地区临床试验可能存在困难。
为避免后续研发风险,及更好地分配集团的资源,公司已决定主动就可能于中国进行的第三期试验撤回现有的新药临床试验申请。

拨康视云同时表示,公司致力于继续开发其半氟化烷烃平台,并将根据最新的法规要求和市场环境,重新评估CBT-009的临床开发策略。待完成相关补充研究或调整临床试验方案后,公司将根据情况再次与药审中心进行临床试验申请前咨询会议或重新提交临床试验申请。
资料显示,拨康视云是一间临床阶段眼科生物科技公司,致力于开发各种疗法。眼科是研究眼部结构、功能和疾病的医学分支。公司首家主要营运实体Cloudbreak USA于2015年9月在美国注册成立及公司于2020年11月在开曼群岛注册成立。
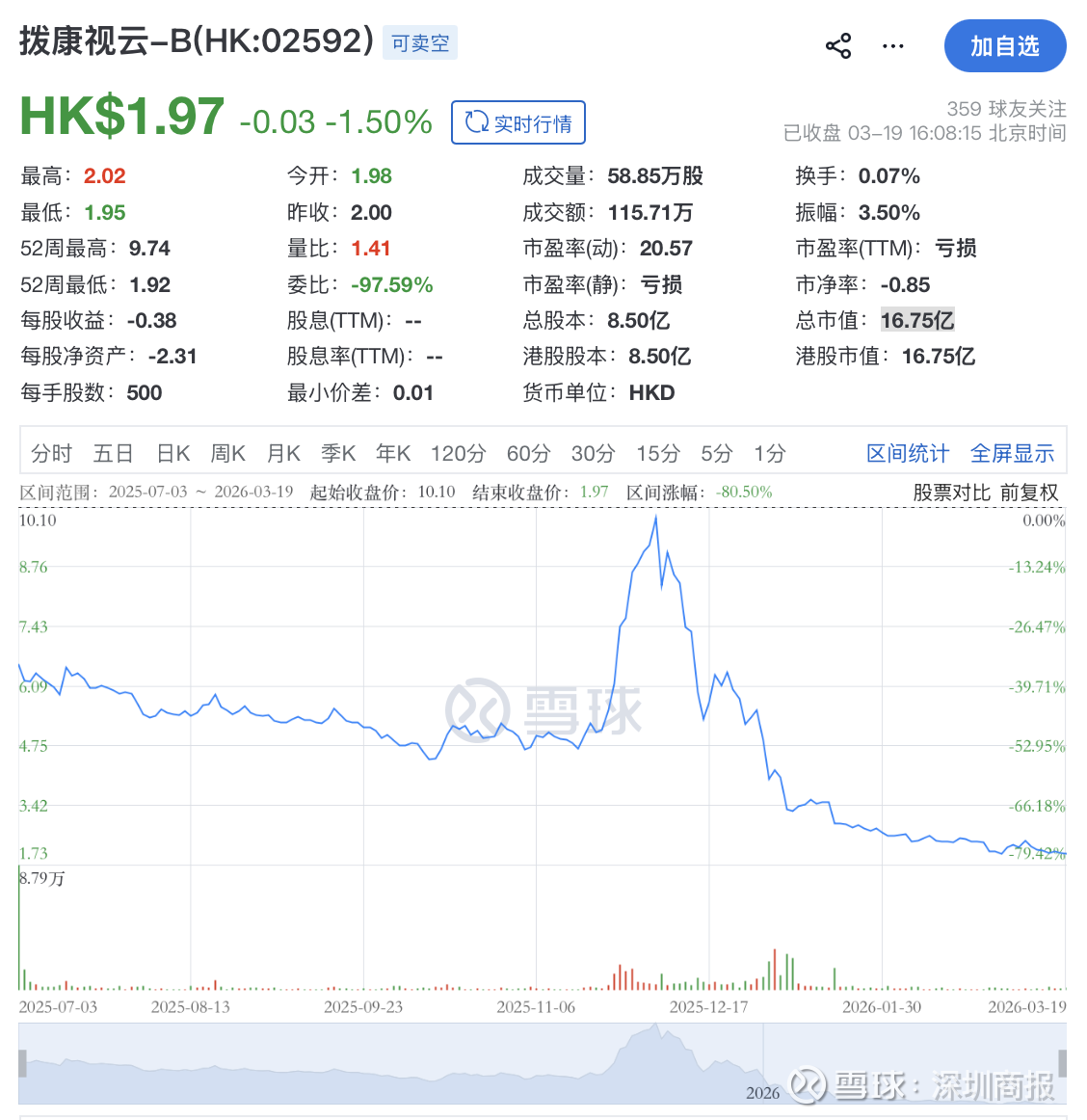
2025年7月3日,拨康视云在港交所上市,其发行价10.1港元/股,截至3月19日收盘,该股股价已跌至1.97港元/股,上市至今股价跌去八成。
其总市值也从上市首日收盘的52亿港元,跌至目前的16.75亿港元。
根据招股书,拨康视云2022年、2023年无收益,2024年营收为1000万美元。拨康视云2022年、2023年、2024年经营亏损分别为2301万美元、3722万美元、3658万元;期内亏损分别为6684万美元、1.29亿美元、9913万美元。
拨康视云将于3月30日举行董事会会议,藉以(其中包括)考虑并批准集团截至2025年12月30日止年度经审核年度业绩及其刊发,以及考虑派发末期股息(如有)。
拨康视云执行董事分别为NI Jinsong博士、Van Son DINH、YANG Rong博士;非执行董事分别为LI Jun Zhi博士、曹旭、周超;独立非执行董事分别为赖显荣、廖仲敏、聂四江女士。
来源:读创财经