开拓医美注射市场,启动第二增长曲线-巨子生物分析之六
$巨子生物(02367)$ 聚焦于“美丽”和“健康”两个领域,从当前收入结构看,公司绝大部分收入来自于“美丽”领域,其中功效性护肤品和医用敷料贡献了大部分收入。前文也分析到,公司当前对明星系列产品“可复美”的依赖性过强,2024年“可复美”系列产品收入占公司总收入82.27%。
为降低对“可复美”系列产品的过度依赖,公司积极研发和推出新产品,以期带动“第二增长曲线”,实现更为稳健和多元化的发展。公司基于发展历程,非常自然地选择了“医美赛道”作为重点主攻方向。
依托自主研发的重组胶原蛋白分子库和充沛产能,公司积极开展相关产品研发和证照申请,截至2026年1月,已经获得国家药品监督管理局(NMPA)颁发的3张III类医疗器械证。
国内医美市场,早期以玻尿酸为主,后来扩大至肉毒素。过去5年,随着重组胶原蛋白、再生材料(聚左旋乳酸和聚己内酯(PCL))以及2025年国内首款羟基磷灰石的获批,加上多聚脱氧核糖核苷酸(PDRN)、丝素蛋白正在排队等待“首证”,医美材料将进入百花齐放的时代。
1.医美材料
分析医美材料之前,先初步了解一下人体皮肤的结构。人体皮肤可分为3层:表皮层、真皮层以及皮下组织,具体如下图所示。
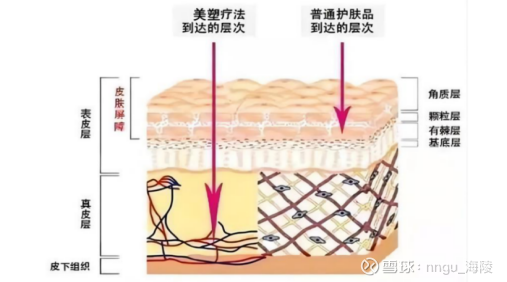
从图中可以看出,角质层位于表皮层最外面,发挥皮肤屏障作用。日常护肤品包括功效性护肤品(生活美容)多只能到达表皮层,见效相对缓慢。
追求快速见效的消费者选择实施医疗美容,医疗美容可以通过注射等方式直达真皮层,皮下组织,达到快速除皱、美白、保湿等作用。下图所示为生活美容和医疗美容的区别。

可见,生活美容与医疗美容最显著的区别在于人体表面是否有创伤性,是否入侵皮肤。医疗美容属于“医疗”大类,必须由具备《医疗机构执业许可证》的医疗机构,包括公立医院和非公立医疗机构,由具有资质的医生开展。
医疗美容项目中,非手术类医美项目因侵入性低和恢复快的特点被消费者广泛接受。下图所示为2023年全球前5名的非手术类和手术类医美项目数量统计,可见非手术类医美项目数量显著领先。
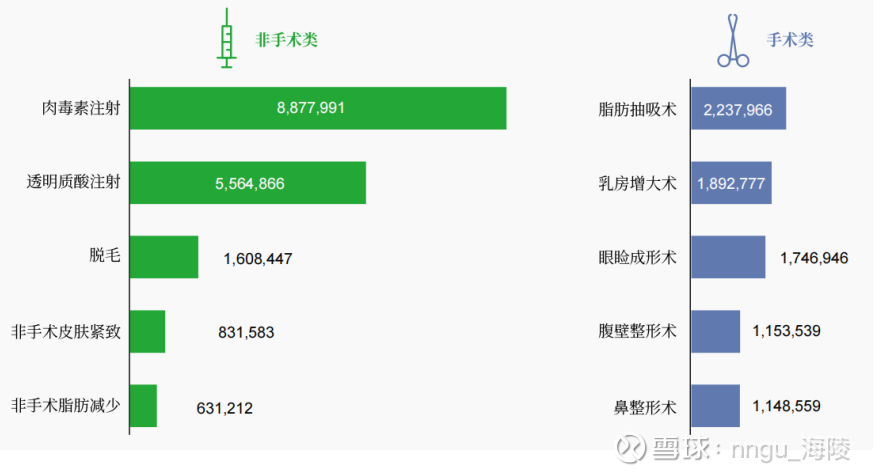
医美注射类产品主要包括玻尿酸类(透明质酸)、胶原蛋白类、聚乳酸为代表的再生材料类、肉毒素类等。
其中,玻尿酸、胶原蛋白和再生材料均属于医疗器械领域的注射材料类,按照《医疗器械分类目录》进行分类管理,并受《医疗器械监督管理条例》等医疗器械相关政策法规的约束。
肉毒素虽广泛应用于医美注射领域,但其属于医疗用毒性药品范畴,其生产和流通须依据《医疗用毒性药品管理办法》等法律法规,对肉毒素从生产源头至最终使用的全过程实施管理和监督。
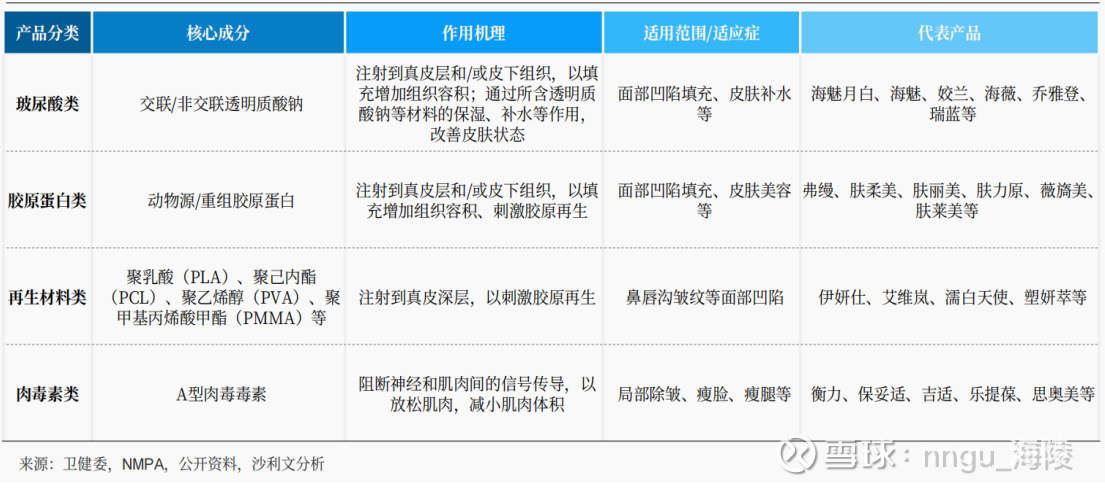
医美注射类产品的产业链包括上游的原料/器械厂家,中游的各类注射产品厂家,下游提供具体服务的医疗机构等。因此,医美注射类产品通过To B实现最终的To C服务。
由于肉毒素应用于医美领域的作用原理与其他医美注射产品不同,下面重点介绍和分析玻尿酸、重组胶原蛋白和再生材料类产品。
1) 玻尿酸:
玻尿酸(Hyaluronic Acid,简称HA),又称透明质酸,是一种天然存在于人体及其它生物体内的高分子多糖体。玻尿酸在人体内有广泛分布,尤其集中在眼玻璃体、关节、脐带、皮肤等部位。玻尿酸在胚胎时期体内的含量最高,随着年龄增长体内含量逐渐减少。
玻尿酸分子基于一种标准化重复二糖模块构建,具有低免疫原性的特点。玻尿酸具有特殊的保水作用,是目前自然界中发现的保湿性最好的物质,被称为理想天然保湿因子。
根据分子量的大小,玻尿酸分为高分子量、低分子量和寡聚玻尿酸,应用场景各不相同,具体如下图所示。

分子量较大的玻尿酸,具有更强的支撑性、黏弹性和抗降解性,常作为塑形填充材料应用于医疗美容中;分子量较小的玻尿酸,能够穿透表皮实现皮肤深层吸收,常用于保湿类的护肤品中。
玻尿酸广泛应用于在各领域,其原料主要可以分为3类:医药级、化妆品级、食品级。其中,作为医美注射类产品使用的玻尿酸属于医药级,按照Ⅲ类医疗器械管理。
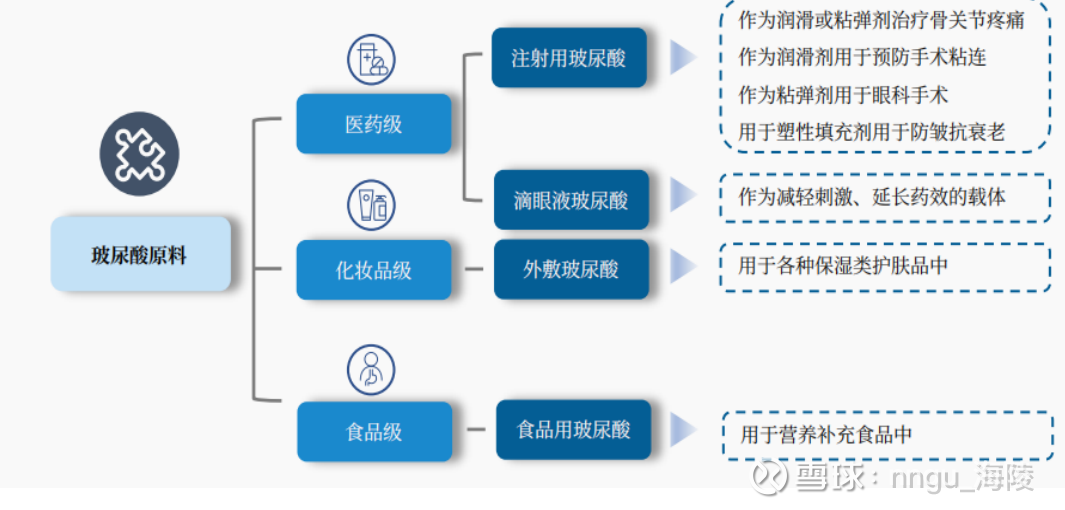
玻尿酸原料的生产工艺主要有:动物组织提取和微生物发酵2种方法。
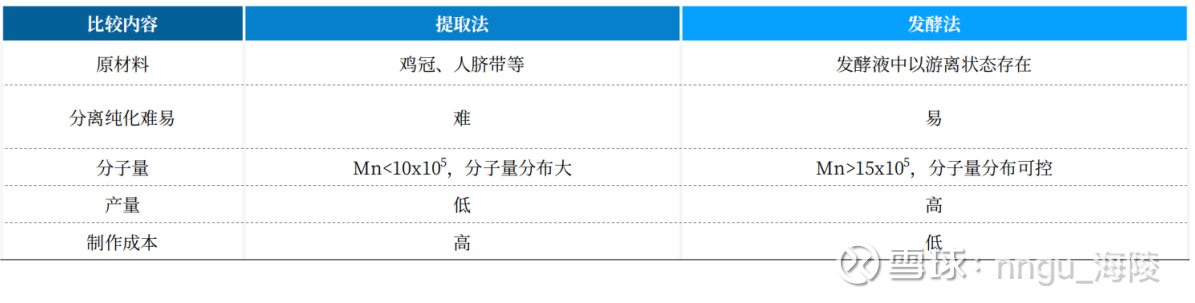
(1)动物组织提取法受到动物资源限制,产量低,分离纯化难度较高,同时该方法对用于提取的动物组织源头需要严格筛选,以最大程度降低动物源性可能引发的用户过敏等不良反应。
(2)微生物发酵法能够通过大规模发酵直接生成游离态的玻尿酸,从而简化并提高了纯化效率,降低了生产成本,适应大规模工业化生产需求。
纯玻尿酸因其易溶于水、吸收迅速、在组织中停留时间短、力学性能较差等特点,须进一步处理后方可更加广泛地应用。
在医美注射类产品领域,最常见的是交联改性。交联是指利用相关交联剂使分子间发生部分或完全交联,形成分子网状结构,增加玻尿酸的强度和塑性支撑能力,延长其降解时间。
玻尿酸交联程度的评价指标为“交联度”,交联度越高,玻尿酸的硬度和强度越大,不易变形,适合用于需要较强支撑力和较长久保持效果的深层组织填充,如隆鼻、填充下巴等;交联度较低的玻尿酸,流动性更好,适合于浅层皮肤的填充和保湿,能提供更好的柔软度和自然度,例如改善泪沟、法令纹等。

随着华熙生物、爱美客和昊海生科等国产玻尿酸头部企业的技术、工艺水平持续提高,国产玻尿酸原料凭借先进的工艺和价格竞争力快速占领全球市场,已成为全球最大的玻尿酸原料生产销售国。
同时,国内更多企业从单纯的玻尿酸原料供应商向自主研发、生产和销售终端产品转型,开始在终端产品层面与国外品牌开展全面竞争。
2) 胶原蛋白
蛋白质指的是由氨基酸借肽键联接起来形成的多肽,然后由多肽经过盘曲折叠形成的具有一定空间结构的物质。
胶原蛋白(Collagen)是蛋白质的一种(结构蛋白),又称胶原多肽(Collagen peptide),占人体总蛋白质含量约30%,是人体内最丰富的蛋白质。蛋白质的主要分类和代表蛋白质参见《初识重组胶原蛋白-巨子生物简析之一》。
胶原蛋白的三螺旋结构由三条以右手螺旋方式紧密缠绕的胶原蛋白分子组成。
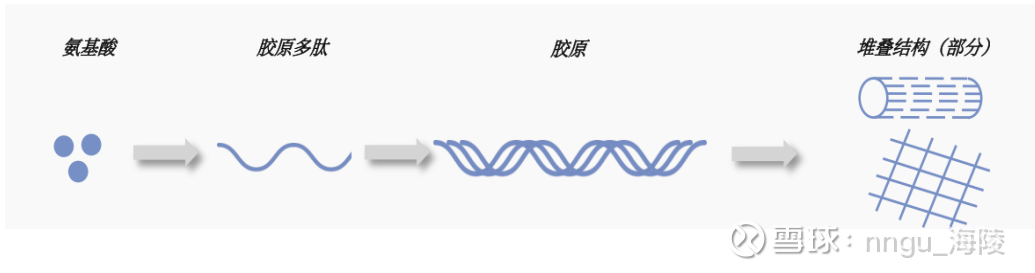
胶原蛋白的主要氨基酸有脯氨酸、甘氨酸、羟脯氨酸等,在三螺旋结构形成过程中,羟脯氨酸羟基能形成强氢键,可提高胶原蛋白强度;脯氨酸和羟脯氨酸能使胶原三螺旋结构发生盘曲和折叠,提高胶原蛋白的稳定性。
胶原蛋白因其独特的生物功能,在皮肤美容、医疗保健等领域展现出广泛应用价值。

胶原蛋白注射产品不仅用于面部填充、除皱,还可能进一步渗透到身体塑形、疤痕修复、脱发防治等领域。
通过上述分析可知,胶原蛋白与玻尿酸在以下几方面很相似:
(1)二者都在人体内天然,广泛存在;
(2)二者都是在婴幼儿时期含量最高,随着年龄增长,含量逐渐降低;
(3)均有两种提取方式:动物组织提取和生物合成发酵,提取方式的优缺点类似;胶原蛋白两种提取方式的优缺点具体参见《初识重组胶原蛋白-巨子生物简析之二》
3) 再生材料:
医美再生注射类产品以生物医用高分子材料为主要成分,通常以微球的形式被注射到真皮层和/或皮下组织,通过刺激人体自身胶原蛋白的再生起到重塑紧致、美容抗衰的作用。下图所示为常见的注射类再生材料。从图中可以看出,除了聚乳酸(PLA)是微生物发酵产物,其他3种产品均为“化学合成”产物。截至2025年,国内有多家公司的产品(“少女针”、“濡白天使”等)获批上市。
化学合成类成分在即时效果上受到较高认可,但温和性、舒适使用感以及适合长期使用的认可度上相对较低。
生物合成类成分(玻尿酸,重组胶原蛋白等)则在“效果持久”方面表现突出,同时在“温和”和“使用舒适”方面处于中高水平。
根据个人当前粗浅的理解,上述3种医用注射材料中,玻尿酸和胶原蛋在人体内天然存在,是人体代谢所需要营养成分,因此它们在进入人体后,能较好地被人体接纳,减少排异反应,能更自然地发挥作用,维持肌肤的正常生理功能。
相比之下,再生材料主要通过刺激人体自身胶原蛋白再生,以达到美容抗衰的效果,但部分化学合成类成分由于并非人体天然存在的物质,在长期使用过程中可能存在一定的不确定性。
2.医疗器械管理
医美注射产品被纳入按照III类医疗器械管理,下面了解一下我国医疗器械相关管理办法。
医疗器械是指直接或者间接用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相关的物品,包括医疗设备与医疗耗材。
根据《医疗器械监督管理条例》,国家对医疗器械按照风险程度实行分类管理,共分三类。
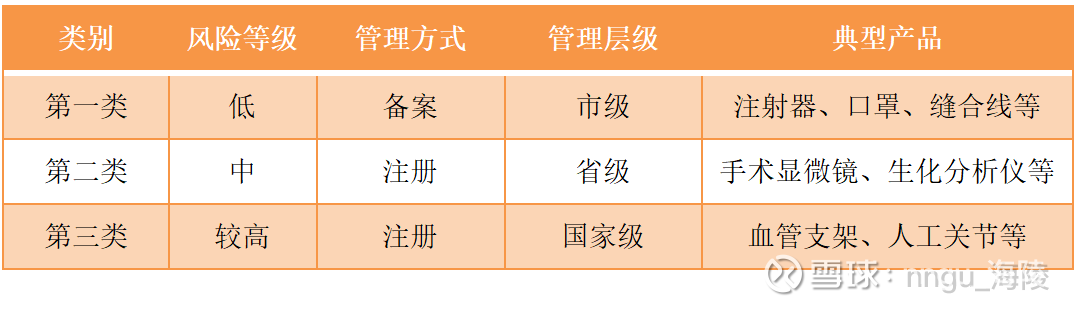
从上表中可见,对第一类风险较低的产品实行备案制,到市级人民政府负责药品监督管理的部门备案就可以。对第二/三类中高风险的产品,实行注册制,管理层级随着产品风险等级的上升而相应提高。
注册制涉及到各种审查,管理层级越高,涉及的环节、部门、人员等越多,所需的时间自然就越长。
第三类医疗器械由国家药品监督管理局发证,要求高、周期长、难度大,对企业而言是个不小挑战;但也正是由于审批难度大,导致III类医疗器械证的稀缺,率先拿到此类证照的企业在市场上可以更早获得商业机会。
此外,在医疗器械产品获得相关部门备案或注册之后,从事医疗器械生产还需要向当地主管部门申请生产许可,其中一类产品生产向市级申请,二类和三类向省级申请。一般情况下,从产品注册到实际生产和销售需2-3个月。
3.公司取证情况
截止2026年1月,公司在骨修复和重组胶原蛋白两个领域,累计获得3张III类医疗器械证。
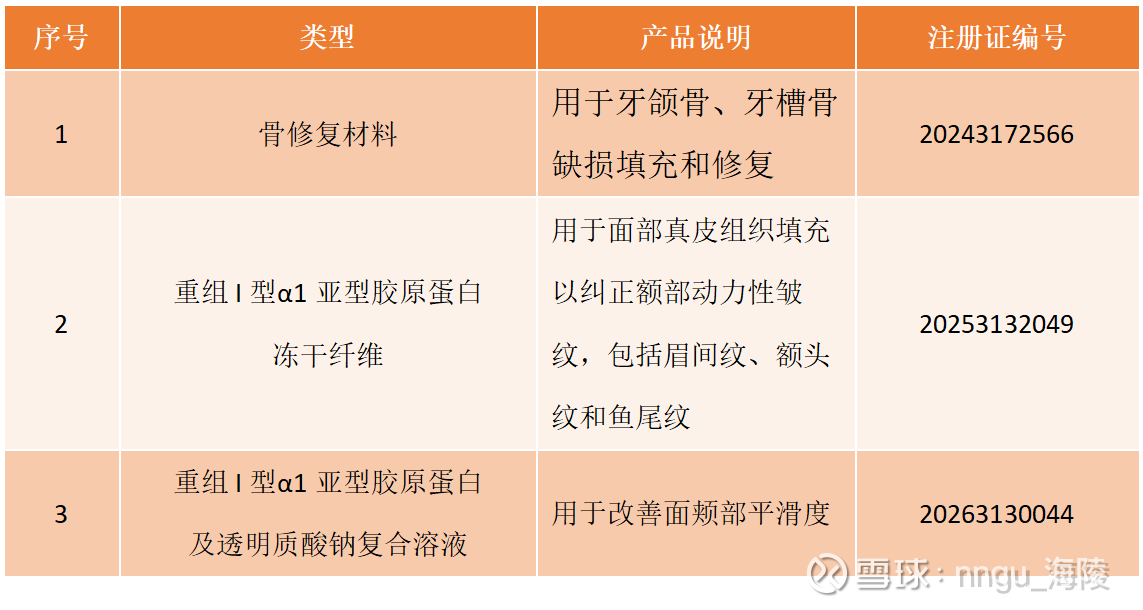
1)骨修复材料:2024年12月17日获批,针对牙颌骨、牙槽骨缺损填充和修复需求,构建的有机无机复合材料。其中,无机成分为羟基磷灰石颗粒,有机成分为大分子多糖,该复合材料既能快速塑形不塌陷,又具有引导骨再生的修复作用,可以加快愈合进程。
笔者是牙周炎患者,由于牙槽骨严重缺损种过牙,过程中使用了骨修复材料以补充缺失的牙槽骨,植入材料后大约半年到一年,形成新的牙槽骨后才具备种牙条件。在切身体会到骨修复材料的重要作用后,日常也对该细分行业多了一份关注。
此外,在口腔种植牙过程中还需要用到可吸收生物膜,该生物膜是以重组胶原蛋白为主要原料,经过物理交联制备而成的膜状产品,主要用于引导骨组织再生,具有良好的骨组织诱导再生功能、可生物降解性、低抗原性和良好的组织相容性。公司正在进行可吸收生物膜研发,并列入III类医疗器械申请计划。相关数据表明:一台种植牙手术中平均需要约2000元的口腔修复材料。
据国内三甲口腔医院医生反馈,目前骨修复材料和可吸收生物膜,已经大面积国产化,临床表现方面国产和瑞士进口产品表现相当。国产产品进了医保目录后,通过集采进入医院,相比进口产品有明显的价格优势,各大医院已在广泛使用国产材料。该细分领域相关国产厂家和产品较多,竞争较为激烈。
2)重组胶原蛋白:于2025年10月和2026年1月,拿到2张基于“重组I型α1亚型胶原蛋白”的III类证。其中第一款产品形态为“冻干纤维”,第二款产品形态为“复合溶液”。
公司的首批械III产品选择了重组I型胶原蛋白,与$锦波生物(BJ920982)$ 已上市的III型胶原蛋白形成了差异化,暂时避开了产品同质化竞争。
本次获批2个产品中的重组胶原蛋白成分:选用人天然I型α1单链氨基酸序列中的305-1057位(共753个氨基酸),注册证中明确标注"不具有三螺旋结构"。该表述体现了监管机构对重组胶原蛋白产品鉴定的专业和严谨,同时也为后续“三螺旋结构”产品预留了空间。
(1) 冻干纤维
该产品用于面部真皮组织填充以纠正额部动力性皱纹,包括眉间纹、额头纹和鱼尾纹。根据产品技术审评报告披露:使用前,需注入无菌生理盐水将其配置成4mg/mL的溶液;产品连续注射3次为一个疗程/周期,每次注射间隔30天;单部位单次最大注射剂量15mg,单次个体总量33mg;产品仅限单疗程/单周期使用,最多注射3次,不得进行多个疗程/多个周期的反复注射。
意味着该产品每个消费者只能使用1个疗程,连续注射3次,时间间隔90天。由于目前多疗程多周期,反复注射的安全性、有效性未经验证,长期使用的风险未知。通过产品上市后的数据收集和分析,在确保安全性的前提下,未来该产品或其他新产品也许会逐渐开展多疗程注射。
(2) 复合溶液
全球首个“用于改善面颊部平滑度的”重组胶原蛋白及透明质酸钠复合溶液植入剂,从产品名字就可以看出该复合溶液含有“重组胶原蛋白”和“透明质酸钠”两种成分。
上述两种成分结合在一起,具有促进组织重生和组织支撑双重作用,属于强强联合,达到“吃一片顶两片”的效果。可见,这两种成分对皮肤都是有效成分,并不存在“有你没有”的替代性竞争关系,$华熙生物(SH688363)$ 于2025年11月向国家药品监督管理局提交了基于重组III型胶原蛋白成分的产品,正在等待审批过程中。可见,市场上关于两种成分的各种纷争,更多是出于商业竞争的噪音。
未来一段时间内,这两种成分的复合产品很可能成为医美注射产品的重要组成,基于各种类型的重组胶原蛋白(I型、III型、I型+III型等)和透明质酸钠(不同分子量,不同交联程度等)分子,将组合出多种类型产品。
III类医疗器械注册证是产品上市的前提条件,正式销售前还需取得生产许可证并通过生产合规性核查。根据上节分析,从获得注册到实际销售通常需2-3个月,这就意味着公司的两款基于重组胶原蛋白的械III类产品,预计2026年1季度具备正式对外销售条件。
4.胶原蛋白械III产品竞争格局
中国医美市场正从“量的增长”向“质的提升”转型,胶原蛋白作为兼具生物相容性与组织修复能力的材料,已成为仅次于透明质酸的第二大医美填充剂品类。
2024-2025年期间,国家药品监督管理局加快审批速度,截至2026年1月,国内共计有15款械III胶原蛋白产品获批。其中:
1)猪胶原:4张,双美生物3张、艾佰瑞1张;
2)牛胶原:6张,斐缦1张、荷兰汉福1张、圣诺华1张、珂瑞康2张、崇山生物1张;
目前,动物胶原的产品数量领先于重组胶原蛋白产品,一方面是动物胶原蛋白产品进入市场较早,另一方面原因是动物胶原蛋白的天然三螺旋稳定结构等在技术上具有一定优势。
根据前面的系列文章分析,基于中国发达的生物合成与工程化规模量产的潜力,重组胶原蛋白原料成本与价格进一步下降只是时间问题。同时,随着基于三螺旋结构的重组胶原蛋白产品的成功研发和规模量产,产品将更加具备竞争力,基于重组胶原蛋白成分的产品有望获得更多的市场份额。
5.小结
公司当前对“可复美”系列产品依赖严重,近几年公司坚持“树品牌、拓渠道、强报批”的战略,加速了对医美械III产品的报批,截止2026年1月累计获得3张械III产品证,为公司的“第二增长曲线”奠定了良好基础。
公司2个重组胶原蛋白械III产品有望在2026年1季度开始对外销售,考虑到当前内需不足的大背景,产品放量速度可能比预想中的慢,“第二增长曲线”的斜率将会比较低。
此外,公司的骨修复材料等用于严肃医疗产品面临激烈竞争,打开市场和占领一定市场份额,同样需要时间和管理层持续不断的努力。
总之,公司积正极拓展产品矩阵,努力实现“第二增长曲线”,走在正确的路上,但是从取证产品到消费者买单的产品,中间依然有一段较长的路要走。
主要参考文献:《2025医美注射类产品行业发展现状与未来趋势蓝皮书》