甘李药业未来可期(数据持续更新中)


$甘李药业(SH603087)$ $贵州茅台(SH600519)$ $腾讯控股(00700)$
药明康德荣昌生物新华保险创新药ETF港股创新药ETF五粮液常山药业众生药业
因过往发的有关甘李药业的帖子零乱繁多,不方便阅读了解,现均已删除处理。
(此贴内容仅供讨论,不作为买卖甘李药业股票的建议,观者责任自负)
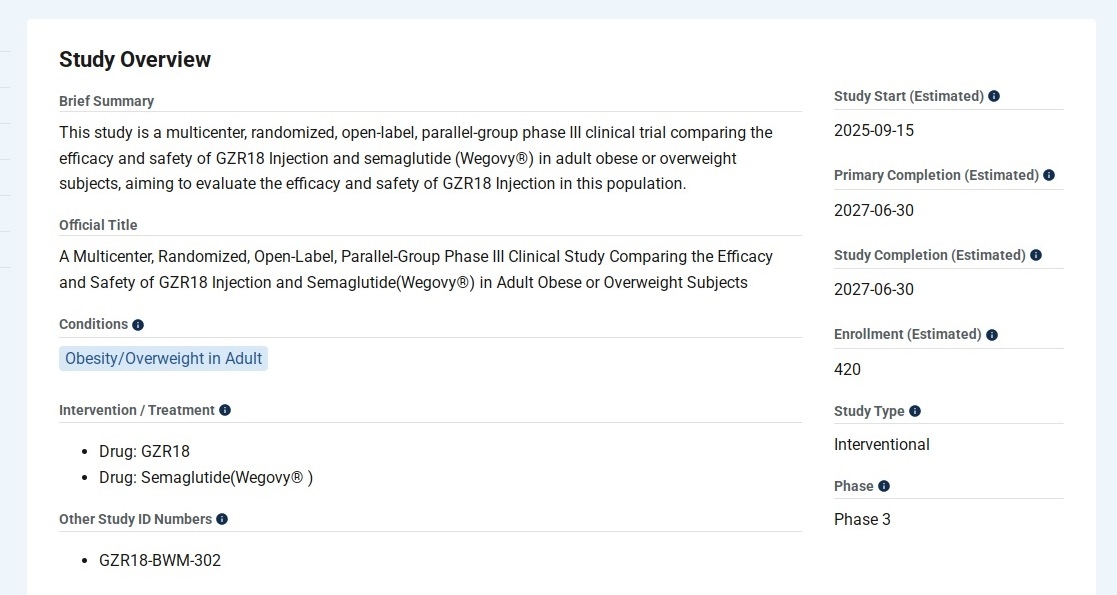
一、甘李药业GZR18几项三期临床进展情况一览
(已完成的 II 临床研究结果显示,治疗24周后,每两周一次18 mg博凡格鲁肽注射液组的HbA1c降幅显著高于司美格鲁肽组(P<0.001)。同时,在体重减轻、血脂谱改善等方面,博凡格鲁肽注射液组均展现出积极结果。)
III 期试验对照药物信息汇总:
1.诺和泰(Semaglutide):是诺和诺德(中国)制药有限公司生产的一种用于治疗2型糖尿病的药物,通过模拟天然激素GLP-1的功能来帮助控制血糖水平,每周注射一次。
最新状态:招募完毕。
登记时间:2025年11月。
拟入组人数:1100人。
实际入组人数:1133人。
实验周期:44/52周。

2.诺和盈(司美格鲁肽):是诺和诺德制药公司生产的一款用于长期体重管理的减重药物,每周注射一次。
最新状态:招募完毕。
登记时间:2026年1月12日。
拟入组人数:471人。
实际入组人数:477人。
试验周期:52/55周。
3.安慰剂
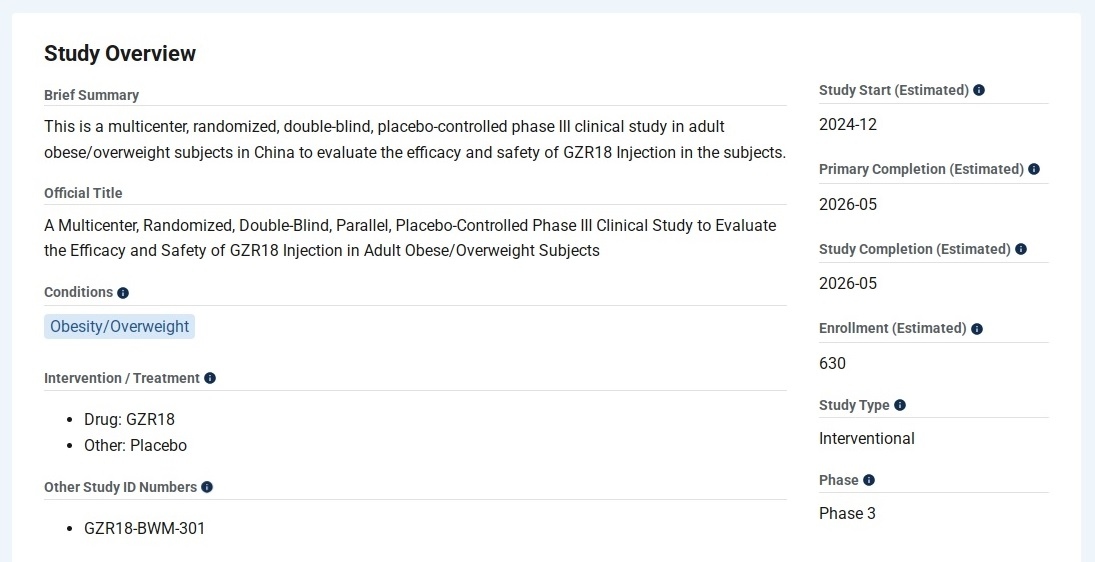
肥胖和超重者GZR18对照安慰剂的三期临床
最新状态:招募完毕。
登记时间:2025年11月。
拟入组人数:630人。
实际入组人数:640人。
试验周期:48周。
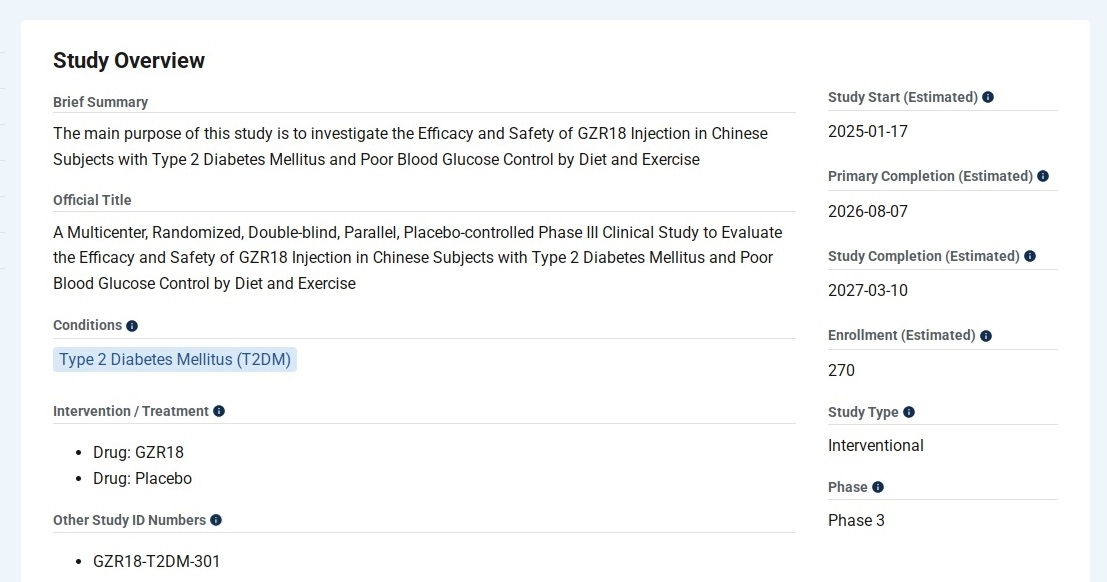
单纯饮食运动控制不佳者GZR18对照安慰剂的三期临床
最新状态:招募完毕。
登记时间:2025年11月。
拟入组人数:270人。
实际入组人数:274人。
试验周期:44/52周。
☆☆☆☆☆甘李药业启动针对肥胖和超重适应症GZR18每月注射一次的 III 期临床试验。
最新状态:进行中,尚未招募。
登记时间:
拟入组人数:500人。
实际入组人数:
试验周期:24/25周。

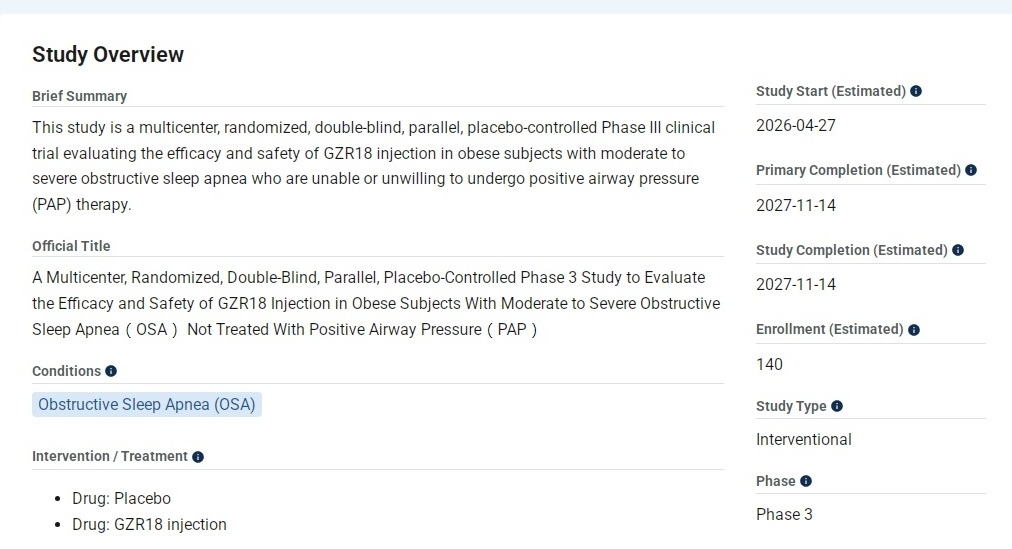
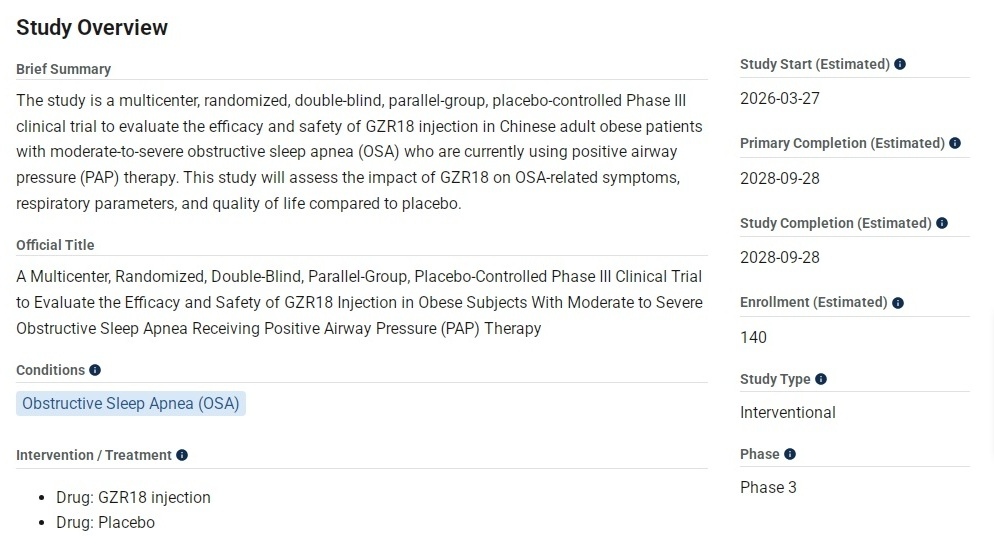
☆☆☆☆☆本研究是一项多中心、随机、双盲、平行、安慰剂对照的 III 期临床试验,评估 GZR18 注射液对未接受气道正压通气 (PAP) 治疗的阻塞性睡眠呼吸暂停肥胖受试者的疗效和安全性。
最新状态:进行中,尚未招募。
登记时间:2026年3月27日
拟入组人数:140人。
实际入组人数:
试验周期:52周。
☆☆☆☆☆本研究是一项多中心、随机、双盲、平行、安慰剂对照的 III 期临床试验,评估 GZR18 注射液对接受气道正压通气 (PAP) 治疗的阻塞性睡眠呼吸暂停肥胖受试者的疗效和安全性的 III 期临床研究。
最新状态:进行中,尚未招募。
登记时间:2026年3月30日
拟入组人数:140人。
实际入组人数:
试验周期:52周。
二、甘李药业GZR4几项三期临床进展情况一览
(已完成的 II 临床研究结果显示,治疗16周后,在基础胰岛素治疗控制不佳的2型糖尿病(T2DM)患者中,每周一次GZR4注射液组的HbA1c降幅显著优于每日一次德谷胰岛素注射液组(-1.26% vs -0.87%,p<0.01)。同时GZR4注射液能有效降低T2DM患者的空腹血糖,并延长葡萄糖目标范围内时间,且安全性良好。)
III 期试验对照药物信息汇总:
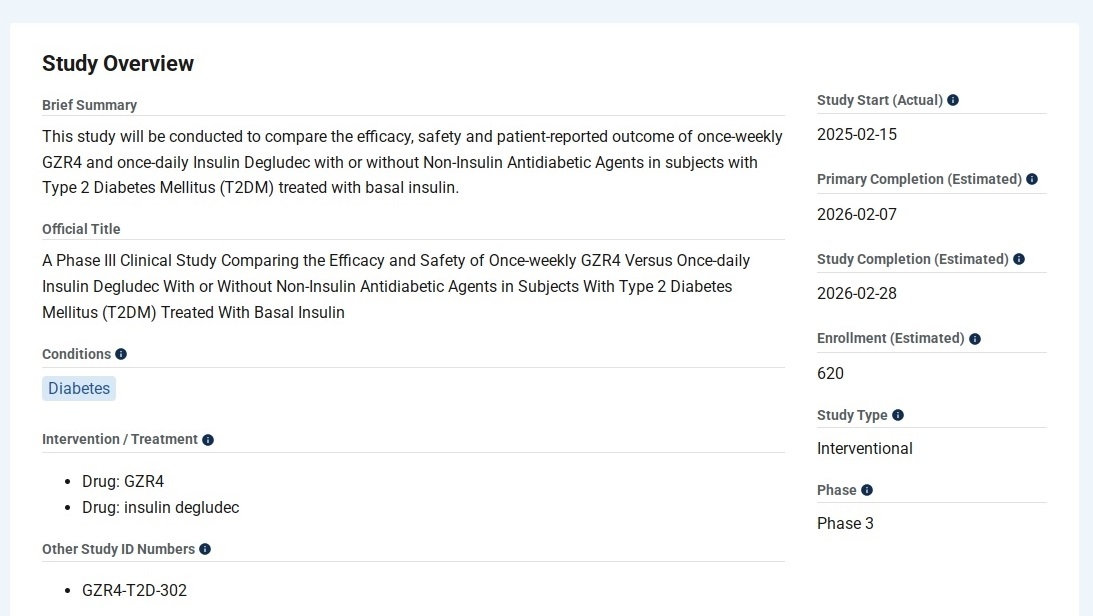
1.super—2 既往已使用基础胰岛素治疗的2型糖尿病患者
诺和达德谷胰岛素:是诺和诺德(中国)制药有限公司生产的一种长效胰岛素,其半衰期长达约25小时,作用时间可长达42小时。
登记时间:2025年11月。
拟入组人数:620人。
实际入组人数:631人。
试验周期:26周。
最新状态(发布时间2026年3月30日):III 期试验达成主要研究终点。GZR4较德谷胰岛素展现出更优的血糖控制疗效。相较每日一次德谷胰岛素,每周一次GZR4治疗26周,在降低HbA1c水平方面表现出优效性(较基线的变化:−1.00% vs −0.58%);组间治疗差异估计值为−0.42%,该差异具有统计学意义。同时,GZR4也展现出了更好的安全达标率:在达成HbA1c<7.0%或≤6.5%的血糖控制目标且不伴有临床意义(2级)的或严重(3级)低血糖这一临床指标上,每周一次GZR4治疗组显著优于每日一次德谷胰岛素治疗组。
每周给药一次GZR4显示出良好的安全性和耐受性,两组均未发生严重(3级)的低血糖事件。
2.诺和期依柯胰岛素:是诺和诺德制药公司研发生产的一种长效胰岛素类似物,主要功效是治疗成人2型糖尿病,作用时间可覆盖一周。。
最新状态:招募中。
登记时间:
拟入组人数:300人。
实际入组人数:
试验周期:26周。

3.来得时甘精胰岛素:是赛诺菲公司研发的一种长效胰岛素类似物,它的起效时间一般在注射后的2—3小时,作用持续时间可达24—30小时,平稳地控制血糖长达1天以上。
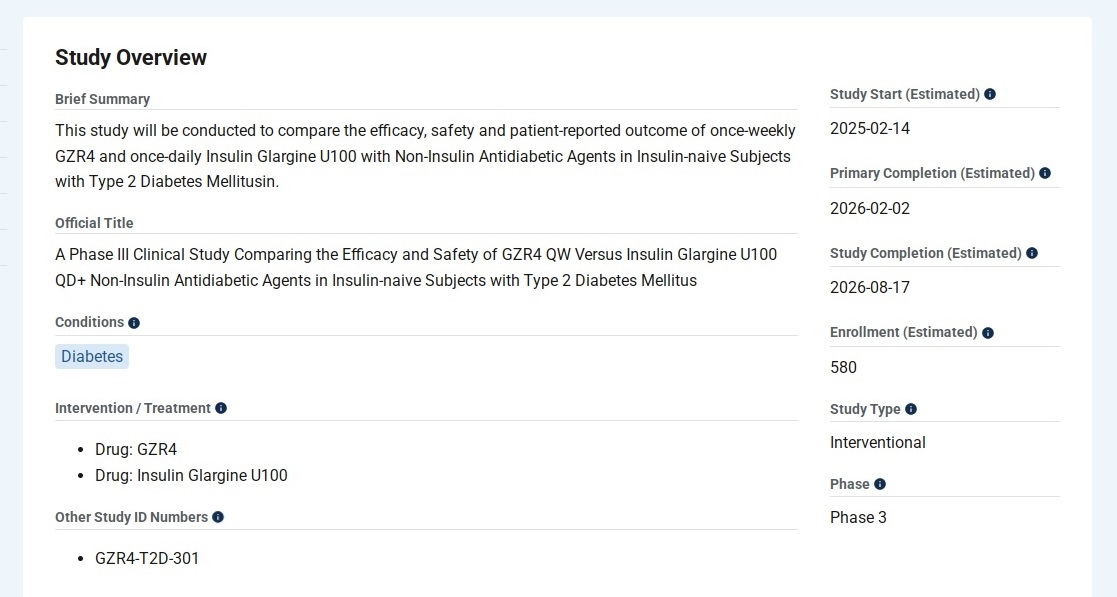
① 一项评估GZR4在未使用过胰岛素的2型糖尿病(T2DM)受试者中的疗效和安全性的III期临床研究
登记时间:2025年11月。
拟入组人数:580人。
实际入组人数:588人。
试验周期:26/52周。
最新状态(发布时间2026年3月30日):III 期试验达成主要研究终点。GZR4较甘精胰岛素U100展现出更优的血糖控制疗效。相较每日一次甘精胰岛素U100,每周一次GZR4治疗26周,在降低HbA1c水平方面表现出优效性(较基线的变化:−1.45% vs −1.22%);组间治疗差异估计值为−0.23%,该差异具有显著统计学意义。同时,GZR4也展现出了更好的安全达标率:在达成HbA1c<7.0%或≤6.5%的血糖控制目标且不伴有临床意义(2级)的或严重(3级)低血糖这一临床指标上,每周一次GZR4治疗组显著优于每日一次甘精胰岛素U100治疗组。
每周给药一次GZR4显示出良好的安全性和耐受性,两组均未发生严重(3级)的低血糖事件。
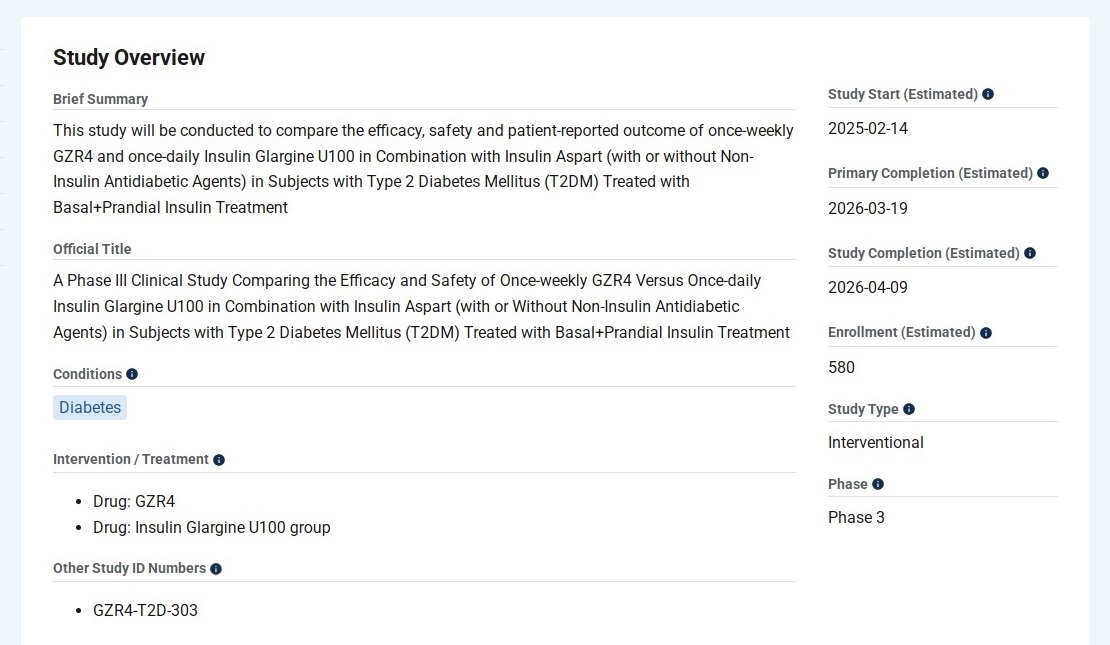
② 一项评估GZR4在接受基础+餐时胰岛素治疗的2型糖尿病(T2DM)受试者中疗效和安全性的III期临床研究
最新状态:招募完毕。
登记时间:2025年11月。
拟入组人数:580人。
实际入组人数:597人。
试验周期:26周。
三、甘李药业出海一览表
甘李药业出海全纪录(可能有遗漏)
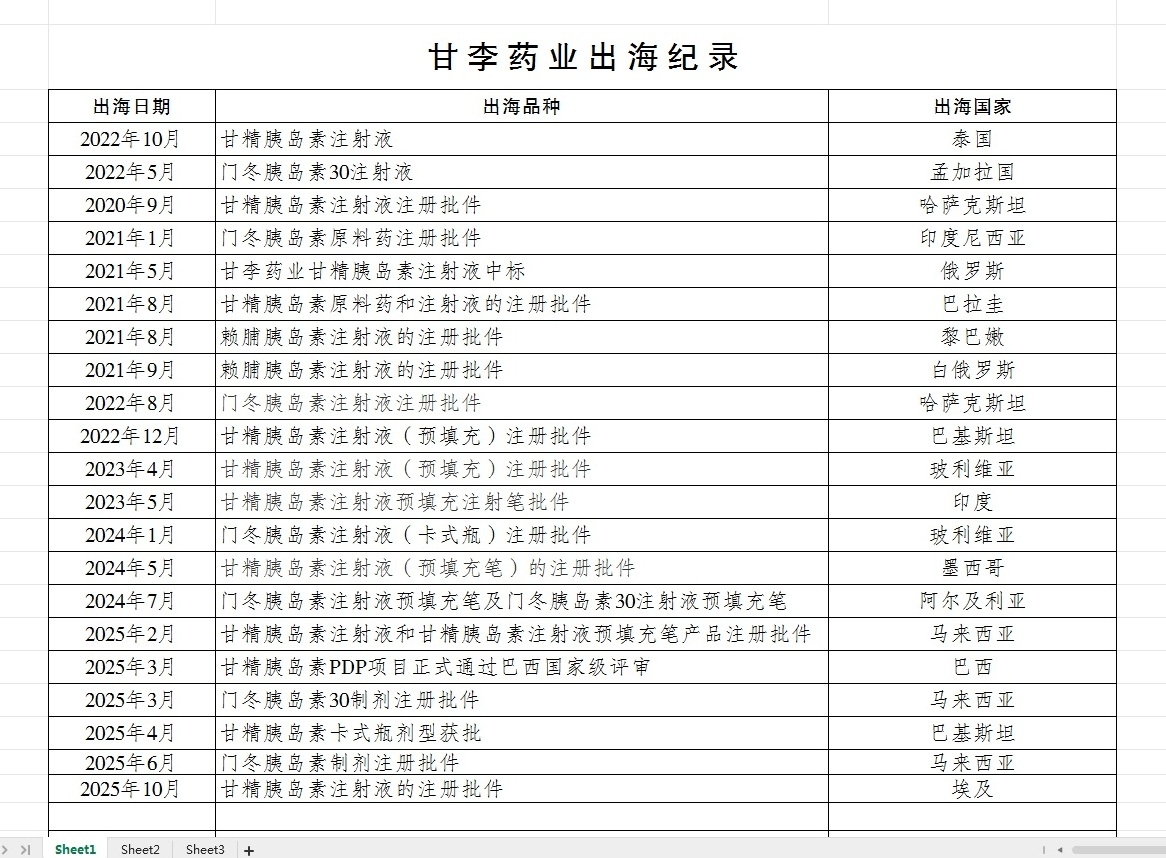
1.新兴国家情况
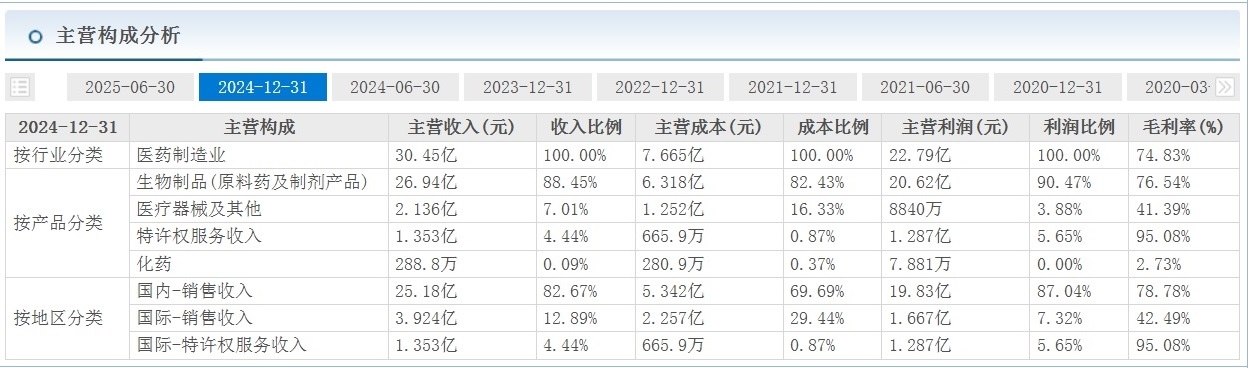
①2024年年报国际销售收入3.924亿,国际特许服务收入1.353亿。
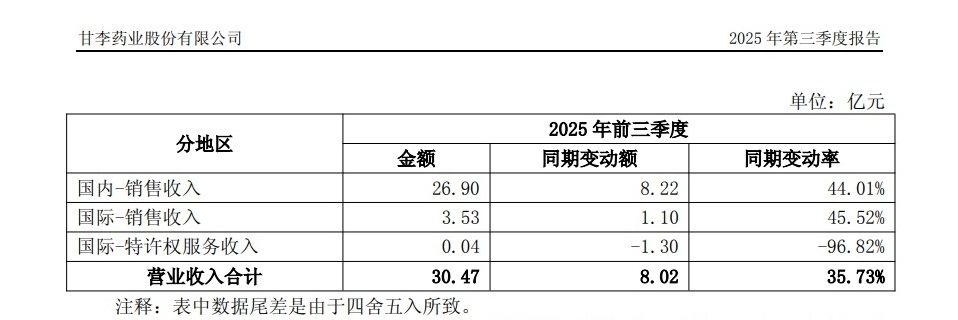
②2025年三季报海外销售收入3.53亿。
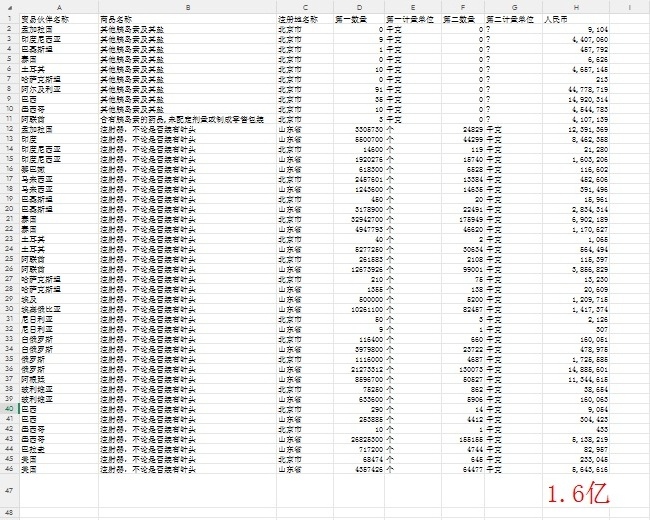
2025年四季度甘李药业海外销售海关查询数据(毛估估):
③GZR18出海露尖角☆☆☆☆☆
2025年11月25日,甘李药业与拉美地区PC公司达成GZR18独家许可商业化协议。
2025年11月25日,甘李药业与印度Lupin公司签署GZR18独家授权与供应协议。
2.欧盟情况(甘李药业未得到欧盟授权前)
①基本数据:欧盟成员国(27个)奥地利、比利时、保加利亚、塞浦路斯、克罗地亚、捷克、丹麦、爱沙尼亚、芬兰、法国、德国、希腊、匈牙利、爱尔兰、意大利、拉脱维亚、立陶宛、卢森堡、马耳他、荷兰、波兰、葡萄牙、罗马尼亚、斯洛伐克、斯洛文尼亚、西班牙、瑞典。累计20-79岁人群中糖尿病患者人数达:6560万人。
②欧盟历史数据
2023年至2024年北京山东出口到欧盟的胰岛素分别为:0.3万元;41.57万元。
2025年1-10月北京山东出口到欧盟的胰岛素贸易额为:0.59万元。
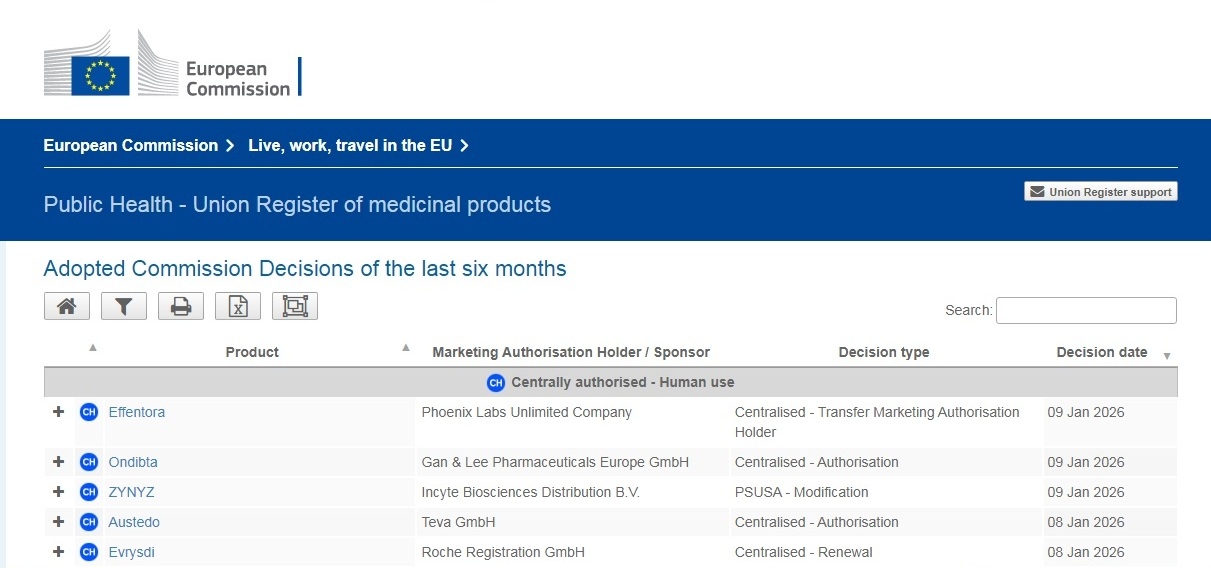
③欧盟进展情况
☆☆☆☆☆2026年1月9日,欧盟会议审议通过集中授权Ondibta上市许可。
☆☆☆☆2026年2月17日甘李药业赖脯胰岛素、门冬胰岛素获得EMA的CHMP会议“positive”意见。
GZR4欧洲临床进展
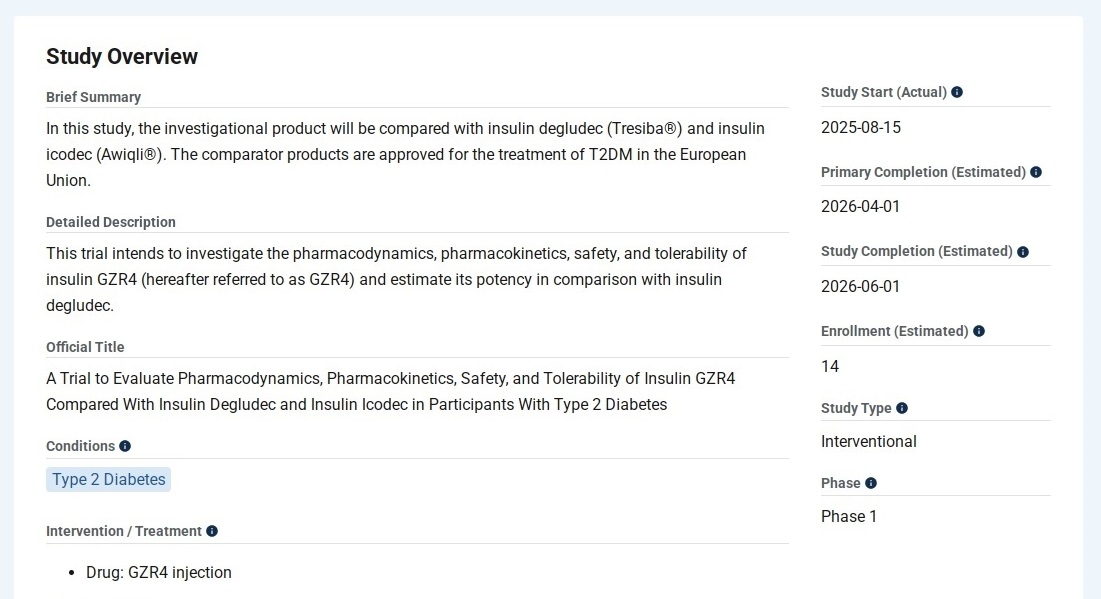
临床: I 期,试验地点:德国,试验对象:二型糖尿病。
GZR33欧洲临床进展

临床: I 期,试验地点:德国,试验对象:一型糖尿病。(2025年11月17日登记)
3.美国情况
①在美国本土甘李药业 GZR18 与 替尔泊肽 头对头 II 期临床进展情况:285个样本数,预计2026年上半年完成。
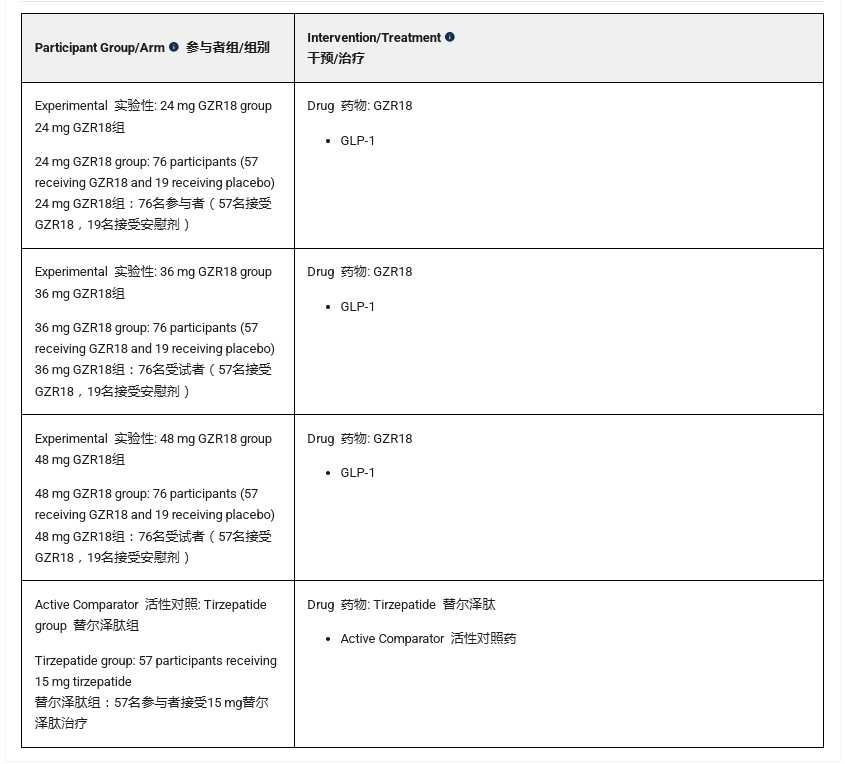
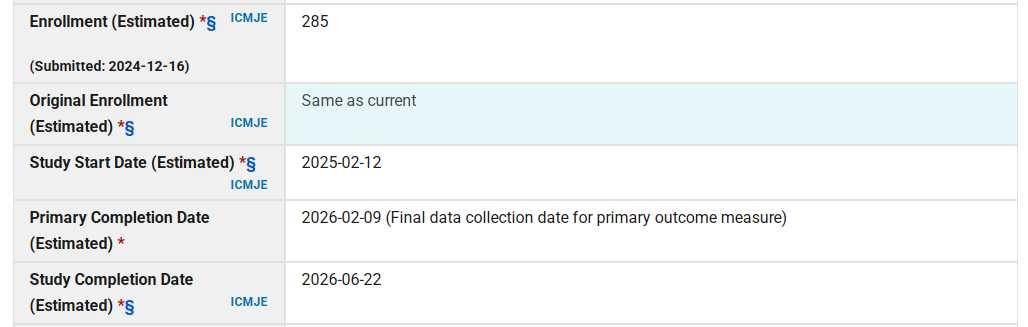
临床试验地点:美国本土十多个州。
②甘李药业门冬胰岛素赖脯胰岛素美国上市申请进展情况(还处在整改沟通阶段)
2025年9月4日,FDA宣布实时发布完全回应函,并公布此前未公开的89封批次文件。

包含2024年3月26日、4月12日FDA的下属部门Center for Drug Evaluation and Research向甘李药业发出的CRL。



四、甘李药业新药进展
1.☆☆☆☆☆2025年11月11日甘李药业在美国肥胖周大会上展示GZR18口服片剂国内 I 期临床数据:
样本量:92名中国成年健康受试者
给药方案:每日一次口服,目标剂量60 mg。
主要终点:相对生物利用度、药代动力学(PK)、药效学(PD)、安全性/耐受性,及进食时间对PK/PD/安全性/耐受性的影响。
体重变化:用药2周,平均较基线下降4.16%;停药1周,继续下降0.51%,累计4.67%;停药后21天,体重与BMI均未回到基线。
PK/PD特征:吸收良好,支持每日一次口服;单次与多次给药均呈剂量反应关系
安全性 总体安全且耐受性良好;最常见不良事件为胃肠道反应,未见非预期安全性信号。
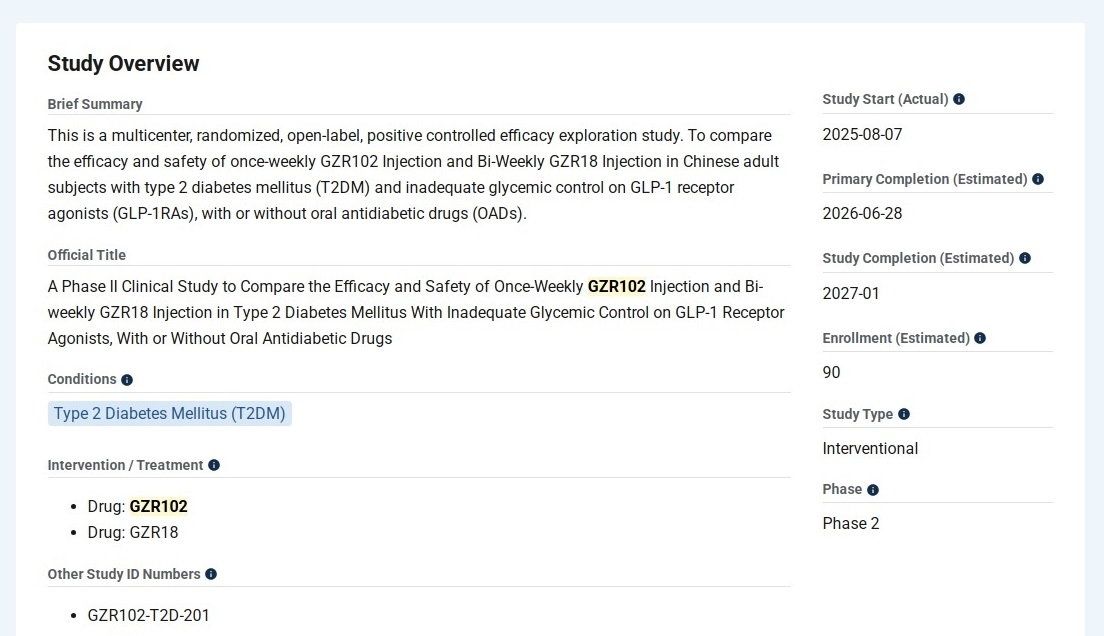
2.☆☆☆GZR102国内二期临床情况:2025年11月完成入组,拟入组人数90人,实际入组人数98人。
3.一项随机、双盲、单次给药、平行比较GLR1044注射液与度普利尤单抗注射液(达必妥®)在中国健康成年男性受试者中的生物相似性对比研究临床 I 期。
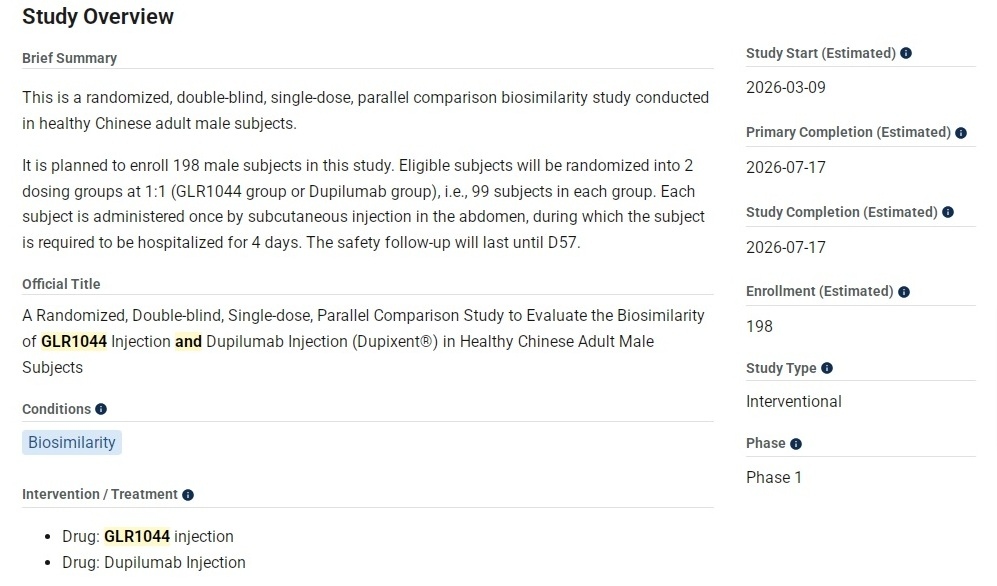
拟入组人数:198人。
最新登记时间:2026年1月12日。
4.GZR101-80二期临床2026年2月4日最新登记动态:

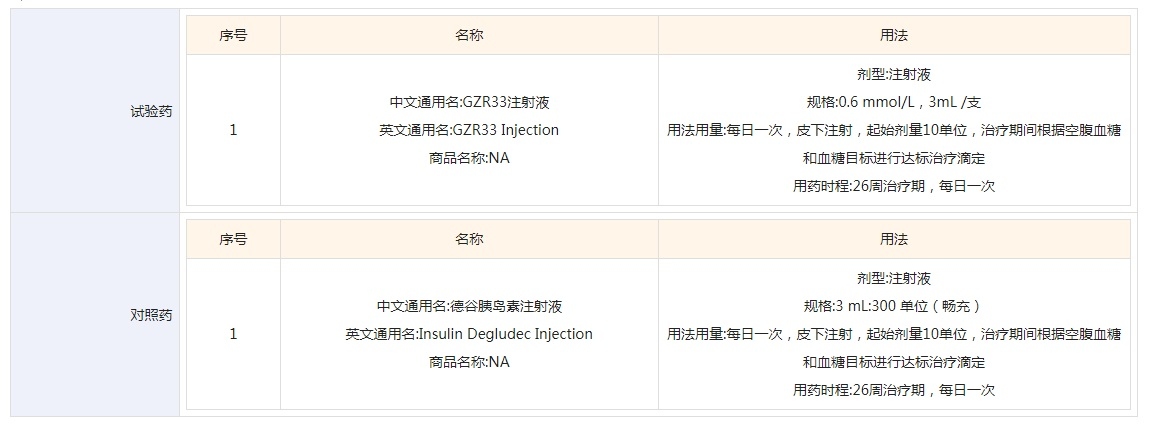
5.☆☆☆☆在口服降糖药物控制不佳的2型糖尿病患者中比较GZR33注射液和德谷胰岛素注射液的有效性和安全性的随机、开放、平行对照的多中心 III 期临床研究
登记日期:2026年3月27日;
拟入组人数:350人;
试验时长:26周。
6.GLR2037 片在晚期前列腺癌患者中的安全性、耐受性、药代动力学特征和初步疗效的单臂、开放、多中心的 I 期临床研究
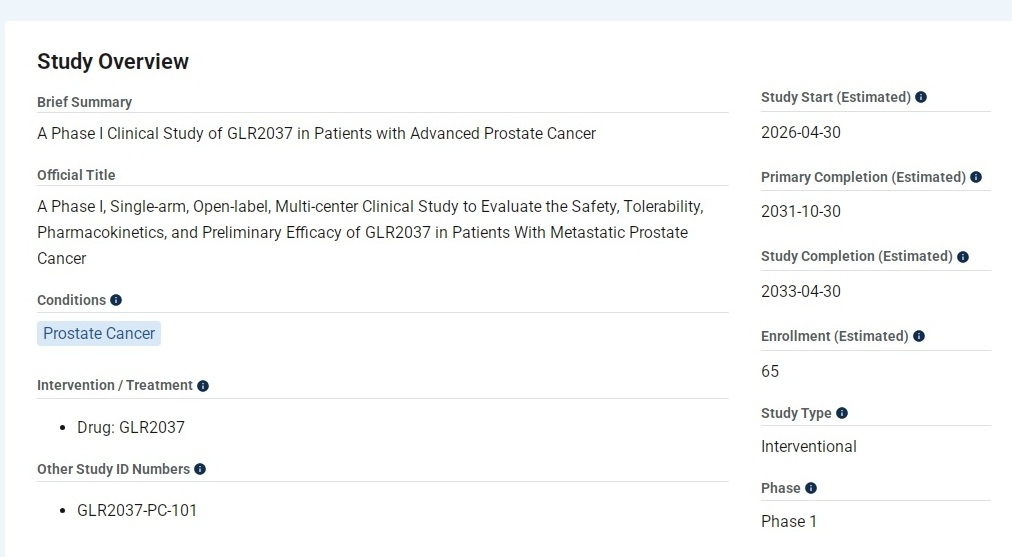
2026年4月3日完成首试给药。

一期临床试验主要指标:
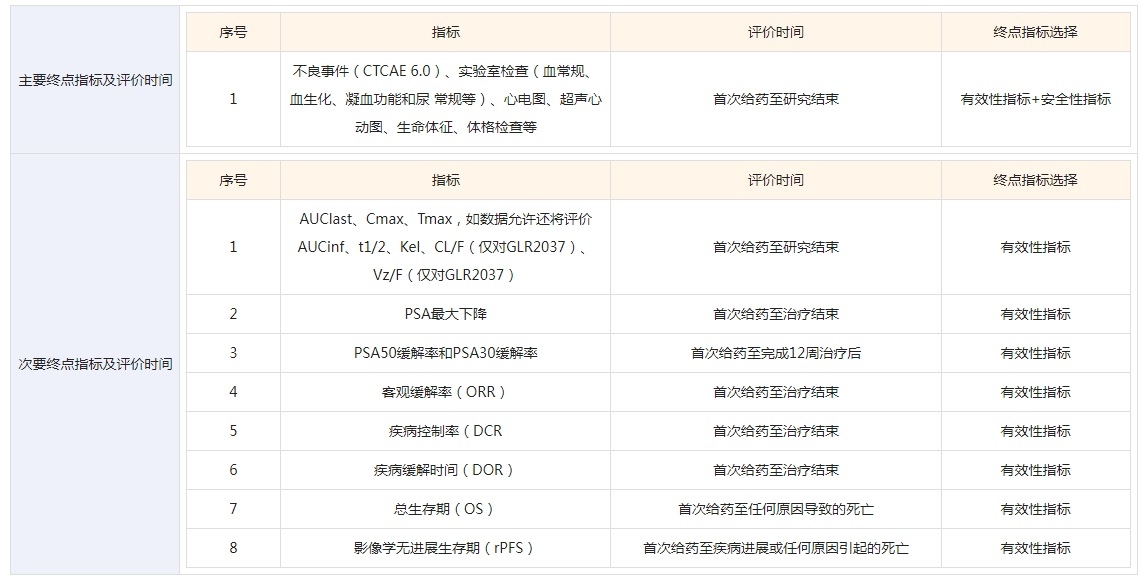
五、最新合作动态
2025年12学9日,甘李药业与晶泰控股签署合作代谢疾病领域AI多肽创新药的研发合作及AI技术平台使用授权协议。
六、甘李药业待上市仿制化药
达格列净片、美沙拉秦肠溶缓释胶囊、西格列汀二甲双胍片、利格列汀片上市在审。
1.达格列净片:是一种降糖类药物,主要用于成人2型糖尿病的血糖控制,能够抑制原尿中钠和葡萄糖的有效吸收,对高血压的症状能够起到预防的作用。
2.美沙拉秦肠溶缓释胶囊:是一种用于治疗炎症性肠病的药物,如溃疡性结肠炎和克罗恩病。它能够减少肠道炎症,缓解症状。
3.西格列汀二甲双胍片:是一种复方降糖药,结合了西格列汀和二甲双胍两种成分。西格列汀是一种DPP-4抑制剂,能够增加体内GLP-1的水平,从而促进胰岛素分泌;二甲双胍是一种大剂量双胍类药物,能够减少肝脏葡萄糖的产生,提高身体对胰岛素的敏感性。
4.利格列汀片:是一种口服降糖药,属于DPP-4抑制剂。它能够通过增加体内GLP-1的水平,促进胰岛素分泌,从而降低血糖。
5.恩格列净片:是一种降糖类药物,属于SGLT2抑制剂。它能够通过抑制肾脏对葡萄糖的重吸收,增加尿液中葡萄糖的排泄,从而降低血糖。
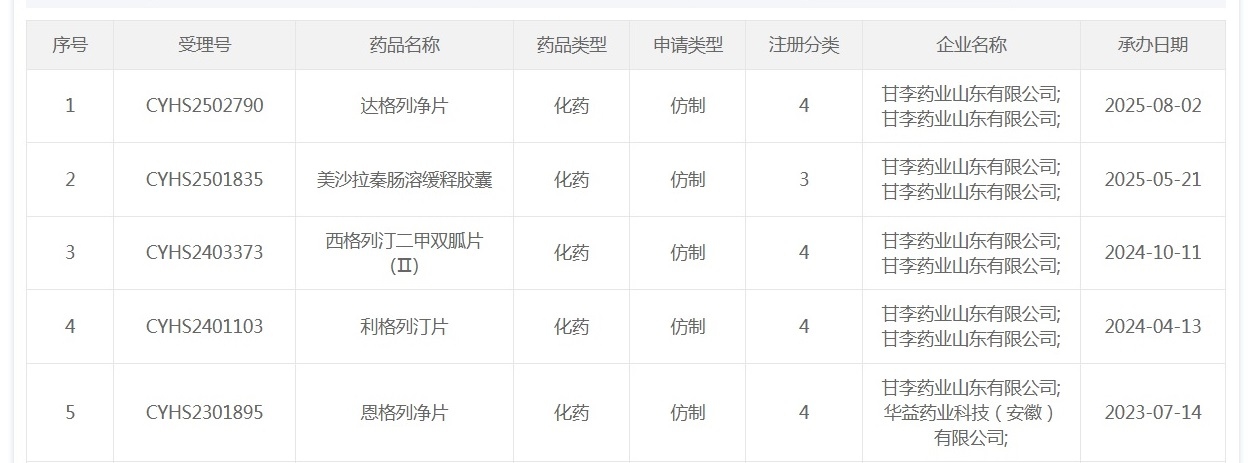
其中,恩格列净片于2025年2月11日拿到注册批件。
静待花开……
