全球创新药物TLX591-Tx的全球III期临床试验第一部分达到主要目标
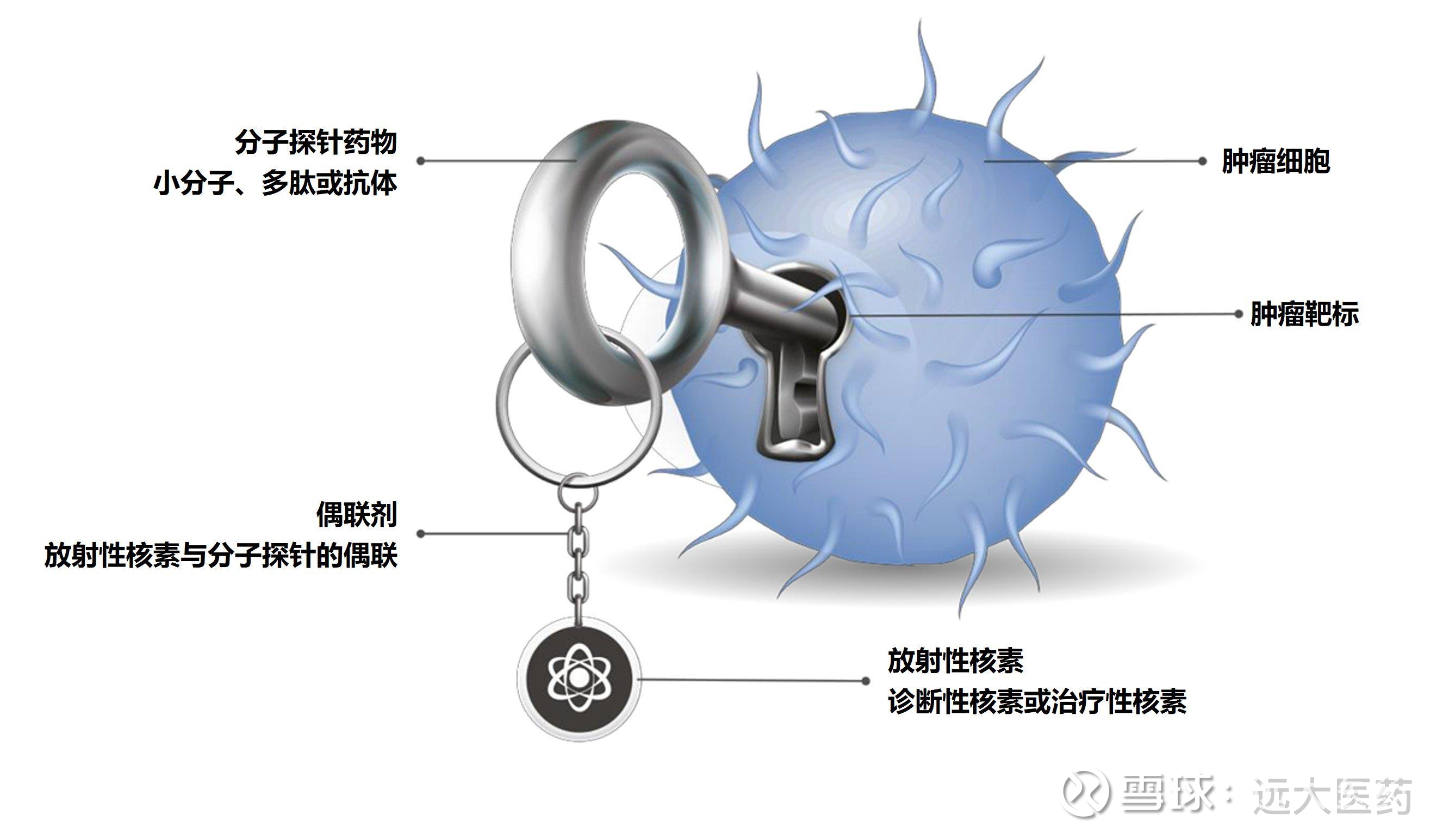
• TLX591-Tx为全球首创(first-in-class)镥标记的治疗性放射性抗体药物偶联物(rADC)候选药物;
• ProstACT Global是一项随机、开放标签的国际多中心III期临床试验,旨在评估TLX591-Tx联合标准疗法对比单独使用标准疗法治疗PSMA阳性的转移性去势抵抗性前列腺癌(mCRPC)患者;
• 第一部分(安全性和剂量学引导)数据表明,TLX591-Tx安全性及耐受性良好,试验血液学事件可控,剂量学数据证实肿瘤摄取。
近日,$远大医药(00512)$ 在放射性核素偶联药物(RDC)领域的战略合作伙伴Telix Pharmaceuticals Limited (ASX: TLX; NASDAQ: TLX, “Telix”)用于治疗前列腺癌的全球创新药物TLX591-Tx (177Lu rosopatamab tetraxetan)的国际多中心III期临床试验(ProstACT Global)的第一部分(安全性和剂量学引导)已成功达到主要目标,证明了该产品的安全性和耐受性,且未观察到新的不良反应[1]。
关于TLX591-Tx及其临床试验:
TLX591-Tx为全球首创(first-in-class)镥标记的治疗性放射性抗体药物偶联物(rADC)候选药物,其靶向性和药理学特性与现有已上市的前列腺特异性膜抗原(PSMA)靶向小肽分子显著不同,旨在实现高内化率、长滞留时间和对PSMA的高度选择性。[2]
ProstACT Global是一项随机、开放标签的国际多中心III期临床试验,旨在评估TLX591-Tx联合标准疗法(阿比特龙、恩扎卢胺或多西他赛)对比单独使用标准疗法治疗PSMA阳性的转移性去势抵抗性前列腺癌(mCRPC)患者。该试验分为两部分:第一部分为安全性和剂量学导入期,已完成全部36例患者的入组;第二部分为2:1随机分组的全球扩展研究,拟入组约490例患者。符合条件的患者必须经68Ga-PSMA-11 PET显像剂(如TLX591-CDx (Illuccix®))确诊为mCRPC,且接受过一种雄激素受体通路抑制剂(ARPI)治疗。
试验第一部分的数据将会递交予美国食品药品监督管理局(FDA),以推进在美国开展该III期临床研究的第二部分。同时,Telix将继续在已获批开展临床试验的地区(包括中国大陆)推进第二部分的受试者招募。
本次该试验第一部分的主要研究结果包括:
• 安全性及耐受性:联合治疗组的安全性良好,TLX591-Tx的耐受性与既往研究结果一致,未观察到新的安全性信号。
• 血液学事件:血液学事件均为短暂且可控,其发生率与此类疗法和疾病程度的预期情况相符。
• 剂量学数据:关键器官的辐射暴露远低于既定安全限值,所有队列的肿瘤部位均观察到药物摄取,且药代动力学显示药物活性可持续15天,未见明显药物间相互作用。[1]
与其他PSMA靶向小分子放射性配体疗法(RLT)相比,TLX591-Tx治疗展现了出不同的靶向性和药理学特性。根据对TLX591-Tx治疗患者的长期随访,未观察到明显的急性或迟发性肾毒性;同时,由于其分子量较大,TLX591-Tx在唾液腺和泪腺的摄取也极低,从而减少了口干和眼干的副作用。[1]
此前,本集团于2020年11月与Telix签署了产品战略合作协议,并获得其开发的包括TLX591、TLX591-CDx、TLX250-CDx在内的多款创新RDC产品在大中华区(中国大陆、中国香港特别行政区、中国澳门特别行政区、中国台湾地区)的独家权益。
持续推进创新产品研发,夯实全球核药领军地位
核药抗肿瘤诊疗板块是本集团的重要战略发展方向之一,本集团在该板块已实现了研发、生产、配送、销售等多个环节的全方位布局,板块全球员工超过900人,以波士顿、成都为核心的研发基地,波士顿、法兰克福、新加坡、成都所在的生产基地以及覆盖全球50多个国家和地区的销售网络为基础,本集团已实现了全球化的核药产业链布局。
本集团位于中国四川省成都市温江区的远大医药放射性药物研发及生产基地已于2025年正式投入运营。该基地为全球首个核药全产业链闭环平台,覆盖“同位素制备-核药研发-生产临床-商业化”全链条,形成从早期研发到临床转化到上市销售的全生命周期管理能力,并解决了核药“卡脖子”难题,100%自主生产破解进口依赖困局,为本集团放射性药物的国产化落地奠定坚实的基础。

围绕肿瘤诊疗一体化的治疗理念,目前本集团在研发注册阶段已储备16款创新产品,涵盖68Ga、177Lu、131I、90Y、89Zr在内的5种放射性核素,覆盖了肝癌、前列腺癌、脑癌等在内的7个癌种;早期研发阶段以RDC药物为主,产品储备10余款。在产品种类方面,涵盖诊断和治疗两类核素药物,为患者提供多适应症治疗选择、多手段且诊疗一体化的全球领先的抗肿瘤方案。[3]

板块内创新产品全球研发工作顺利推进。中国方面,易甘泰®钇[90Y]微球注射液于2025年5月获得国家药监局批准开展治疗不可切除HCC的II期注册性临床试验;全球创新温度敏感性栓塞剂GPN00289于2025年10月完成了注册性临床研究的全部患者入组。海外注册方面,SIR-Spheres®钇[90Y]微球注射液(易甘泰®)于2025年7月在美国提前正式获批新适应证,用于治疗不可切除HCC,标志着SIR-Spheres®钇[90Y]微球注射液成为全球首个且唯一获FDA批准用于不可切除HCC和结直肠癌肝转移双重适应症的选择性内放射治疗产品;并于2025年9月获欧洲CE标志认证新增多种肝癌适应症;此外,本集团正携手中外专家合作开发钇[90Y]微球注射液的其他适应症,并将采用“中美双报”的国际化注册路径,加速该产品的全球市场拓展。
目前,本集团在核药抗肿瘤诊疗板块已有六款创新RDC获批开展注册性临床研究,其中四款已进入III期临床阶段,本集团是进入中国III期临床研究中诊断和治疗类RDC创新药总计储备最多的企业,也是全球范围内在核药抗肿瘤领域拥有最丰富产品管线和诊疗一体化布局的创新药企之一。
在核药领域持续发力的同时,本集团亦积极推进多个业务板块协同创新发展,2026年,本集团多款重磅创新产品有望相继上市并实现商业化拓展,多个板块同步发力,产品梯队持续丰富完善,持续巩固本集团全球化创新布局。其中,全球首创干眼症治疗创新产品酒石酸伐尼克兰鼻喷雾剂、治疗过敏性鼻炎的复方鼻喷剂莱特灵®、治疗I型过敏反应的肾上腺素鼻喷雾剂优敏速®,以及全球唯一用于治疗蠕形螨睑缘炎的洛替拉纳滴眼液等创新产品将陆续推向市场。上述产品将进一步夯实本集团优势领域的管线布局,突破性填补临床空白、破解未被满足的治疗需求,助力本集团开辟全新黄金赛道、抢占广阔蓝海增量市场,为长远高质量发展注入强劲持久的核心增长动力。
研发创新及国际化布局方面,本集团有望在2026年落地多项标志性里程碑,持续体现全球创新研发能力与全球化临床推进实力。本集团核心重磅脓毒症全球创新药STC3141研发进展亮眼,该产品已于2025年成功达到中国II期临床研究预设终点,目前正积极与FDA等国际权威监管机构沟通优化临床方案,全面推进国际多中心III期临床试验的前期筹备工作,未来有望为全球近5000万脓毒症患者提供突破性的治疗方案;本集团用于前列腺癌诊断的放射性核素偶联药物TLX591-CDx已完成新药上市申请(NDA)提交,有望于2026年正式获批上市;本集团自主研发的全球创新FAP靶点放射性核素偶联药物GPN01530针对实体瘤诊断的美国I/II期临床研究预计于年内全面开展,该产品是本集团首款获得FDA批准开展临床研究的自研RDC产品,其临床研究的成功获批为本集团核药产品管线的国际化开发提供了重要范式;此外,全球创新、基于放射性核素-抗体偶联技术的靶向磷脂酰肌醇蛋白聚糖3 (GPC-3)的肝细胞癌诊断产品GPN02006早前在中国开展的研究者发起的临床研究(IIT临床研究)取得了里程碑式突破,并在2025年北美核医学与分子影像学会(SNMMI)年会斩获口头报告,该产品极具潜力,有望成为全球首个针对GPC-3靶点的肝细胞癌(HCC)诊断类RDC产品,其预计年内向FDA提交临床试验申请(IND),多项全球化创新研发布局稳步落地。[3]
凭借持续突破的前沿技术、全球化协同的临床体系与丰富的核药创新管线布局,本集团核药板块已建立起全球领先的研发技术壁垒与核心竞争优势,引领核药诊疗领域的创新发展浪潮,为本集团长远发展筑牢最坚实的创新根基。未来,本集团将持续加强核药抗肿瘤诊疗板块的研发和建设,丰富和完善产品管线及产业布局,形成以易甘泰®钇[90Y]微球注射液为核心的核药抗肿瘤诊疗产品集群,持续夯实本集团在全球核药抗肿瘤诊疗领域领军企业地位。
远大医药集团有限公司董事会表示:“本集团一直高度重视创新产品和先进技术的研发,以患者需求为核心,以科技创新为驱动,针对尚未满足的临床需求,加大对全球创新产品和先进技术的投入,丰富和完善产品管线及产业布局,采用‘全球化运营布局,双循环经营发展’策略,形成国内国际双循环联动发展并相互促进的新格局,充分发挥本集团的产业优势和研发实力,快速将科技创新产品落地上市,为全球患者提供更先进更多样的治疗方案。”
[1]基于TLX591-Tx临床研究数据;
[2]根据现有公开信息;
[3]研发风险提示:文中提及的在研产品尚未获得上市批准,其安全性和有效性需经完整临床研究及监管审批确认,不构成任何治疗承诺或商业推广。对在研产品上市时间的任何预期仅为基于当前情况进行初步判断的前瞻性表述,具有相当风险和不确定性。
前瞻性声明:
本新闻稿旨在分享本集团业务相关动态及进展,仅供医疗卫生专业人士参阅,非广告用途。本新闻稿信息仅供参考,不作为诊疗依据,如有身体不适请及时就医,本集团不对任何药品和/或适应症作推荐。
本新闻稿中可能会包含某些前瞻性表述。这些表述本质上具有相当风险和不确定性。在使用“预期”、“相信”、“预测”、“期望”、“打算”及其他类似词语进行表述时,凡与本集团有关的,均属于前瞻性表述。本集团并无义务不断地更新这些预测性陈述。
这些前瞻性表述是基于本集团管理层在做出表述时对未来事务的现有看法、假设、期望、估计、预测和理解。这些表述并非对未来发展的保证,会受到风险、不确性及其他因素的影响,有些是超出本集团的控制范围,难以预计。因此,受我们的业务、竞争环境、政治、经济、法律和社会情况的未来变化及发展的影响,实际结果可能会与前瞻性表述所含资料有较大差别。
本集团、本集团董事及雇员代理概不承担(1)更正或更新本网站所载前瞻性表述的任何义务;及(2)若因任何前瞻性表述不能实现或变成不正确而引致的任何责任。