香港大学团队在皮层脑电脑机接口(ECoG-BCI)领域取得重大突破
近日,香港大学机械工程系与香港科技园先进生物医学仪器中心有限公司等联合研究团队,开发出一种由“导丝驱动”展开的高密度ECoG阵列。
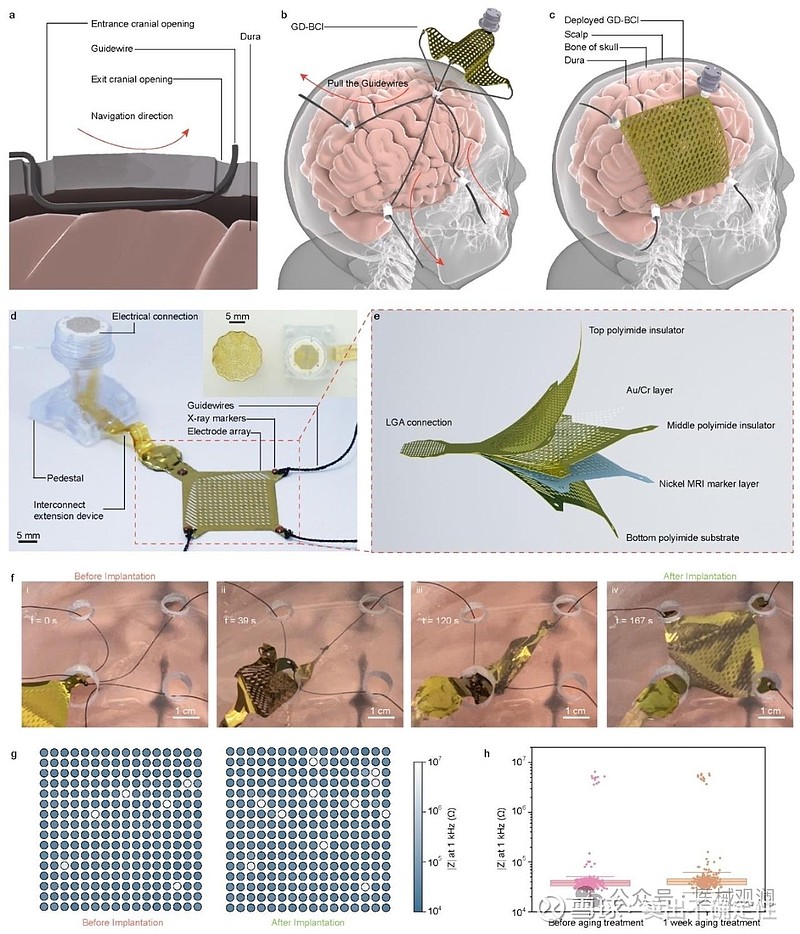
该装置采用超柔性薄膜电极阵列,可在仅毫米级的小孔下折叠植入,并在脑硬膜外自动展开,覆盖面积达4平方厘米,集成256个电极。
这是皮层脑电脑机接口(ECoG-BCI)领域的一项重大突破。该团队研发的“导丝驱动脑机接口(Guidewire-Driven BCI), 简称GD-BCI装置,可通过微创手术进行硬膜外植入,能够以毫米级分辨率捕获和解码大脑运动皮层详细信号,听觉解码准确率≥80%,实现了手术“微创”安全 与产品 “高性能”有效的共振。
同时该装置生物相容性良好,可用于长期监测,部署简便快速,解决了限制当前ECoG-BCI脑机接口领域电极覆盖范围、电极密度与手术安全性之间的核心矛盾,为该领域提供了一条新的技术路径。
ECoG-BCI脑机接口领域现状
ECoG-BCI因信号质量优于头皮脑电图、侵入性低于颅内植入电极,被视为临床应用的“黄金标准”。但传统 ECoG-BCI也存在不少问题。
(1)传统 ECoG-BCI的电极空间分辨率与电极密度不高,无法捕捉精细神经活动。
传统 ECoG-BCI的电极接触面积通常在毫米至厘米级,间距多为 4~10mm,导致电极密度极低(1个电极/平方厘米)。这使得设备难以定位大脑中 “空间离散的毫米级神经 hubs”,进而限制了对复杂脑功能(如语言功能)的解码能力。
(2)手术侵入性高,临床风险与并发症隐患显著
传统 ECoG-BCI 的植入依赖大规模开颅手术:为部署覆盖较大皮层区域,需移除尺寸大于电极阵列的颅骨片段,使大面积脑组织直接暴露于外部环境,这种手术可能引发脑水肿,同时感染风险概率很大,手术恢复周期也长,临床风险显著。
(3)信号质量与稳定性存在矛盾,长期监测能力不足。
传统 ECoG-BCI 在 “信号保真度” 与 “长期使用” 间存在难以调和的矛盾。传统电极阵列在使用过程中阻抗升高与信噪比下降始终存在,同时其材料多为刚性或低柔性基底,无法紧密贴合大脑皮层,导致信号采集时出现 “接触噪声”,信号衰减严重,最后传统装置依赖固定引线连接电极与信号采集单元,当通道数增加时,引线占用空间增加,导致压缩电极密度,增加信号传输的干扰风险。
传统 ECoG-BCI存在的这些问题,正是当前 ECoG-BCI脑机接口领域的重大挑战。
目前,这一困扰该领域的挑战被正式破解。
该研究团队通过一系列的研究攻关,在以下几个方面来对现有问题进行攻克。
首创 “导丝驱动 + 超柔性薄膜” 的微创部署方案,打破传统 BCI 的技术僵局
该团队采用光刻技术打造超柔性薄膜电极阵列(21μm 厚,4cm² 内集成 256 个电极),电极密度达到64个/平方厘米,97.7%的电极在1kHz频率下阻抗≤100kΩ。
在如何让电极更好的贴合大脑这块,研究人员通过在聚酰亚胺基板上设计微小穿孔,这样既能引导脑脊液远离电极位点,又能减少界面摩擦,避免对脆弱脑组织造成损伤。
同时该团队还为装置定制了3D打印基座。通过对患者的颅骨做CT,得到相关数据,做出适合患者颅骨自然曲率的基座。其重量轻且兼容磁共振成像(MRI),完美解决了传统钛合金基座贴合性差、易产生图像干扰的问题。
最终通过超柔性薄膜电极阵列与导丝驱动策略结合,电极折叠后通过4个毫米级颅骨孔拉入硬膜外空间,再借助超柔性导丝精准展开,全程仅需 2 小时且无需移除大块颅骨。
这种设计既避免了复杂手术器械带来的脑损伤风险,又实现了 “高密度 + 大面积” 的信号采集能力。是首个同时满足 “微创植入” 与 “高性能记录” 的 ECoG-BCI 方案,彻底打破了传统技术的核心矛盾。