$Intellia(NTLA)$ Intellia Therapeutics (NTLA) 2025 Q4 财报会议核心纪要
会议时间:2026年2月26日
核心主题:体内基因编辑疗法商业化前夜,HAE项目即将读出关键数据,ATTR项目解除部分临床暂停。
1. 核心业务进展 (Business Highlights)
重点管线:Lonvo-z (遗传性血管性水肿 HAE)
临床进度: III期临床试验 (HAELO) 已于2025年9月完成入组(80例患者),耗时仅9个月,远超预期。 数据读出:预计 2026年年中 公布顶线数据。 监管申报:计划于 2026年下半年 提交生物制品许可申请 (BLA)。 上市预期:若获批,预计 2027年上半年 在美国上市。 市场反馈: 患者意愿:99%的受访患者表示愿意尝试该疗法,近2/3表示“极有可能”。 医生意愿:92%的医生表示会处方该药,预计覆盖其管理患者总数的54%。 未满足需求:现有长期预防疗法(LTP)仍有沉重负担,仅20%患者实现无发作;而Lonvo-z I/II期数据显示76%患者实现无发作且停药。 竞争优势:作为一次性治愈疗法,对比现有需终身注射的高价LTP药物(终身费用数百万美元),具有极高的药物经济学价值。重点管线:Nex-z (转甲状腺素蛋白淀粉样变性 ATTR)
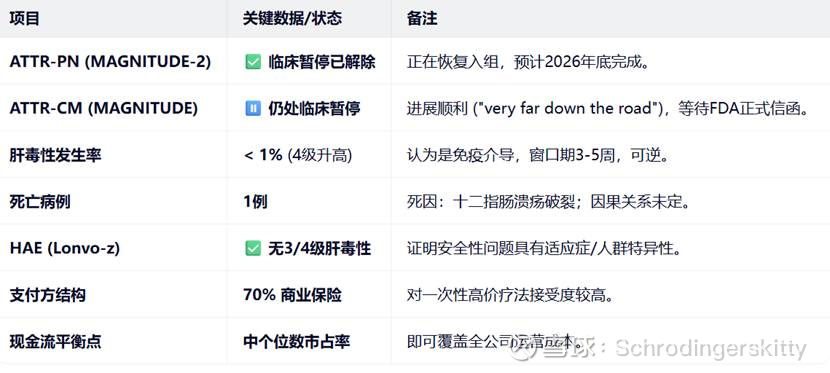
临床暂停事件回顾:2025年10月,因MAGNITUDE研究(心肌病适应症)中出现一例患者肝酶升高并随后死亡(死因为十二指肠溃疡破裂,因果关系未定),试验被FDA暂停。 最新进展: MAGNITUDE-2 (多发性神经病变适应症):FDA已于2026年1月底解除临床暂停。 方案调整:增加给药后几周的补充肝脏检测;若发现肝酶升高,短期使用类固醇干预;排除基线肝酶显著升高或有自身免疫性肝炎病史的患者。 入组计划:目标入组从50人增至60人,预计 2026年下半年 完成入组。 MAGNITUDE (心肌病适应症):仍处于临床暂停状态,但正在与FDA积极沟通。 差异化管理:FDA认为心肌病患者(老年、多药共用、合并症多)与神经病变患者(较年轻、较健康)人群特征不同,因此采取分步解除策略。 安全性数据:整个MAGNITUDE研究中,4级肝酶升高发生率 <1%。公司认为这是免疫介导反应,可通过监测和短期类固醇控制。2. 财务摘要 (Financial Summary)
资金指引:当前现金储备预计可支持公司运营至 2027年下半年,覆盖Lonvo-z上市启动及ATTR项目重启等关键里程碑。 商业化准备:已建立实地医疗团队,正在扩大销售和报销团队,制定定价及分销策略。若Lonvo-z获得个位数中段市场份额,产生的现金流有望完全覆盖公司整体运营成本。
3. 管理层展望与战略 (Management Outlook)
2026年是转折之年:将迎来全球首个体内CRISPR基因编辑疗法的 pivotal 数据读出及潜在上市。 商业化策略: 定位:强调“一次性治疗”带来的终身自由(无发作、无药疗),解决患者对终身用药的恐惧。 支付方沟通:支付方认可现有疗法的高昂成本和未满足需求,对一次性疗法的价值主张反馈积极。 生产准备 (CMC):III期临床所用材料即为商业化规模材料,无需额外的可比性研究,生产网络(CDMO)已验证并准备就绪。 安全性应对: 针对ATTR项目的肝酶升高,确认为免疫介导反应,主要发生在给药后3-5周内。 通过早期监测 + 短期类固醇干预可有效管理,预计长期使用类固醇的患者比例极低(个位数百分比)。 该安全性信号目前被视为ATTR心肌病人群特有(因患者年龄大、基础病多),在HAE及其他管线中未观察到类似现象。4. 问答环节精华 (Q&A Highlights)
关于HAE III期数据预期: 现有LTP药物的最佳攻击减少率在80%左右,无发作率约60%。管理层预期Lonvo-z在安慰剂对照试验中将极具竞争力,且在真实世界(非盲态)中表现可能更好(参考I/II期 pooled 数据)。 美国患者入组并未导致人群特征偏差,具有代表性。 关于ATTR临床暂停解除差异: FDA区分对待是因为患者人群差异巨大。神经病变患者更年轻、更健康;心肌病患者多为老年人,合并多种疾病和用药,风险因素更复杂。 MAGNITUDE(心肌病)的解除仍需等待更多数据审查和方案细化,但进展顺利。 关于竞争格局 (vs. RNAi疗法): 强调“护理负担”差异。RNAi疗法需每3-6个月注射一次,且每次都需要繁琐的预先授权(Prior Authorization),对患者生活造成长期约束。 Lonvo-z作为一次性疗法,彻底消除了这种长期的行政和生理负担,这是巨大的差异化优势。 关于生产成本与定价: 虽未透露具体定价,但强调相对于现有疗法数百万美元的终身费用,一次性疗法具有显著的成本节约潜力。 生产流程已商业化验证,具备大规模供应能力。商业化前景与资金自给能力 (CEO John Leonard & CFO Ed Dulac)
定价逻辑:
目前谈论具体定价为时过早,但参照现有HAE长期预防疗法(LTP),患者终身治疗费用高达数百万美元。
Lonvo-z作为一次性疗法,有望为患者和支付方节省巨额开支,同时消除终身用药的社会、情感及生活质量负担,并减少医生处理繁琐“预先授权”的工作量。
资金转折点:
美国约有 7,000名 接受治疗的HAE患者。
若Lonvo-z获批并获得中个位数(mid-single-digit)的市场份额,其产生的现金流预计将完全覆盖公司整体运营成本。这意味着公司可能不再需要依赖股权融资,实现自我造血。
现金储备:
截至2025年底,现金及等价物为 6.051亿美元。
足以支持运营至 2027年下半年,覆盖ATTR项目重启、HAE项目上市等所有关键里程碑。
📉 财务数据回顾 (CFO Ed Dulac)
营收:Q4合作收入 2,300万美元(同比+78%),主要源于SparingVision协议终止确认收入及Regeneron成本报销增加。
研发费用 (R&D):Q4支出 8,870万美元(同比-24%),主要因员工相关费用、股权激励及外包服务减少,部分被Lonvo-z临床费用增加抵消。
净亏损:Q4净亏损 9,580万美元(去年同期为1.289亿美元),亏损显著收窄。
2. 问答环节精华 (Q&A Highlights)
关于HAE III期试验的美国患者差异 (Jefferies)
问题:I/II期数据主要来自美国以外,而III期包含美国患者。基线特征(如BMI、背景用药)是否有差异?如何看安慰剂组表现?
回答 (John Leonard):
III期人群与II期高度重叠,具有代表性,未出现特定人口学偏差。
美国患者入组意愿极强:需停药洗脱、建立基线发作率、再进入双盲安慰剂期,患者仍愿意参与,证明了极高的未满足需求。
结论:II期数据在美国人群中具有可重复性。
❓ 关于HAE目标患者群与ATTR临床暂停进展 (Leerink)
问题1 (HAE策略):哪类患者最可能接受基因编辑疗法(年轻vs重症)?
回答 (Ed Dulac):
患者不关心技术原理(基因编辑vs其他),只关心疗效和结果。
Lonvo-z是唯一能提供“无发作 + 无药疗”双重自由的疗法,这是核心卖点。
策略重点:教育医生、建立基础设施、扩大实地医疗团队和报销团队。
问题2 (ATTR进展):临床暂停解除的时间表?对死亡病例的理解是否有更新?
回答 (John Leonard):
MAGNITUDE-2 (神经病变):正在恢复入组,预计年底完成。
MAGNITUDE (心肌病):仍在暂停中,但与FDA沟通进展顺利("very far down that road")。
死亡病例复盘:该患者病程复杂,虽出现4级肝酶升高,但死因为十二指肠溃疡破裂。腹痛症状在纯肝酶升高病例中不典型,因果关系未定。这是一个离群值 (outlier)。
应对措施:通过加强监测和短期类固醇干预,确保受试者安全。
❓ 关于ATTR神经病变研究的 interim analysis (BofA)
问题:重启后是否可能进行中期分析?如何看待9个月终点?
回答 (John Leonard):
目前计划是18个月读出数据,暂无中期分析计划,但不排除未来根据数据表现调整。
I/II期长期随访显示:深度降低TTR的患者病情基本停止进展,甚至部分曾在使用Patisiran期间进展的患者出现了改善。这支撑了较小样本量(50-60人)的设计合理性。
❓ 关于CMC准备与全球监管对齐 (TD Cowen)
问题:Lonvo-z的CMC准备情况?II期到III期是否有工艺变更?非美监管机构是否认可?
回答 (John Leonard & Ed Dulac):
CMC状态:完全准备就绪。
工艺一致性:III期(HAELO)使用的材料即为商业化规模材料,无需额外的可比性研究或更换生产场地。
供应链:已建立成熟的CDMO网络(主要在欧洲),工艺已验证,具备大规模供应能力。
❓ 关于支付方态度与疗效门槛 (RBC)
问题:支付方对疗效的门槛是什么?是否有阻力?
回答 (Ed Dulac):
支付方反馈非常积极,认可现有疗法的高昂成本和未满足需求。
疗效门槛:现有最佳疗法的发作减少率约80%,无发作率约60%。Lonvo-z预期将在这些指标上极具竞争力。
价值主张:考虑到患者年轻、需数十年高价治疗,一次性疗法对支付方也是双赢。
❓ 关于肝毒性机制与长期风险 (Evercore ISI)
问题:若是免疫介导反应,患者是否会长期易感?能否提前筛查?
回答 (John Leonard):
机制确认:高度符合免疫介导反应特征,典型发生窗口为给药后 3-5周。
长期风险:数据未显示长期易感性。此后未见类似反应。
筛查难点:目前无法提前预测哪些患者会反应,因此策略是严密监测 + 快速干预(短期类固醇)。
预后:除死亡个案外,其他出现肝酶升高的患者均快速恢复,多数甚至无需治疗。预计仅需个位数百分比的患者需要使用类固醇。
❓ 为什么FDA解除神经病变(PN)暂停却保留心肌病(CM)暂停?(Wolfe Research)
问题:同一款药、同一个基因编辑,为何FDA对两个适应症态度不同? 回答 (CEO John Leonard): 人群特征差异巨大: PN患者:通常较年轻(早发型),健康状况相对较好,合并症少。 CM患者:通常是老年病(野生型ATTR多发于70岁以上),伴有多重用药 (Polypharmacy) 和其他基础疾病(如心脏病、糖尿病等)。 安全性数据背景:PN研究至今安全性记录良好;而CM研究数据量大且复杂,需更仔细审查。 结论:FDA认为风险主要集中于脆弱的老年CM人群,因此采取分步解除策略。❓ 死亡病例复盘与新缓解策略的有效性 (Goldman Sachs & Wells Fargo)
问题1:除了死亡病例,还有多少例4级肝酶升高?新策略能防止此类事件吗? 回答:整个MAGNITUDE研究中,4级肝酶升高发生率 <1%。 关于死亡病例:死因为十二指肠溃疡破裂,因果关系未定。若在新策略下,虽然无法完全排除溃疡风险,但肝酶升高会被更早发现,从而更早启动类固醇治疗,避免发展到严重程度。 问题2:具体的监测频率是多少? 回答:在给药后风险窗口期(3-5周),进行每周甚至半周两次的密集肝功能检测,确保“早发现、早干预”。❓ 竞争格局:一次性基因编辑 vs. 半年一次RNAi (Citizens JMP)
问题:如何定位“一次性疗法”相对于“每6个月注射一次”的RNAi疗法(如Argo Biopharma等新进入者)的优势? 回答 (CEO & CFO): 护理负担 (Burden of Care) 是核心差异: 不仅仅是注射频率,还包括每次给药前的预先授权 (Prior Authorization) 繁琐流程、保险中断风险、对患者职业选择的限制(不敢换工作怕失保)。 患者(尤其是年轻患者)极度渴望彻底摆脱药物依赖和行政负担。 数据解读提醒:早期开放标签研究(Open-label)的数据往往优于随机双盲安慰剂对照试验(因患者知晓自己用药,报告发作率更低)。Intellia的III期数据将更严谨,但真实世界表现预计会非常强劲。❓ 肝毒性是否具有管线特异性?(William Blair)
问题:ATTR项目的肝酶升高是否源于TTR基因编辑本身?会影响其他管线(如HAE)吗? 回答 (CEO John Leonard): 无跨管线风险:HAE项目(Lonvo-z)的I/II/III期研究中,从未观察到任何3级或4级肝酶升高。 原因推测:这可能与特定基因 (TTR)、特定编辑方式以及特定患者人群 (老年、多病) 有关,而非CRISPR平台本身的系统性缺陷。 机制判断:目前迹象高度指向免疫介导反应,可通过短期类固醇控制,且无长期易感性证据。❓ 财务自给模型详解 (Morgan Stanley)
问题:“中个位数市占率即可覆盖全部运营成本”的假设基础是什么?费用会如何变化? 回答 (CFO Ed Dulac): 费用端:公司已完成重组,研发费用聚焦,未来主要是商业化团队扩建。预计未来12-24个月净现金消耗维持在 4亿美元/年 左右,不会大幅激增。 收入端:HAE市场约7,000人,其中 70%为商业保险。鉴于现有疗法终身费用高达数百万美元,一次性疗法即使定价较高也能显著节约支付方成本。 结论:只需获得少量市场份额(mid-single-digit),产生的高额毛利即可覆盖公司整体运营,实现自我造血,无需再融资。❓ 方案修订对数据一致性的影响 (Baird)
问题:PN研究中途暂停并修改方案,是否会导致前后数据不可比? 回答 (CEO John Leonard): 影响微乎其微 (De minimis): 暂停时间很短(仅3个月)。 入组已接近完成(目标50人,已达47人),新增的10人主要是为了容纳暂停期间筛选的患者。 患者人群特征和外部治疗环境未发生显著变化。 结论:数据集仍具有高度一致性和可比性。2. 关键数据与事实核对 (Key Facts Check)