GRAIL 季度财报更新,下半年将引来重要数据更新
近日,$Grail(GRAL)$ 公布2025年第二季度财报,二季度里程碑亮点之前已经陆续披露,唯一的亮点是在没有FDA批准的情况下,泛癌种早筛产品Galleri已经累积售出超过37万份,实在是令人惊讶的数据,也侧面说明了早筛市场广阔的前进。
2025年第二季度亮点和里程碑更新:
Grail 第二季度总收入为3550万美元,比2024年第二季度增长11%。收入几乎都来自其泛癌种筛查产品Galleri,美国Galleri收入为3420万美元,同比增长21%,共计超过45,000份Galleri检测,截至2025年6月30日,累计售出超过370,000份Galleri商业检测。重复检测量持续增长,目前超过25%的Galleri检测量是重复检测。Galleri已整合到Quest Diagnostics检测订购平台,推动了检测量的增长。第二季度约有7%的订单通过Quest平台获得。我们也看到合作伙伴包括了$英伟达(NVDA)$ ,未来AI的应用将如何加速早筛产品的塑造呢
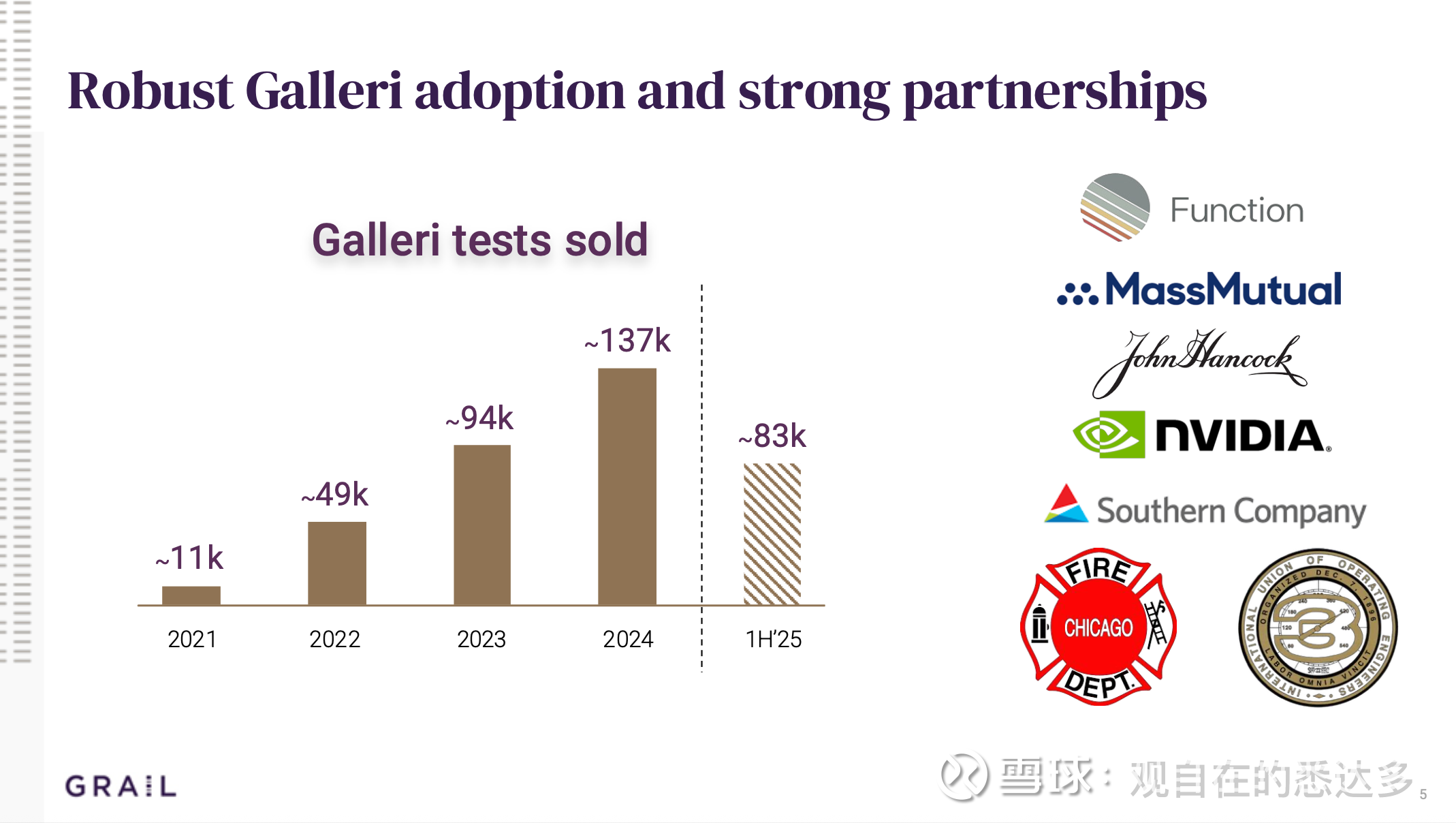
第二季度净亏损为1.14亿美元,较2024年第二季度显著改善93%。截至2025年6月30日,现金余额为6.061亿美元。将2025年全年现金消耗指引更新为不超过3.1亿美元(此前为3.2亿美元),这比2024年减少了40%以上。公司预计现金流可持续到2028年。
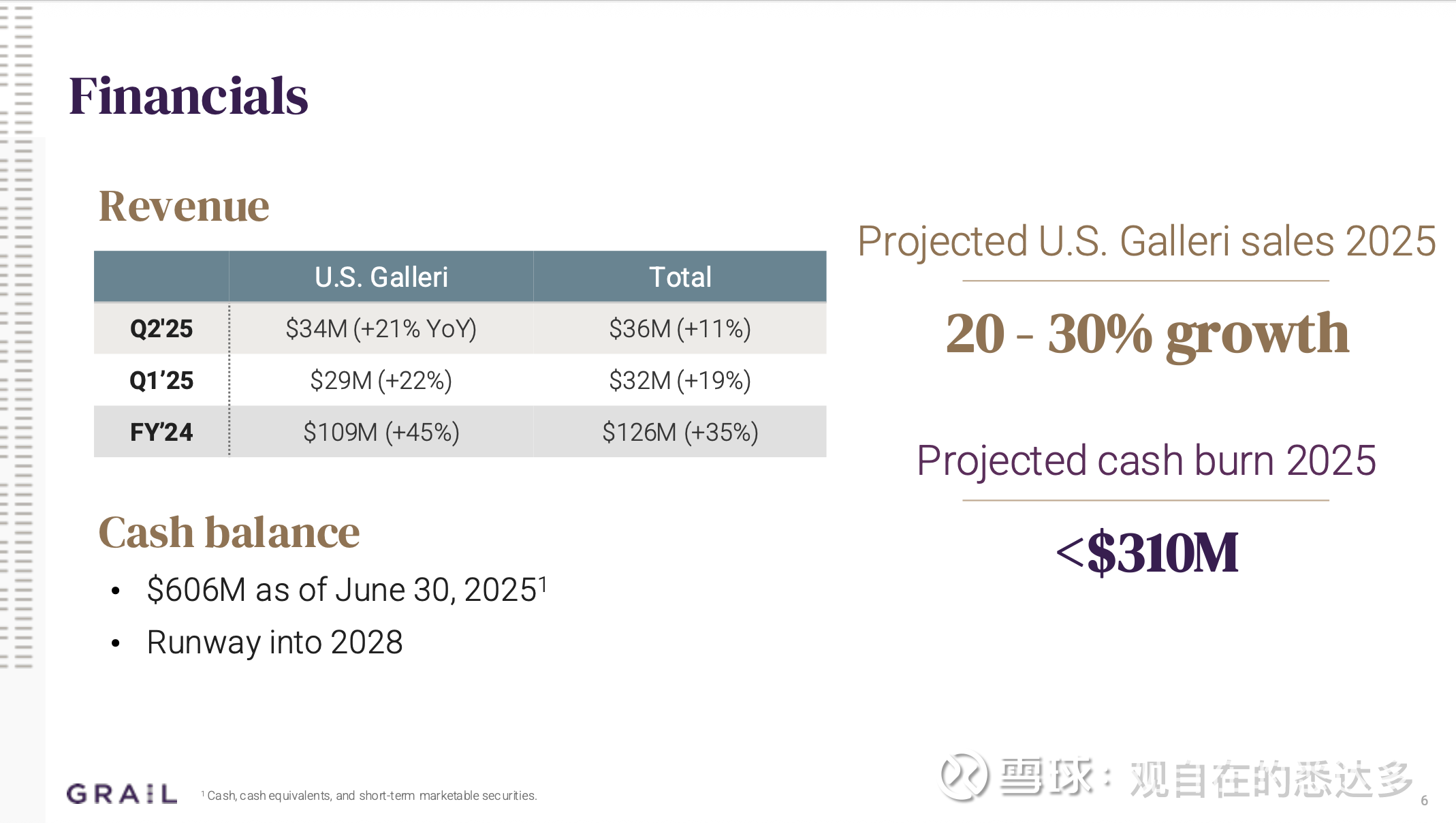
目前有两个重要的临床研究,NHS-Galleri研究和PATHFINDER 2研究的积极结果已经在今年上半年公布,两项研究都是希望评估Galleri检测的临床效用,有不同的目的,我们这里做个简单比较:
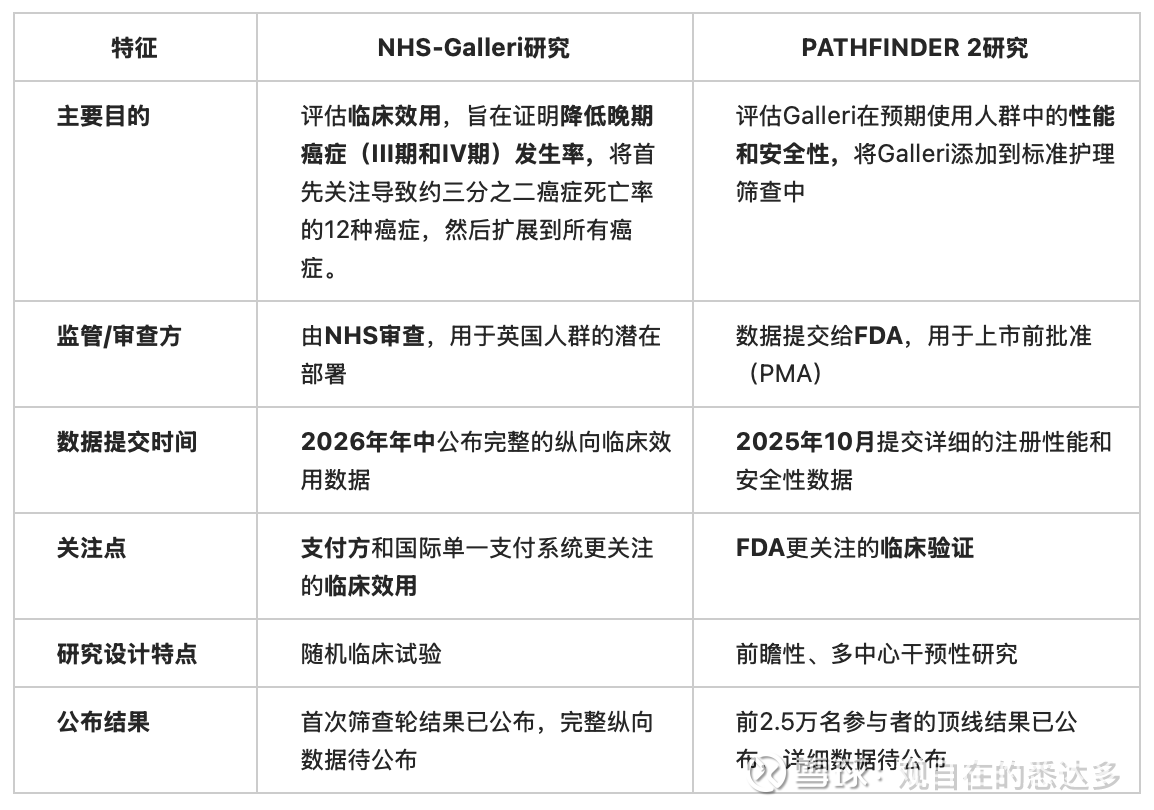
简而言之,PATHFINDER 2研究的重点在于为Galleri获取FDA批准,证明其在检测性能和安全性方面的临床验证。而NHS-Galleri研究的重点则是提供Galleri在降低晚期癌症发生率方面的临床效用数据,以支持其在英国的部署,并作为全球其他支付方获得报销的关键证据。
未来Grail 最主要的两个重要里程碑是FDA的批准和纳入商业保险
Galleri产品获得FDA最关键的条件是,任何检测开发商都必须在针对无症状成年人(即预期使用人群)的临床实践中确认临床验证,才能将其检测引入临床实践中。GRAIL计划在2025年10月向ESMO大会提交PATHFINDER 2注册研究的详细性能和安全性数据,该数据集将提交给FDA。这些数据表明,与首次PATHFINDER研究相比,PATHFINDER 2在加入标准护理筛查时显示出显著更高的额外癌症检出率和显著更高的阳性预测值(PPV),同时特异性和CSO(癌症信号来源)准确性保持一致,且没有报告严重安全问题。FDA将重点关注临床验证而非临床效用。他们将审查检测的益处与潜在危害。由于Galleri预计是首个通过FDA审批的多癌早期检测(MCED)产品,GRAIL预计审批过程将需要大约一年时间,可能在2027年上半年完成,这可能包括召开一个咨询委员会会议。

GRAIL希望争取CMS(医疗保险和医疗补助服务中心)的覆盖以及广泛的商业报销。与FDA的关注点不同,支付方(包括商业保险公司)将更关注临床效用数据。公司预计在2026年年中获得14万名参与者的NHS-Galleri研究的完整纵向临床效用数据。这些数据将由NHS审查,以确定Galleri在英国人群中的潜在部署。GRAIL认为,这项研究的成功结果将是与全球许多国家进行重要讨论的“绝佳名片”,因为它规模庞大、严谨,且NHS享有盛誉,这些数据将被视为“强有力的证据包”,可用于其他国际单一支付系统机会。
关于竞争
GRAIL无疑是MCED的领先者,但这并不意味着没有人在做同样的事情,那么Grail的竞争格局是怎样的呢?
首先,GRAIL其在多癌早期检测领域树立了高证据门槛,通过多年的临床研究和随访数据,但是NHS的队列就有14万人,这样的规模暂时还没有其他公司可以做出,此外,Galleri在真实世界的商业应用中已经完成370,000份,依旧表现出色。这些对于后来者是一个很难超越的证据门槛。
其次,GRAIL拥有关键性能指标优势,GRAIL 认为 PPV 是MCED测试最临床重要的性能指标之一。它衡量的是在所有检测结果呈阳性的案例中,有多少是真正的癌症病例,即“在阳性检测结果中,有多少癌症被发现,或者有多少是真正的阳性”。GRAIL 认为,高 PPV 对于 MCED 检测至关重要,因为它可以指导高效且有效的临床检查。他们不认为依赖全身影像检查等其他方法是可行的,因为这涉及辐射暴露、成本高昂且缺乏性能或安全性数据。Galleri的PPV显著高于领先的单癌筛查检测(其PPV通常为个位数)。与其他单癌筛查的比较,Galleri 的 PPV 显著高于领先的单癌筛查检测。在 PATHFINDER 研究中,Galleri 的 PPV 为43%。相比之下,领先的单癌筛查检测的 PPV 通常在个位数。这表明 Galleri 在避免假阳性方面表现出色,从而减少不必要的后续检查和患者焦虑。
Galleri的特异性高达99.5%,这意味着其假阳性率极低,仅为0.5%。GRAIL指出,如果其他检测开发商的特异性较低(例如98.5%),则假阳性率将高出三倍。
GRAIL认为,任何MCED检测都必须报告预测的癌症信号来源(CSO),以指导高效的临床检查。Galleri的CSO准确性在首次PATHFINDER研究中达到88%,并在后续研究中保持一致。
GRAIL强调,其检测在预期使用人群的临床验证中表现出色,关键性能指标(特异性、PPV或癌症检出率)没有出现下降。这与其他一些在观察性病例对照研究中表现良好,但在真实世界中未能确认结果的检测形成对比。
下半年及未来的关键催化剂:

2025年下半年:
计划于10月向ESMO 2025大会提交PATHFINDER 2研究的详细注册性能和安全性数据,以供展示。这些数据将被提交给FDA。
计划于11月举办2025年分析师日。
2026年及以后:
预计在2026年上半年完成PMA(上市前批准)的模块化提交。公司预计FDA批准过程(对于首个MCED)约为一年,可能在2027年上半年完成。
预计在2026年中期获得NHS-Galleri研究的完整纵向临床效用数据。这些数据将由NHS审查,以确定Galleri在英国人群中的潜在部署。
楼主持续追踪美股小而美的生物科技及大型生命科学,ivd诊断类公司,包括早筛,MRD,AI医疗等方向,希望大家多多关注,一起讨论交流。