德琪200亿之路,AnTenGager平台及其核心管线「ATG-201」
前言:德琪TCE平台「AnTenGager™」具有空间位阻遮蔽、CD3自主设计、DAA二价结合等亮点,相比竞对优势突出,极有可能是下一代TCE技术的领跑者。「ATG-201」基于「AnTenGager™」开发,已在动物实验中取得远超同润生物「CN201」的数据,是潜在的BIC。参考同润与默沙东的BD案例,「ATG-201」有望斩获首付款超7亿美元的deal。
一、AnTenGager™平台
TCE是一种双特异性抗体,拥有两种不同的抗原结合域,一种靶向致病细胞表面特异性抗原(TAA,e.g. BCMA、CD19等),另一种靶向T细胞表面受体(e.g. CD3)。不同于传统抗体,TCE无需依赖抗原呈递细胞或MHC分子,能够直接桥接T细胞和致病细胞,形成免疫突触并激活T细胞免疫杀伤功能,在实体瘤、血液瘤、自免疾病领域具有治疗潜力。
第一代TCE平台通常为1+1型,即具有1个TAA结合臂和1个CD3结合臂。Amgen的blinatumomab(CD19×CD3)是1+1型代表药物,其两个片段通过柔性linker连接,分子量仅55kDa,能够高效介导T细胞与靶细胞结合,被应用于r/r B-ALL治疗。
但是,第一代TCE平台存在诸多不足之处,一方面,其仅有一个TAA结合臂,一价结合亲和力不足以实现对于低表达靶点的靶向作用;另一方面,其CD3缺乏遮蔽,存在脱靶效应(攻击正常细胞)和CRS风险(T细胞过快激活)。
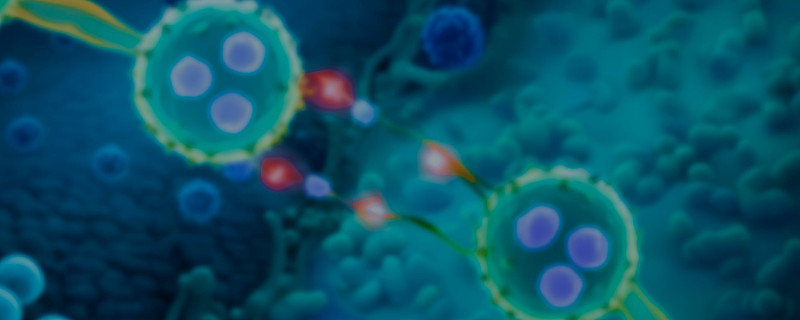
第二代TCE平台通常为2+1型,即具有2个TAA结合臂和1个CD3结合臂。德琪「AnTenGager™」平台基于2+1结构构建,采用空间位阻遮蔽技术,相比上代平台具有更高的安全性和更强的疗效。
「AnTenGager™」的优势具体表现为:
1. 与DAA二价结合,大幅提升亲和力,使靶向低表达靶点成为可能。
2. 利用空间位阻效应实现CD3遮蔽和靶点依赖活性,最大限度减少脱靶因子释放,可应用于肿瘤及自免疾病。
3. CD3自主设计,通过与独特构象表位结合(CD3εγ或CD3εσ复合体),具有快上快下的结合动力学,最大程度减少在靶因子释放,并保持强大的T细胞激活作用。
4. 半衰期更长,小鼠体内半衰期为100-300小时。
与其他2+1平台对比,「AnTenGager™」的条件激活逻辑精准、适应症范围广阔、安全性更佳。Roche(Prot-TCB)、Janux(TRACTr)、Xilio的CD3遮蔽需要酶切暴露,依赖肿瘤微环境,只能应用于癌症领域;Xencor(XmAb)、Zymeworks(Azymetric)、信达(Innobody)、维立志博(Leadsbody)的CD3表位保守,使用的是已过专利期的sp34衍生序列,通过下调亲和力降低CRS的策略可能会牺牲T细胞激活强度。
基于「AnTenGager™」,德琪开发了10条TCE管线,聚焦实体瘤、血液瘤、自免疾病的治疗,包括2条未披露靶点的三抗,其中「ATG-201」研发进度最为领先。

二、ATG-201
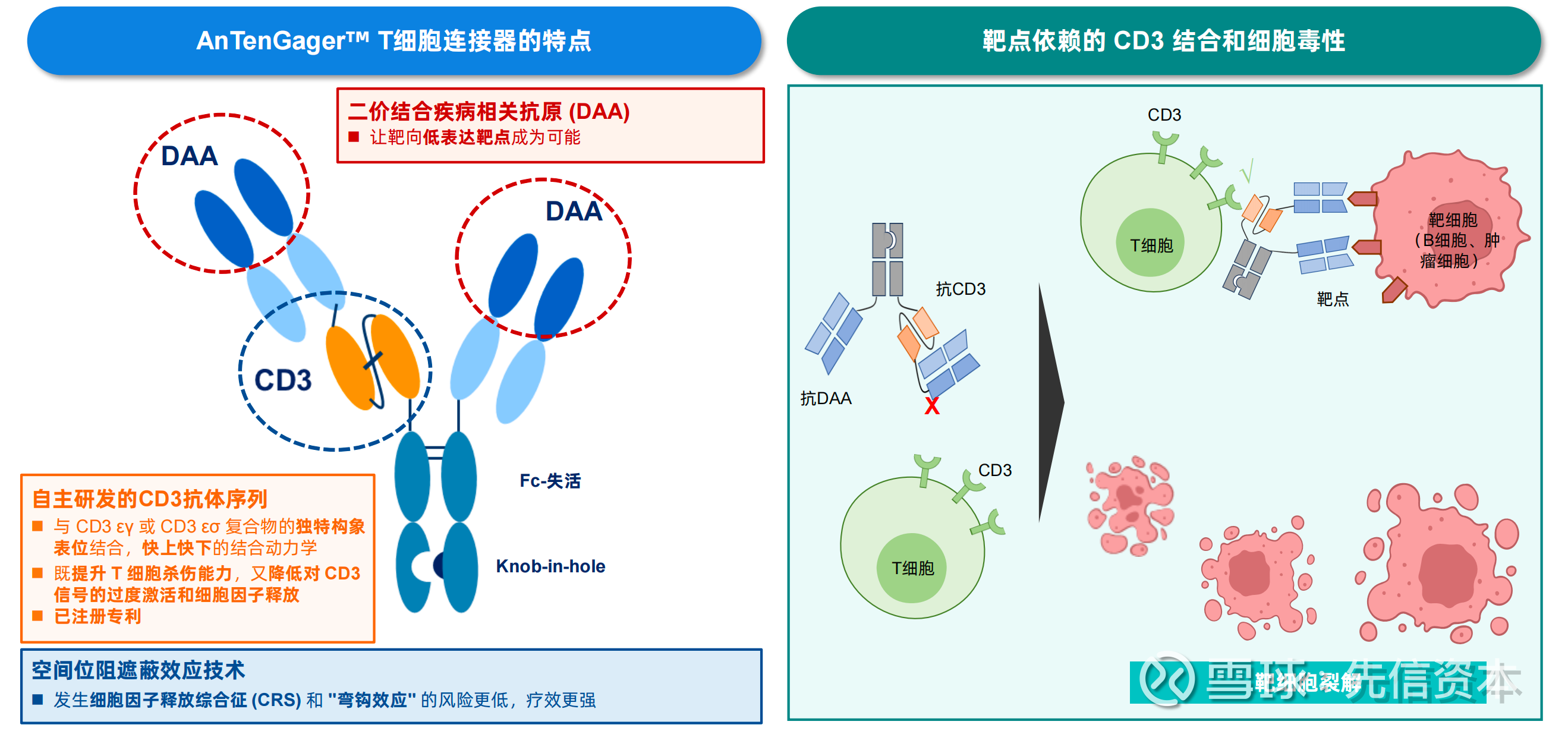
「ATG-201」是靶向CD19和CD3的双抗TCE,用于治疗B细胞相关自免疾病,当前IND支持性研究和CMC工作进展顺利,计划25年底递交IND。
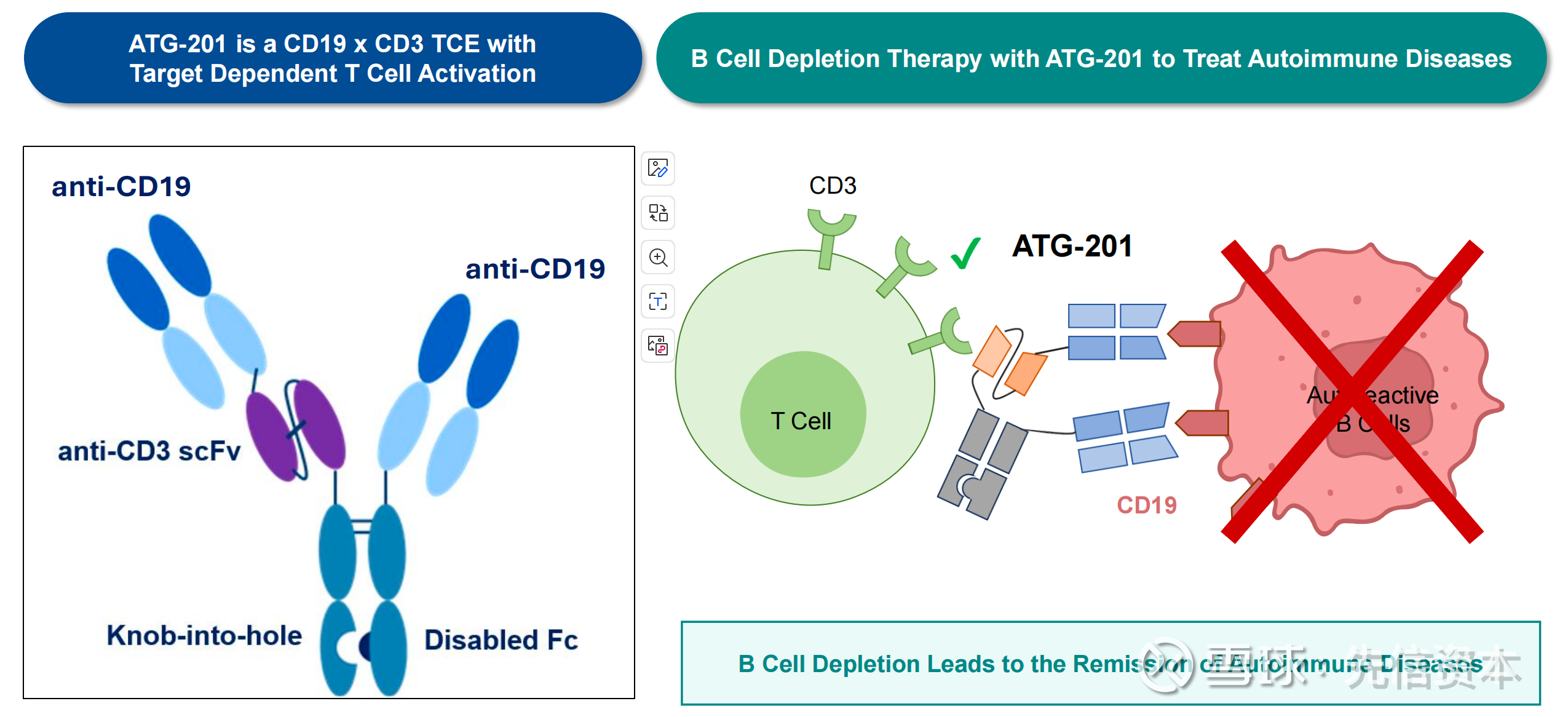
在CD34+细胞人源化小鼠模型中,单次给药后分别在第3/5/7/14天采集样本,「ATG-201」显示较「CN201」具有更深且更持久的体内B细胞清除:
1. ATG-201:单次给药彻底且深度的清除了小鼠体内的B细胞,治疗后第14天在血液、骨髓和脾脏中均未检测到B细胞。
2. CN201(Benchmark4):骨髓中的B细胞被清除;血液和脾脏中的B细胞在第3天被清除,但第5天开始反弹。
3. 细胞因子释放:「ATG-201」较「CN201」诱导释放了明显更少的IL-6和TNF-α。
「ATG-201」的脾脏数据尤为突出,通常大型器官中B细胞完全清除难度非常大。
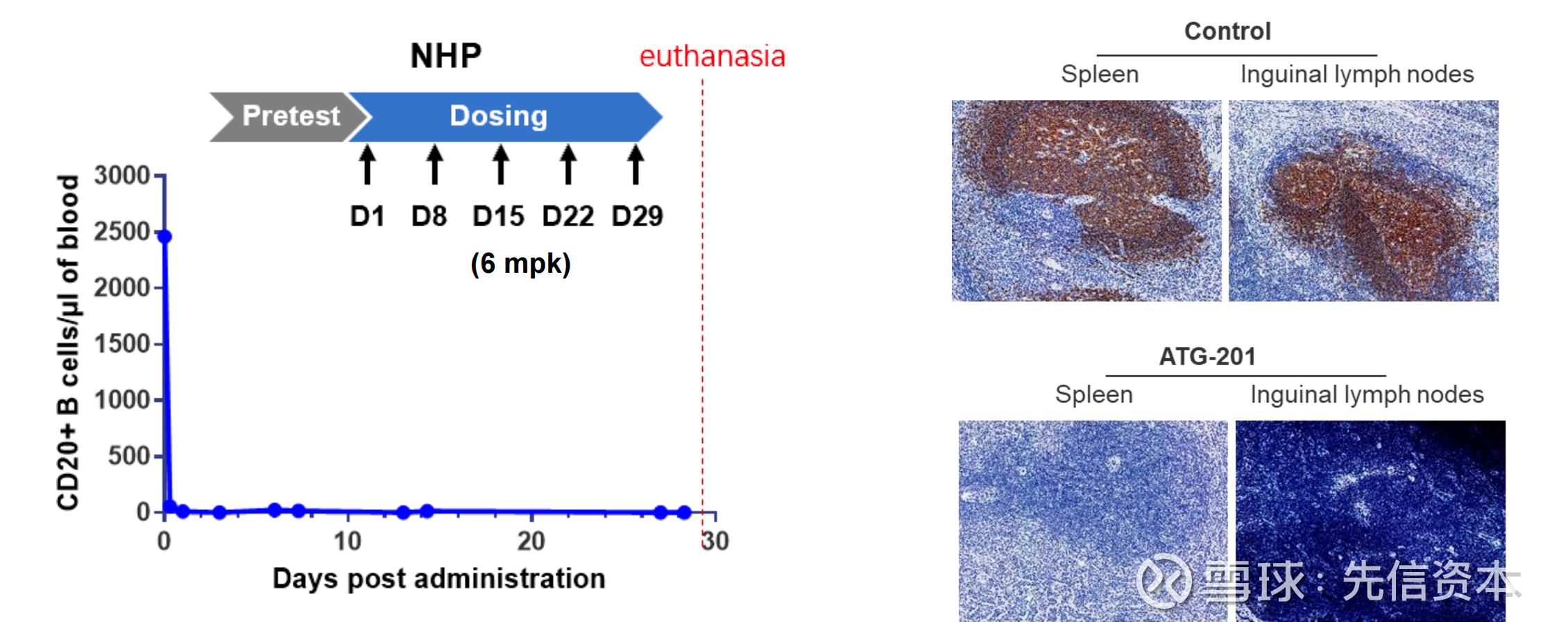
在非人灵长动物重复给药实验中,「ATG-201」分别以1mpk/3mpk/6mpk剂量水平给药,NHP均显示了非常好的耐受性和安全性,引发CRS极低,同时带来深度且持久的B细胞清除。
「CN201」由同润生物开发,当前处于临床I期和Ib/II期阶段。默沙东已于24年8月收购「CN201」全球独家权利,对价为13亿美元(首付款高达7亿美元)。「ATG-201」的小鼠数据远超「CN201」,是潜在的BIC,26年进入临床+读出数据后,有望斩获更大的BD合同,预计全球权益转让首付款超7亿美金,整体deal规模超20亿美金。
***以上观点仅供参考,不构成任何投资建议或买卖要约。投资者据此操作,风险自担。本人及本人所在投资机构可能持有所述公司的股票、认股证、期权,或第三方所发行与所述公司有关的衍生金融工具等,且持仓情况随时可能发生变动。