【面向未来的迈威看点五:结直肠癌的潜在明星】
突破性进展的苗头,吹响了结直肠癌ADC的进攻号角,国内创新药在该领域布局广泛且充分,非常卷了已经。
CDH17作为结直肠癌的高潜泛靶点,目前尚无产品上市(蓝海),多数处于I/II期,2026年是关键数据读出期。CDH17 虽是消化道靶点,但其特异性比 EpCAM 更高(在正常组织中的表达更局促)。
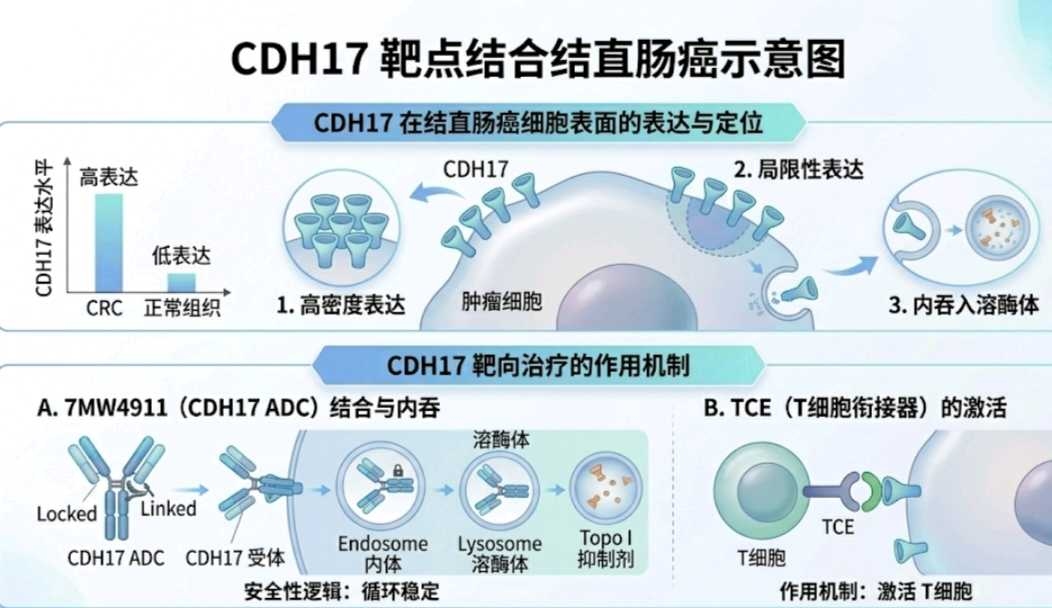
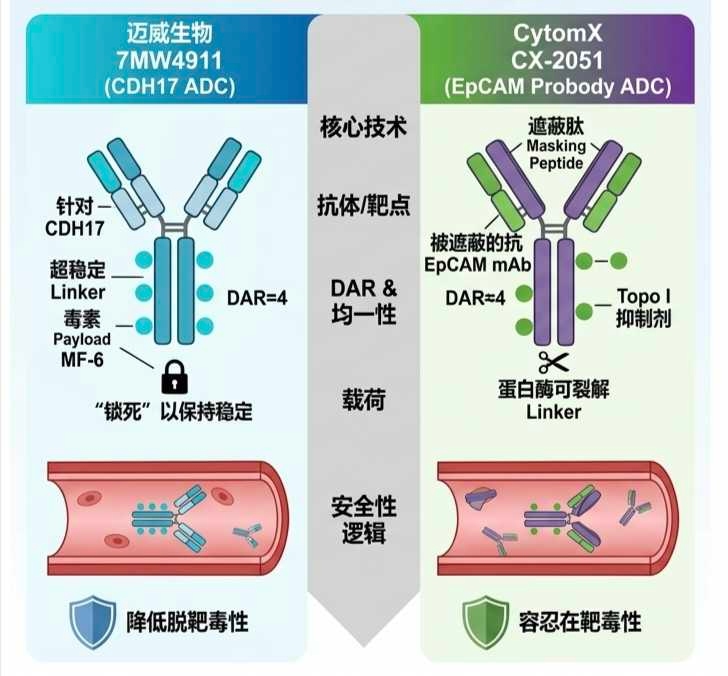
迈威生物的4911临床前数据验证出色。跟CytomX“蒙眼”制导炸弹不同的是,4911依赖的是“更坚固的锁扣”,都可以实现精准杀伤、降低毒性的目标。归根结底,这是个工程学问题,国内的强项,迈威已多次验证有效性,预计年内可以读出数据。
这里需要了解两个问题。
第一个问题,为何CX-2051会引起轰动?
那是因为在 ADC 领域,10mg/kg 是一个非常具有挑战性的剂量门槛。通常情况下,像 Enhertu(DS-8201)这类主流 ADC 的剂量多在 5.4–6.4 mg/kg 之间。
而CX-2051可以10mg/kg 下实现10%的三级腹泻,说明遮蔽能力一流,也基本走通了路径,这一点非常爆炸!
第二个问题,迈威4911临床如何设计的?
基于公开的临床试验登记信息(NCT07216560)以及迈威披露的临床前数据,7MW4911 的剂量设计极具侵略性:
1、起始剂量与爬坡:虽然起始剂量通常较低,但迈威在食蟹猴实验中测得的最高非严重毒性剂量(HNSTD)超过 20 mg/kg。这意味着在人体临床中,它有极大概率平稳爬升至 10 mg/kg 甚至更高。
2、给药频率:采用 Q3W(每三周给药一次) 方案,这与CytomX 的CX-2051 节奏一致,便于后续在CRC(结直肠癌)赛道进行直接的数据对标。
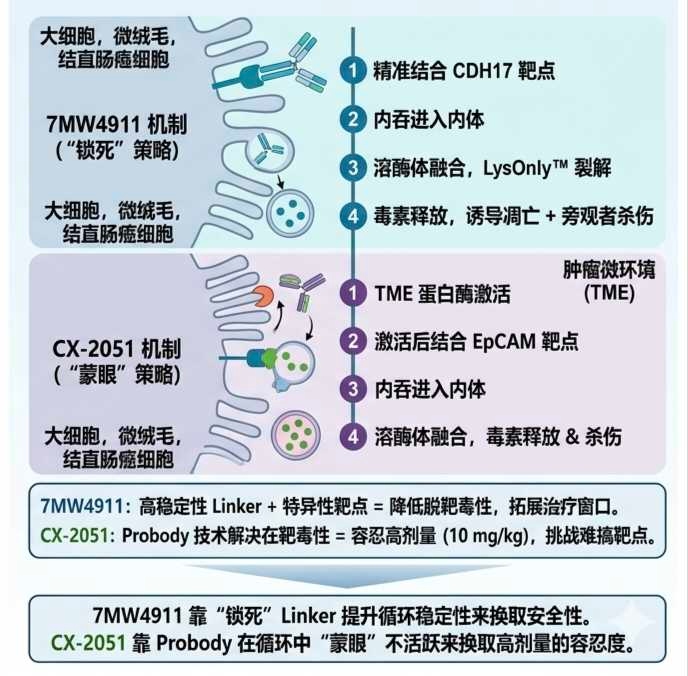
简而言之,对标最强、死磕到底!有信心,有底气!
OK,接下来,除了公司提前公告,我们主要需要关注的是2026 年 10 月在西班牙马德里举办的 ESMO 大会,4911大概率会公布相关数据。
1、安全性窗口期对标:剂量爬升后,如果 3 级腹泻率能低于 10%,它将直接在安全性上封神。
2、“零脱落”验证:通过 PK 数据观察血液中游离毒素 MF-6 的浓度。如果极低,则更进一步证明了迈威 IDDC平台在降低 ADC 全身毒性方面的领先地位。
4911是中美同步临床,届时两地患者的耐受性差异数据也将首次浮出水面,这个潜在明星的BD价值也就水涨船高。
【重要补充】
这是一个从确定后即就被赋予全球开发定位的管线,开发路径从一开始就围绕FDA注册、BD交易和全球商业化设计,I/II期临床一体化推进、比国内常规甚至快一代,以抢跑姿态拼该靶点的FIC,就是要争全球定价权!
ADC临床传统是I期做完要停下来,分析数据,写总结,再向监管机构提交II期方案。这个“间歇期”通常需要 6-12 个月。
但迈威生物4911一体化路径 (I/II),方案在一开始就定好了:只要 I 期爬到某个安全剂量,不需要停顿,直接自动触发 Part B(扩张队列)。这个需要非常高的安全性和对平台的自信才敢这么做,不然就是“以卵击石”!
多说一句,后续实验如果数据足够惊艳(ORR远超标准治疗),企业可以直接去申请加速批准 ,直接跳过或者大幅推迟大规模III期(上市销售同步验证)。
所以,不仅仅是快了整整一代,也备了提前申报的后手。
所以,这种“I/II 期一体化”的设计,孤注一掷的数据驱动、饱和攻击,让 4911 在 2026 年底就有可能读出足以支撑海外授权甚至注册申报的核心数据。不这么做,如果按传统路径,这个数据可能要到 2028 年甚至更晚才能看到。
$迈威生物-U(SH688062)$ $荣昌生物(SH688331)$ $CytomX Therapeutics(CTMX)$