康宁杰瑞JSKN027(112的PLUS版本)之一:能否成为康方生物AK112的升级版?
$康宁杰瑞制药-B(09966)$ $康方生物(09926)$
PD-(L)1和VEGF(R)靶点和临床数据
第一:PD-1和PD-L1的区别
这个几乎没有什么好讨论的,默沙东K药和BMS的O药的销售额远超罗氏的阿替利珠单抗和AZ的度伐利尤单抗,市场的认知是PD-1的疗效是好于PD-L1的,PD-1在肺癌大获全胜,而PD-L1更多的是在消化道肿瘤发力。
但基石药业的PD-L1舒格利单抗在非小适应症国内和欧盟都获批了,并且通过BD在欧盟商业化。PD-L1单抗真的比PD-1弱吗?市场是这样认为的,但是PD-L1的安全性比PD-1好基本确认了。
第二:VEGF靶点和VEGFR2靶点的区别
转发文章,VEGF和VEGFR2的区别,网页链接
具体文章内容,大家可以去仔细读,这个讲的机制非常清楚了,这里直接上图
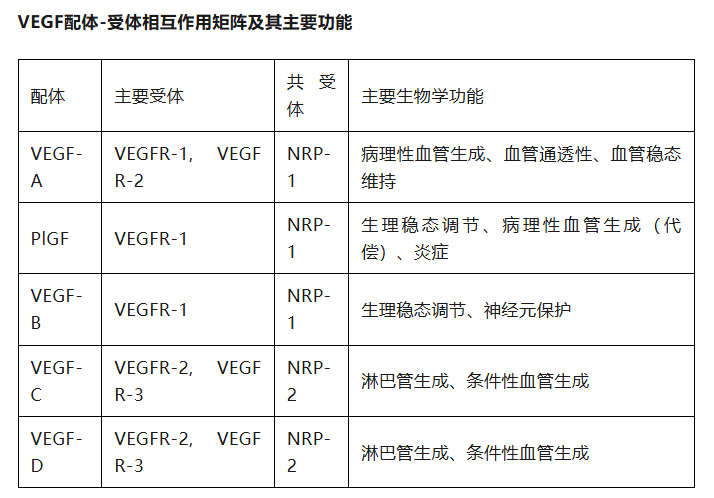
区别和结论就是:VEGF作为配体的代表是贝伐珠单抗,已经批准在非小细胞肺癌的非鳞癌上面使用,由于出血风险不允许在鳞癌上面使用;而VEGFR2作为受体的代表是雷莫芦单抗,安全性得到提升,已经批准在非小细胞肺癌的鳞癌上面使用,因此说明VEGFR2的安全性比VEGF更好基本得到市场认同。下图是安全性对比
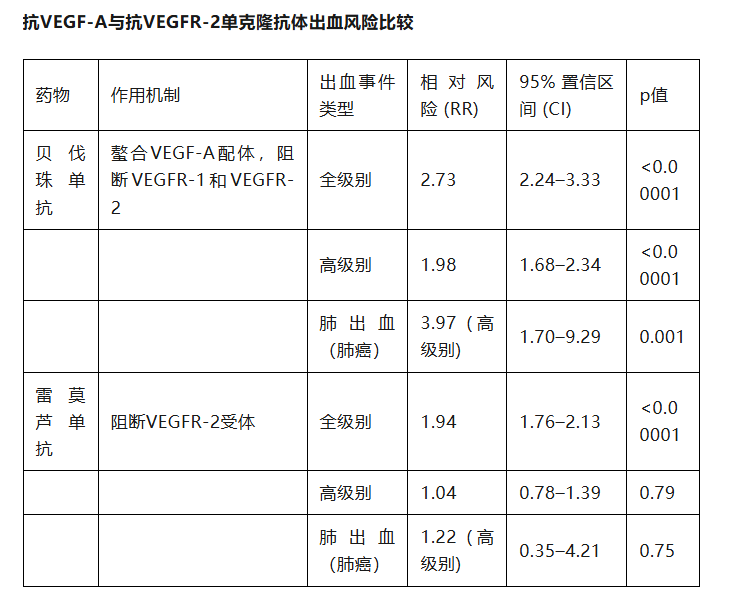
第三:PD-(L)1/VEGF(R)双抗结构和疗效对比
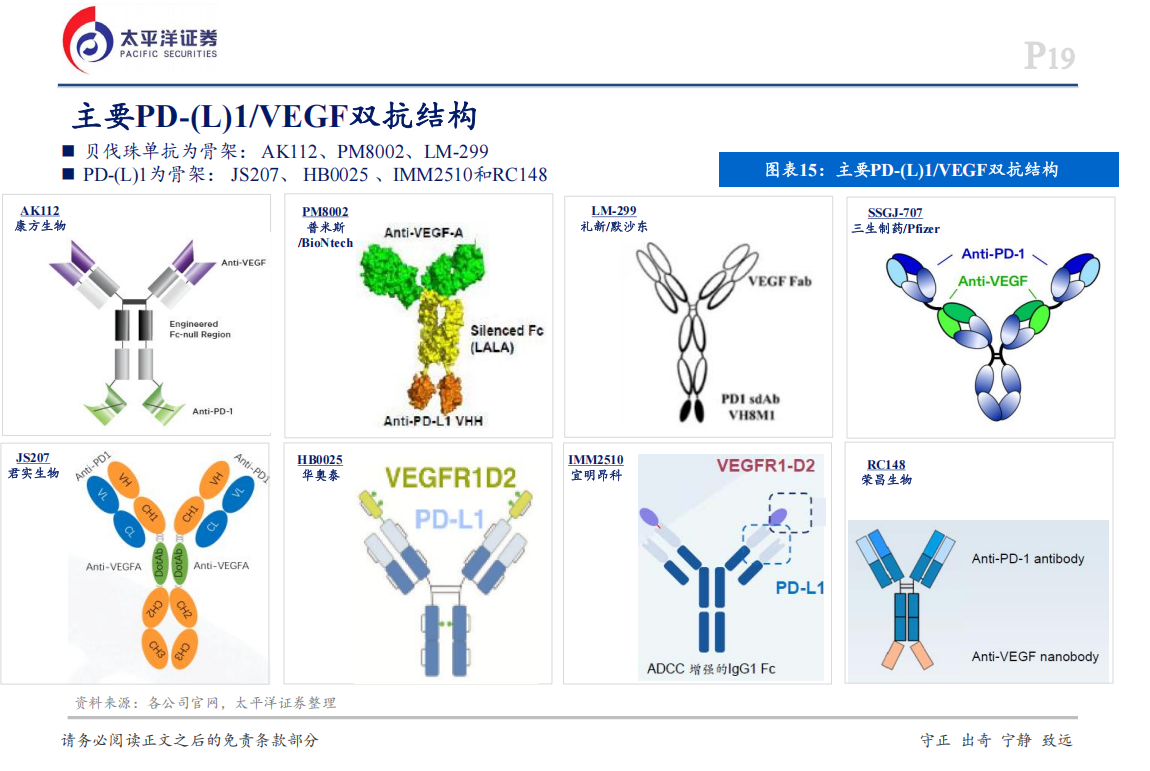
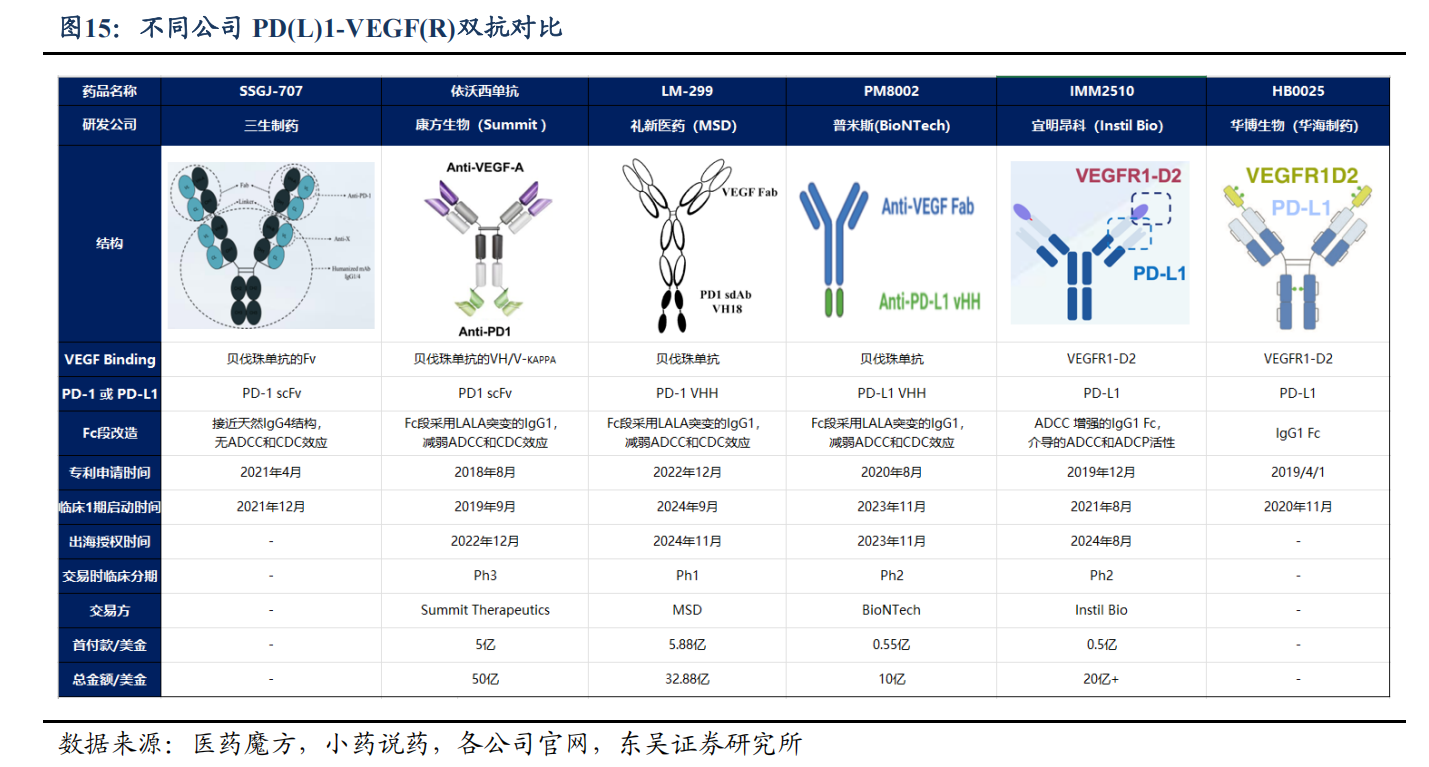
第四:康方生物的AK112的机制可以从这个图来说明,VEGF二聚体成簇,然后提高了PD-1亲和力。
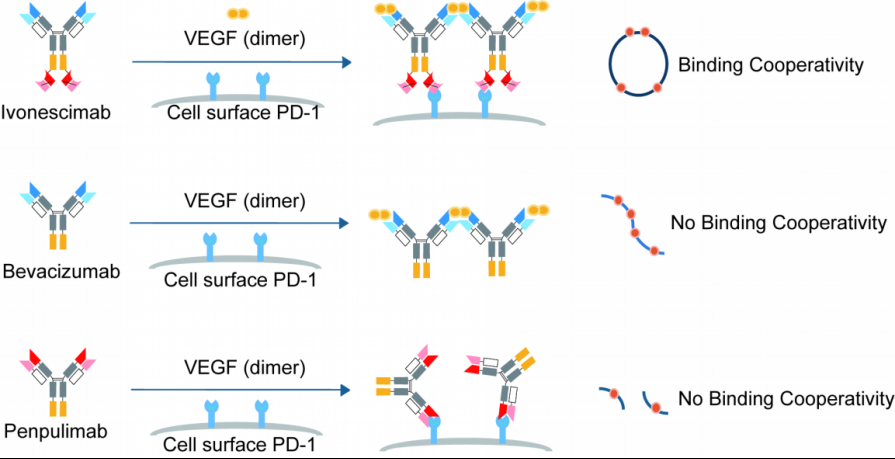
如果只从这个图来说,华海HB0025和宜明昂科的2510他们都使用VEGFR受体来抗血管的机制来说,应该不存在这样的成簇机制,那么疗效ORR(其他分子现在只看就ORR还没有公布PFS和OS)不应该比康方的AK112好的,但是
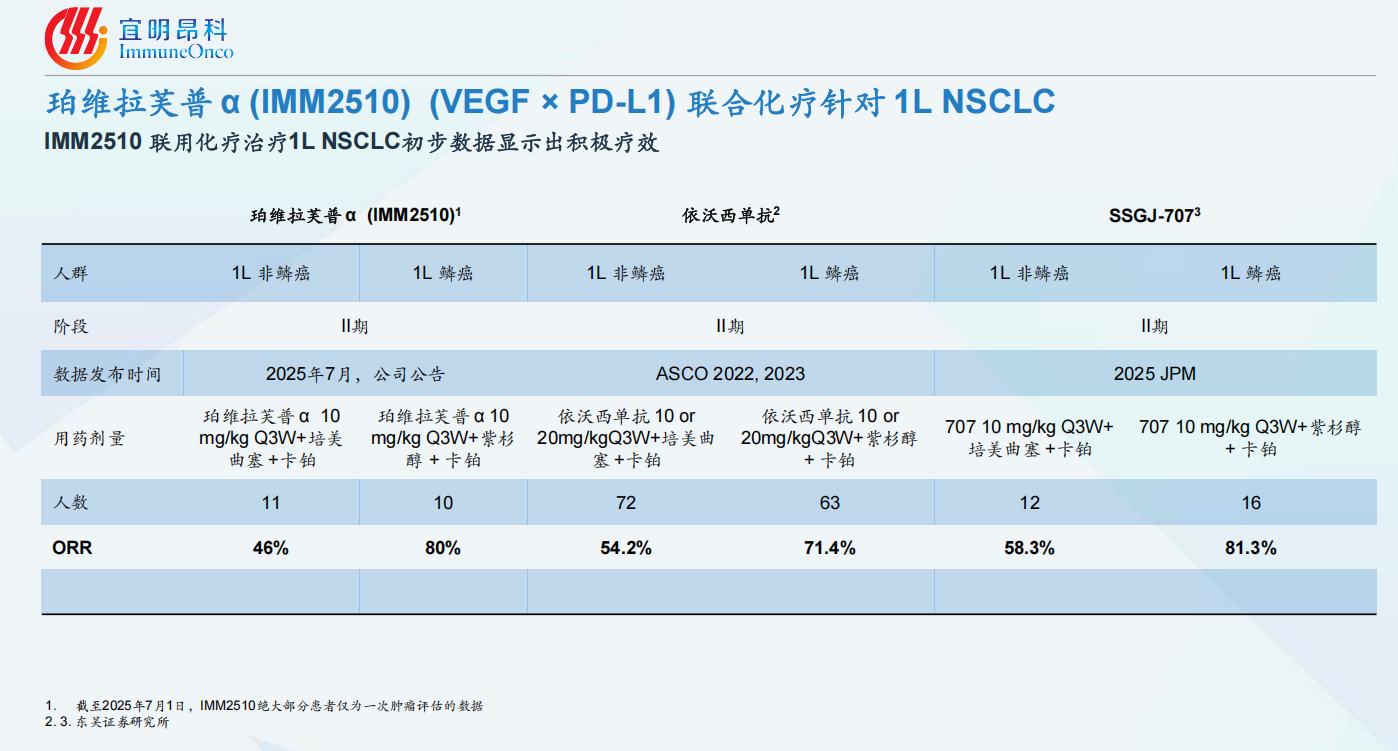
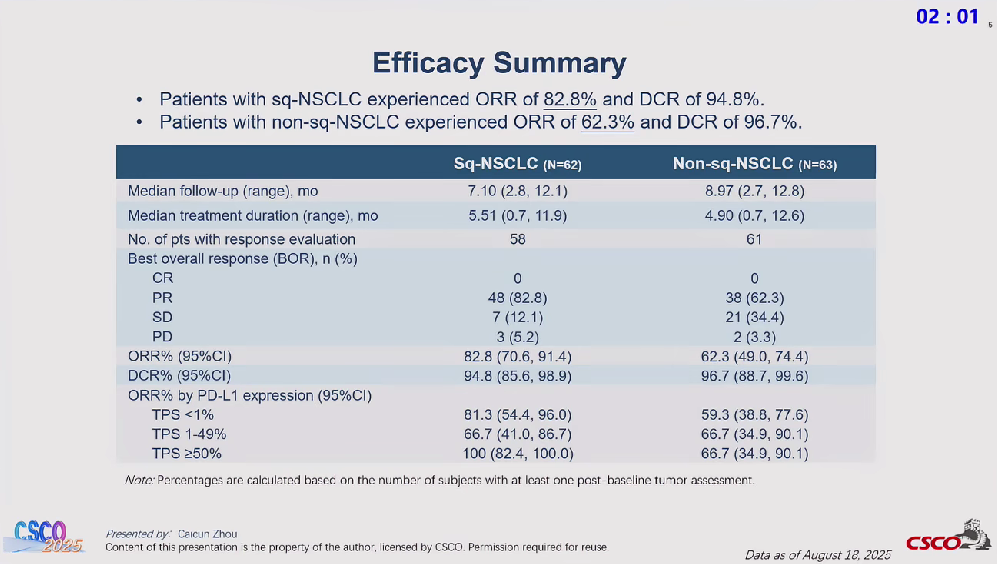
ORR数据:各种结构的PD-(L)1/VEGF(R)双抗联合化疗在一线NSCLC上面的ORR数据,大家其实都差不太多,感觉华海的HB0025在ORR上面有那么一点点优势,ORR比康方生物的AK112高10%左右,所以康方生物在AK112提出的二聚体成簇机制来解释的亲和力提升可能被证伪。其他的几个分子没有成簇机制的数据并不比AK112差,他们都在加快进度追赶得到PFS数据,国内时间差距很大,国外由于SMMT的猪队友还有追赶机会。
HB0025的结构是PD-L1/VEGFR1的,这样联想起来康宁杰瑞的JSKN027的结构是PD-L1/VEGFR2, 和HB0025的PD-L1/VEGFR1差别是华海的VEGFR1是trap捕获器,而康宁杰瑞的VEGFR2是抗体结构。HB0025的临床数据给了康宁杰瑞的JSKN027非常大的信心。包括三生的707的结构数据,也给了康宁杰瑞的JSKN027非常大的信心。现在看JSKN027的分子结构设计,不是心血来潮,而是经过深思熟虑的考虑后做出的理性决策。
安全性:
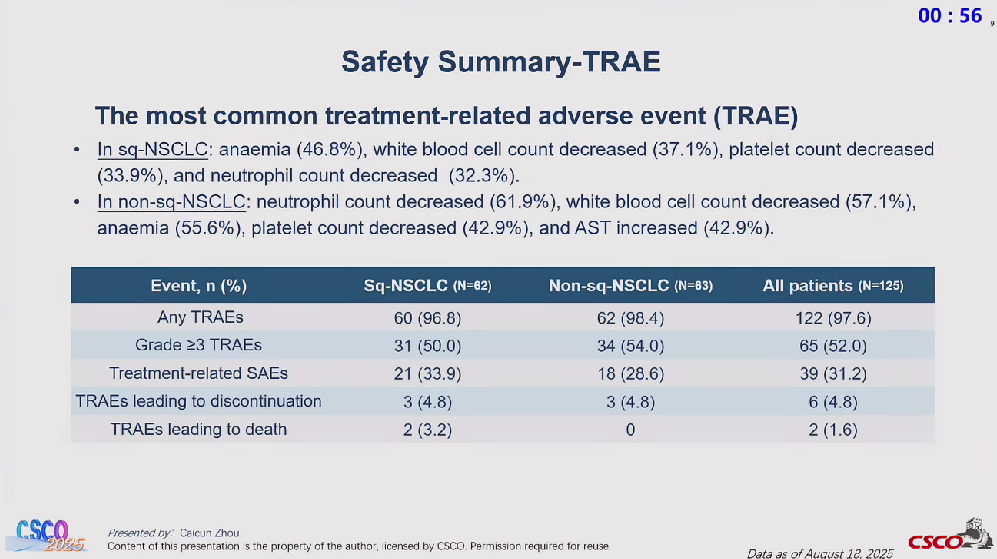
现在在说说本文的重点:康宁杰瑞的JSKN027的机制
1、免疫治疗PD-L1机制:PD-L1抗体免疫治疗疗效上面已经谈过了,康宁杰瑞的027的PD-L1的免疫治疗一端,采取的是PD-L1靶点,从辉瑞和复宏汉霖的PD-L1 ADC分子HLX43的临床数据来看,已经展现出比PD-1更好的数据,特别是在IO耐药方面,展现出非常有潜力和积极的数据支持。并且辉瑞的PD-L1 ADC已经进入临床三期。
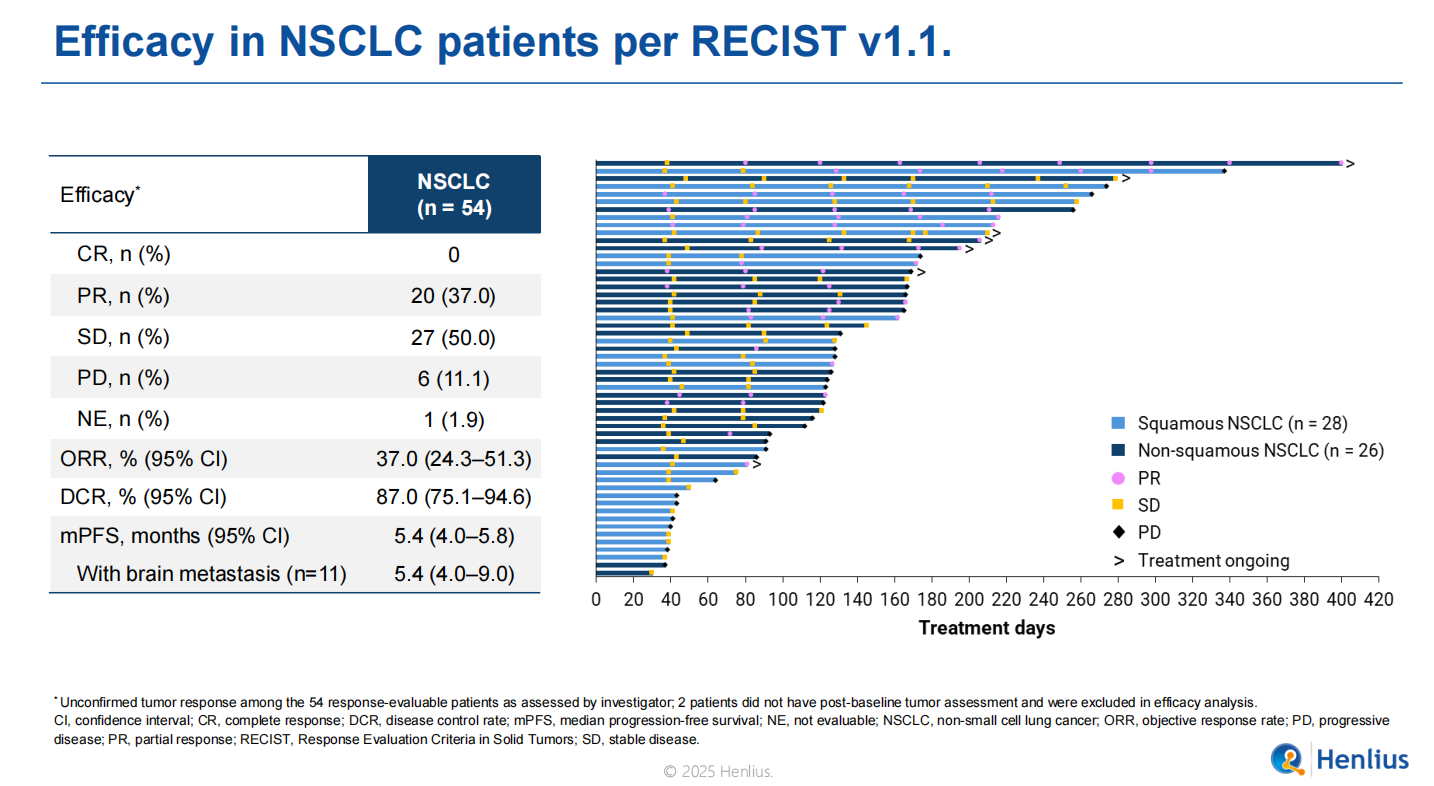
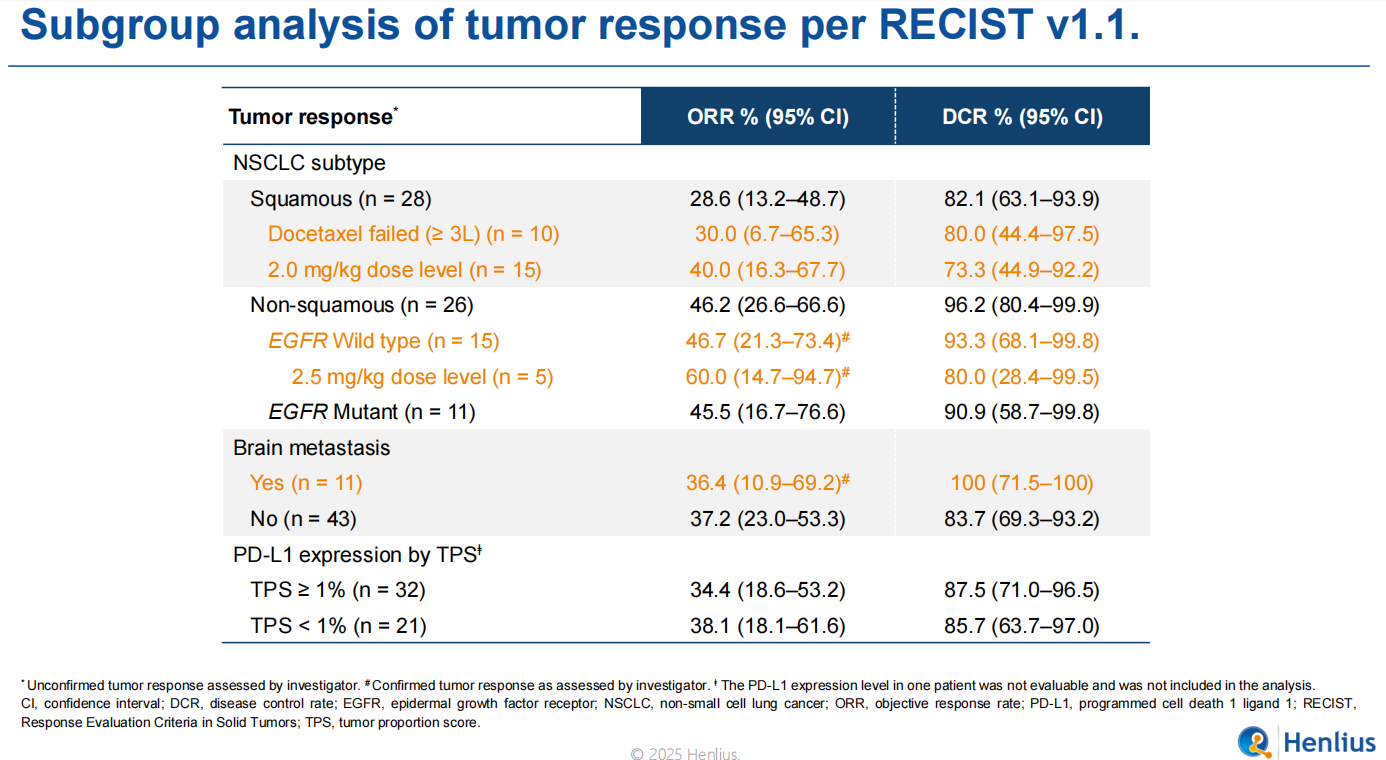
2、VEGF抗血管机制:康宁杰瑞的027 的抗血管这一端,采取的是VEGFR2靶点,根据上面的雷莫芦单抗分析来看,安全性应该比HB0025的更好的安全性,如果单从抗体来看,剂量可以提高到更高的剂量。但因为是ADC,所以剂量如果可以达到8毫克/公斤的话,那么就比较好的满足生物学机制,从曲妥珠单抗升级到8201来看疗效有非常大的提升,因此期待JSKN027可以进一步升级AK112,把疗效提升到新的高度。
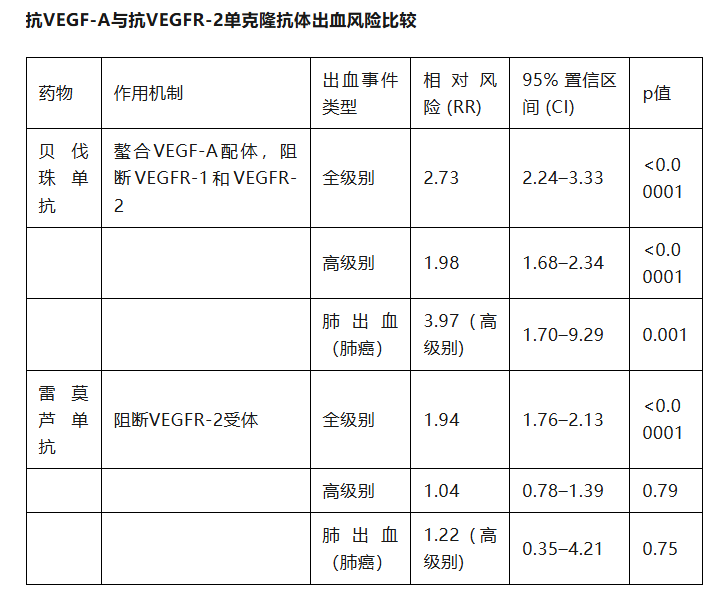
3、JSKN027双抗ADC优势:1、康宁传统优势糖基偶联安全性优势;2、DAR4;3、从复宏汉霖的PD-L1抗体到PD-L1 ADC的疗效提升;4、曲妥珠单抗到8201的ADC的疗效的提升;5、HER3、B7-H3、B7-H4单抗失败而ADC获得成功;6、VEGFR2的安全性保,大家是否可以更积极的期待一下JSKN027呢。
至于JSKN027是否可以成为康方生物AK112的升级版?现在从裸抗体机制来说(HB0025的数据和AK112的数据比较提高大约10%的ORR)存在一定程度的可能性,但还不敢说拉开代际差距,如果从双抗的抗体机制加上ADC机制来说,我觉得AK112的升级版的可能性比较高,有可能真的会拉开代际差距!
4、时间进度:TROP2/HER3双靶点ADC分子JSKN016从2024年5月开始首例患者入组,经过1年3个月的时间,大约200人的样本量,基本验证了在ORR上面的BIC潜力,至于PFS还需要更长的随访时间,关于016的详细文章,请参见“决战JSKN016------他日若遂凌云志 敢笑黄巢不丈夫之九(大结局:为什么迟早会爆发)链接网页链接,临床前的预测正在逐步变成现实。
PD-L1/ITGB6双靶点ADC分子JSKN022在7月底申请了IND临床试验,如果9月底拿到批文,11月底入组首例患者,中山肿瘤的徐瑞华院长作为PI,大约2026年底或者2027年一季度可以看见200人左右的ORR数据,主打头颈癌和结直肠癌。关于022的详细文章,请参见“JSKN022:时人不识凌云木,直待凌云始道高之---临床前汇总贴”链接网页链接。到时候看看这个预测和现实有多少差距。
那么这个JSKN027如果11月申请IND,大约2027年底可以看见200人左右的样本数据,也就是说2年时间基本上可以看见结果,是否真正的是AK112的升级版。
总结:未来肺癌的治疗模式除了IO2.0+ADC2.0之外,本人全市场第一个提出:还可以期待ADC2.0比如JSKN027联合ADC2.0比如JSKN016.也就是JSKN027+JSKN016。这可能是康宁杰瑞除了KN026 ,JSKN016,JSKN022 之外的第四个大药,未来已来!耐心等待!
理性思考,欢迎讨论@TfR1lyxxx快乐鼠鼠 @高棋剑 @大隐无言 。
鉴于鼠博士开始谈机制,不上杀手锏他是不服气的,仔细把这个文章读一下吧。
Molecular Cancer:PD-L1/VEGFR2双抗纳米体短暂表达即可长期激活T细胞,抑制癌症转移。网页链接
2025年4月19日,来自中国科学院、中国科学院大学、中山大学研究人员在Molecular Cancer上发表了标题为“Transient intracellular expression of PD-L1 and VEGFR2 bispecific nanobody in cancer cells inspires long-term T cell activation and infiltration to combat tumor and inhibit cancer metastasis.”的研究成果,发现癌细胞中PD-L1和VEGFR2双特异性纳米体在细胞内的短暂表达激发T细胞的长期活化和浸润,从而对抗肿瘤并抑制癌症转移。
为解决癌症治疗中药物治疗无效及免疫反应不足的问题,本研究开展了针对PD-L1 和 VEGFR2 双特异性纳米抗体的研究。PD-L1和VEGFR2在肿瘤发生中起着关键作用。然而,当前在免疫检查点阻断和抗转移抗癌治疗方向,针对微型双特异性细胞内纳米体仍存在空白。本研究成功开发了与抗体VH区融合的双特异性体内FAP1V2,并证实其能够靶向和阻断人和小鼠的PD-L1和VEGFR2,抑制癌细胞与PD-1的结合,降低细胞迁移能力。PD-L1和VEGFR2双特异性VH细胞内纳米体具有高度的生物相容性,通过PD-L1/PD-1检查点阻断介导的长期免疫激活和VEGFR2阻断介导的抗肿瘤转移,证明其具有联合以上两种作用抗癌的潜力。