康宁杰瑞JSKN027(AK112的PLUS版本)之五:PD-L1和VEGFR2双抗的机制说明
$康宁杰瑞制药-B(09966)$ $康方生物(09926)$ 转发一篇公众号的文章,说明“双靶点纳米抗体新突破!同时阻断PD-L1与VEGFR2,激活长效抗癌免疫+抑制转移”,过去的文章都写的不够详细,这个文章写得非常详细,大家可以参考这个文章,对于理解康宁杰瑞的JSKN027的PD-L1和VEGFR2双靶点ADC更有帮助,而康方生物的AK112的靶点是PD-1和VEGF,一个是作用在免疫细胞,一个作用在抗血管的因子,康方生物和康宁杰瑞的作用的方向不一样,康方是一个配体,而康宁是受体。因为是作用于肿瘤的受体上,所以康宁杰瑞在这个文章提到的双抗基础上,又进一步进行了升级做成了双抗ADC,加上了毒素拓扑异构酶抑制剂Dxd的细胞毒性的化疗功能,这样就具有细胞毒杀伤+抗血管生成+免疫调节三个功能了,可以说是结合了三个功能的IO2.0+ADC2.0的一步到位功能。
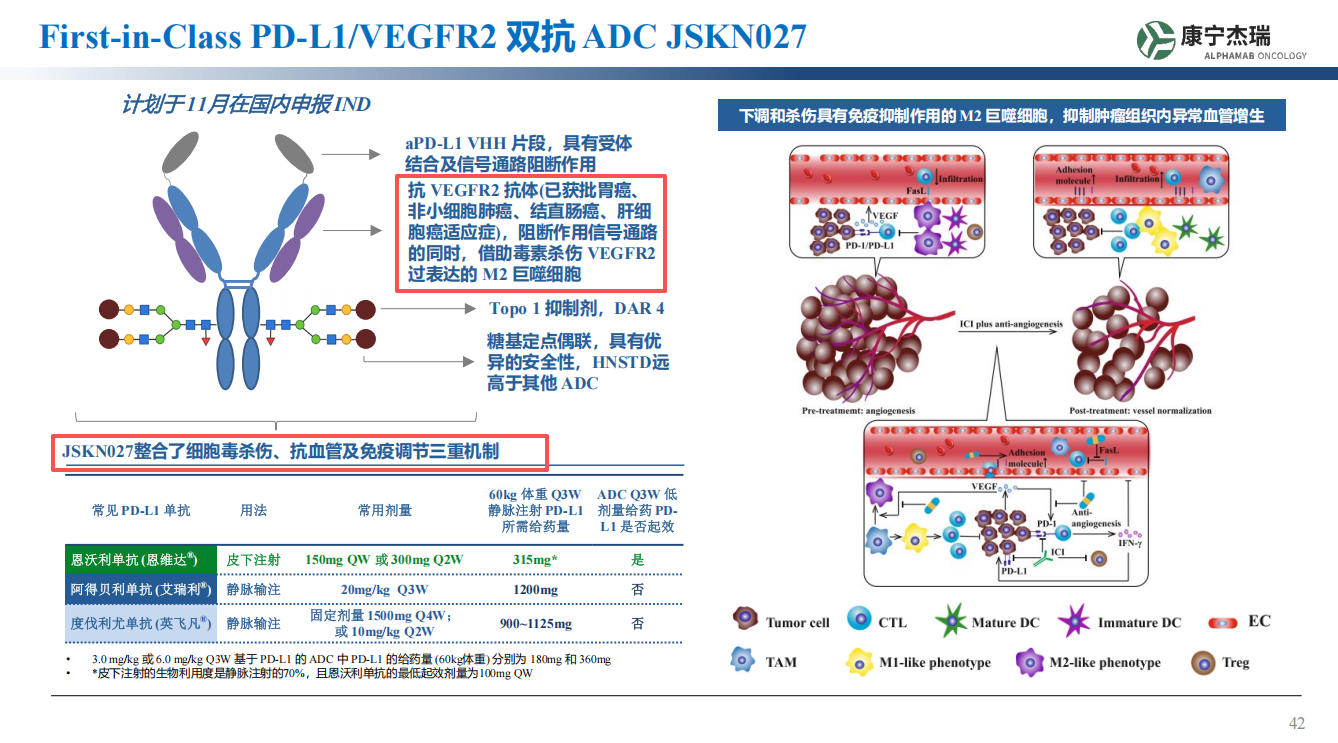
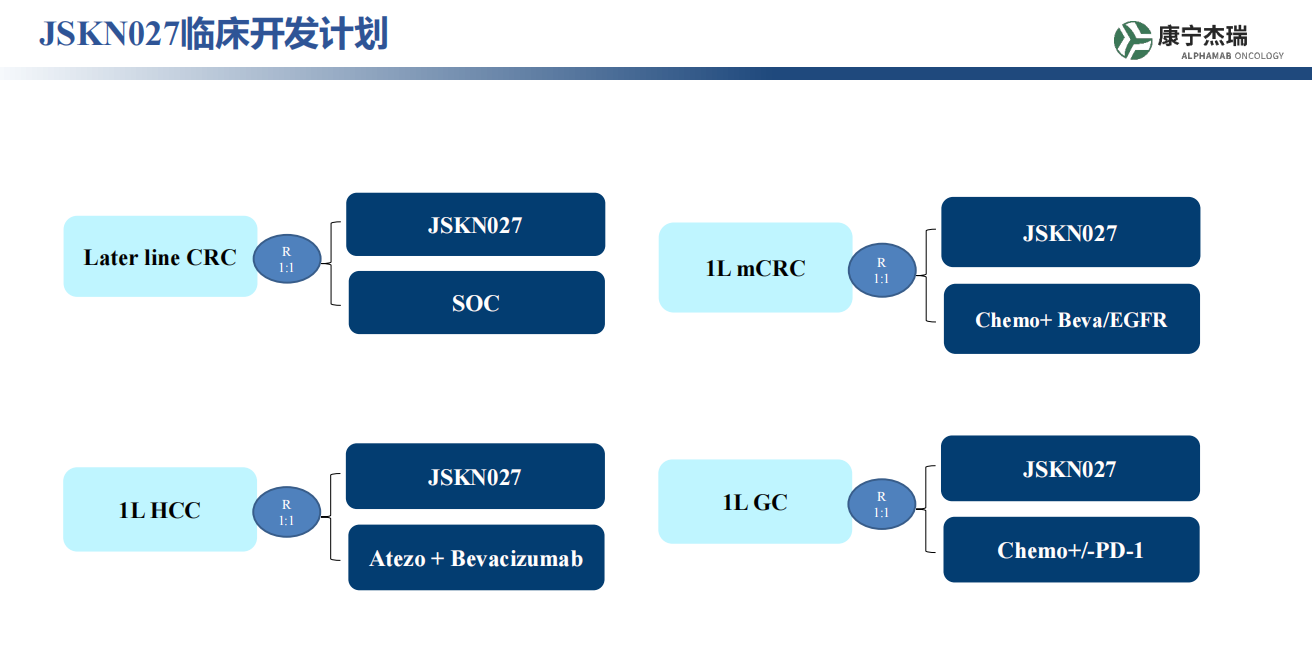
2026年3月17日,中国苏州,康宁杰瑞生物制药(股票代码:9966.HK)宣布,公司自主研发的PD-L1/VEGFR2双特异性抗体偶联药物(ADC)JSKN027治疗晚期恶性实体瘤的Ⅰ期临床研究(研究编号:JSKN027-101)已完成首例患者给药,经过7-8个月剂量爬坡,可能在年底就会看见027的初步数据了。
文章链接:网页链接
文章具体内容:癌症治疗的两大核心难题——免疫逃逸与远处转移,长期制约着临床疗效。PD-L1介导的免疫检查点通路会让肿瘤细胞“隐身”躲避T细胞攻击,而VEGFR2信号通路则驱动肿瘤血管生成与转移扩散,两者协同促进癌症进展。传统单一疗法难以同时破解这两大困境,且易引发免疫相关副作用或脱靶效应。
近期,《Molecular Cancer》发表的一项创新性研究,成功开发出PD-L1/VEGFR2双特异性纳米抗体FAP1V2,通过胞内瞬时表达技术,实现“免疫激活+抗转移”双重功效,在肺癌模型中展现出显著的肿瘤抑制效果,甚至诱导长效免疫记忆,为癌症联合治疗提供了全新思路。
一、核心设计:双靶点纳米抗体的“精准打击”逻辑
研究团队摒弃传统抗体的Fc片段与轻链可变区(VL),仅保留重链可变区(VH),构建出超小型双特异性胞内抗体FAP1V2,其设计亮点兼具特异性与实用性:
•双靶点协同:一端靶向PD-L1,阻断PD-1/PD-L1免疫抑制通路;另一端靶向VEGFR2,抑制肿瘤血管生成与细胞迁移,同时解决免疫逃逸与转移两大痛点;
•结构优化:通过柔性连接肽(GGGGS)串联抗PD-L1 VH(FAP1)与抗VEGFR2 VH(FAV2),中间融合EGFP作为示踪标记,N端添加IL-2信号肽、C端连接GPI锚定序列,确保抗体在细胞内精准定位并发挥作用;
•低免疫原性:仅含VH结构域,分子量小且无外源异源片段,生物相容性高,避免传统抗体引发的免疫相关不良反应。
•
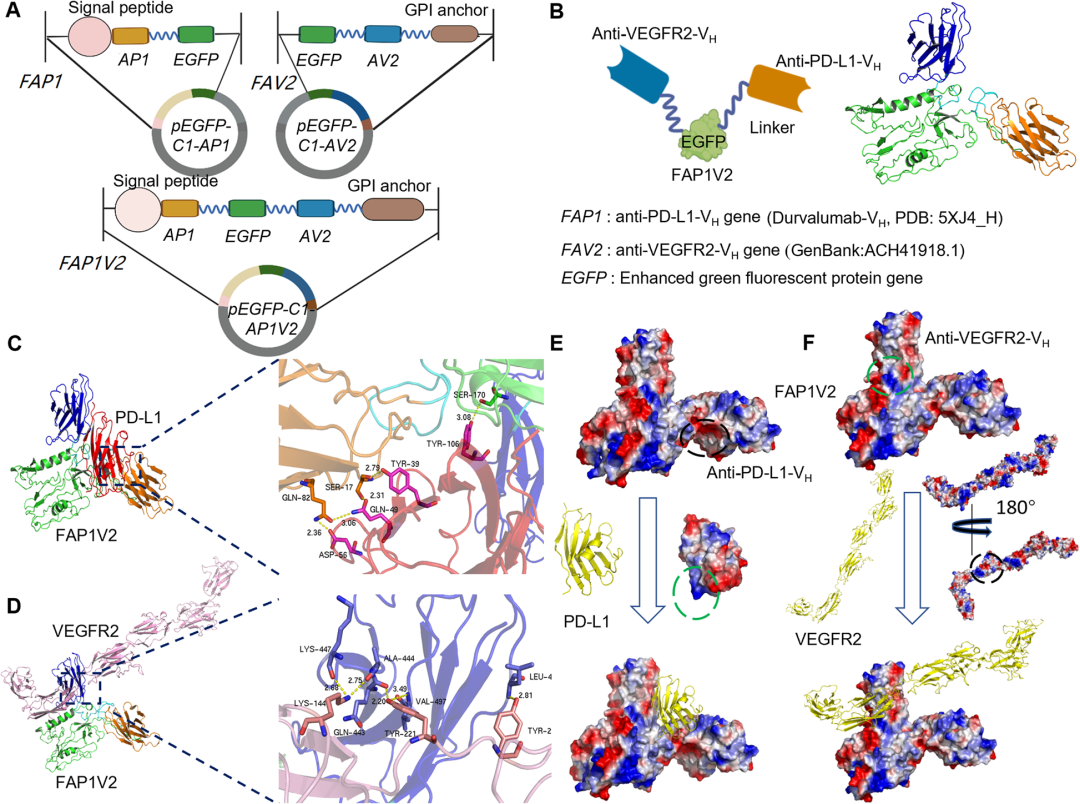
图1:FAP1V2双特异性纳米抗体结构与作用机制
:A图为FAP1V2分子结构示意图,展示IL-2信号肽、抗PD-L1 VH、EGFP、抗VEGFR2 VH及GPI锚定序列的串联模式;B图为3D模型,橙色区域为抗PD-L1结构域,深蓝色为抗VEGFR2结构域,绿色为EGFP,呈现“夹子状”结合构象,可同时识别两个靶点的不同表位。
二、核心功能:三重功效,重塑抗癌防线
FAP1V2通过精准靶向PD-L1与VEGFR2,在体外与体内实验中均展现出“阻断通路+激活免疫+抑制转移”的三重核心功效:
1. 特异性阻断双靶点,抑制肿瘤细胞功能
•PD-L1阻断:FAP1V2可与细胞表面及胞内PD-L1结合,占据其与PD-1的结合位点,显著降低PD-L1与PD-1的相互作用,解除免疫抑制;
•VEGFR2阻断:特异性结合VEGFR2,抑制其下游AKT、ERK等信号通路激活,减少肿瘤细胞迁移能力,体外划痕实验显示,FAP1V2表达组细胞迁移距离较对照组减少50%以上;
•特异性验证:免疫共沉淀与竞争结合实验证实,FAP1V2仅与PD-L1、VEGFR2结合,不与其他细胞因子交叉反应,靶点特异性强。
2. 激活长效T细胞免疫,避免T细胞耗竭
在LLC肺癌小鼠模型中,FAP1V2胞内瞬时表达展现出强效免疫激活效果:
•肿瘤组织中高表达TCRβ的活化T细胞(TCRβhi)浸润显著增加,这类细胞是特异性杀伤肿瘤细胞的核心力量;
•脾脏中CD25hi活化T细胞比例升高2.2倍,CD25是T细胞激活的关键标志物,提示全身免疫应答被有效唤醒;
•肿瘤微环境中PD-1高表达(PD-1hi)的耗竭型免疫细胞数量大幅减少,避免T细胞功能衰竭,维持长期抗癌活性。
•
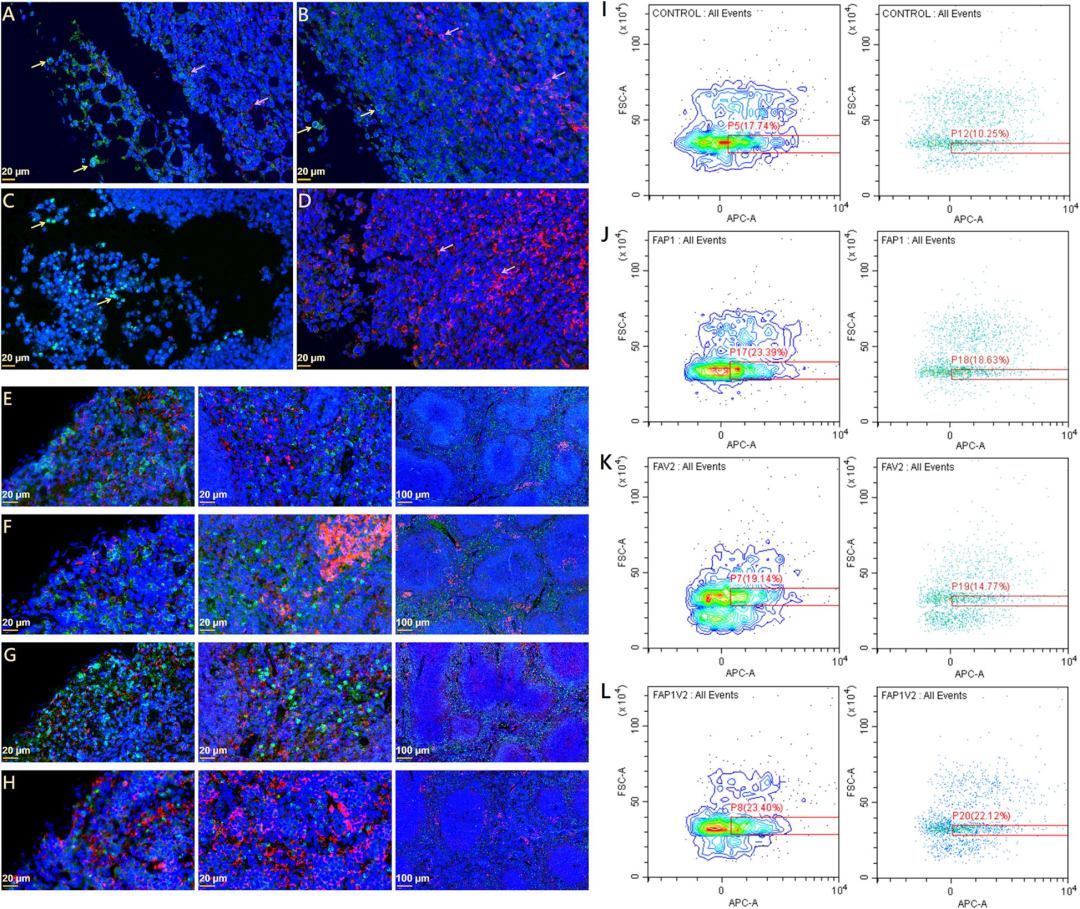
图2:FAP1V2对T细胞活化的调控作用
:左图为免疫荧光结果,黄色箭头指示肿瘤组织中TCRβhi T细胞(绿色荧光)浸润,红色箭头指示PD-1hi免疫细胞(红色荧光),FAP1V2组绿色荧光显著多于对照组,红色荧光明显减少;右图为流式分析结果,显示FAP1V2组脾脏CD25hi T细胞比例显著高于对照组,证实免疫激活效果。
3. 强效抑制肿瘤转移,降低远处扩散风险
•体外抑制迁移:HeLa与LLC细胞中表达FAP1V2后,迁移能力显著下降,且对细胞活力无明显影响,说明其通过抑制迁移通路发挥作用,而非直接杀伤细胞;
•体内抗转移验证:小鼠肺、肝组织免疫荧光分析显示,FAP1V2组未检测到明显的LLC肿瘤细胞转移灶,而对照组与单靶点抗体组均出现不同程度的转移,证实其阻断VEGFR2通路的抗转移功效。
三、体内疗效:肿瘤抑制+免疫记忆,双重保障
在C57BL/6小鼠LLC肺癌模型中,FAP1V2的治疗效果显著优于单靶点抗体(FAP1、FAV2)与对照组:
•肿瘤生长抑制:通过两次瞬时表达FAP1V2,小鼠原发肿瘤与二次接种肿瘤的生长均被显著抑制,1/6小鼠实现肿瘤完全消退;
•免疫记忆形成:对完全缓解的小鼠进行肿瘤细胞再挑战,90%的小鼠未出现肿瘤复发,表明FAP1V2诱导产生了长效抗原特异性免疫记忆,持续保护机体免受肿瘤侵袭;
•安全性优异:实验期间小鼠体重无明显下降,主要器官(心、肝、脾、肺、肾)的组织病理学分析未发现异常损伤,证实其生物安全性。
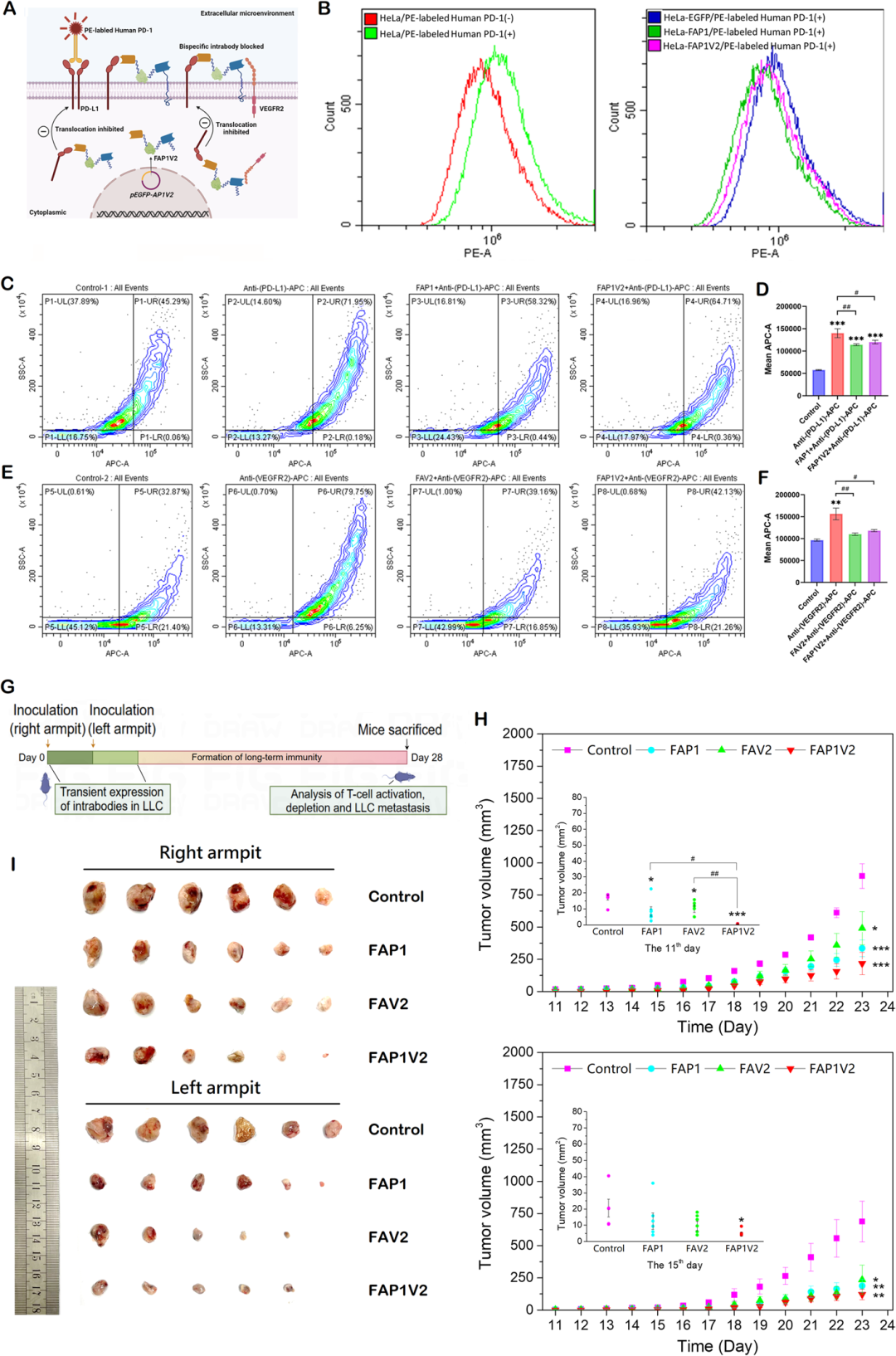
•图3:FAP1V2在小鼠模型中的肿瘤抑制效果:H图为肿瘤生长曲线,显示FAP1V2组肿瘤体积显著小于对照组、FAP1组与FAV2组;I图为实验终点剥离的肿瘤实物图,直观呈现FAP1V2对肿瘤生长的强效抑制作用,二次接种肿瘤的抑制效果更显著。
四、分子机制:转录组层面揭示核心调控通路
通过转录组测序分析,FAP1V2表达后,HeLa细胞中多个与肿瘤进展相关的通路发生显著变化:
•免疫相关基因:CD160(NK细胞激活因子)、FOXP3(免疫调节因子)等上调,增强免疫应答;
•迁移抑制基因:PCDHA6、UCN、MXRA8等上调,这些基因可抑制细胞黏附与迁移;MET、DDR2、PI16等促迁移基因下调,阻断肿瘤转移信号;
•关键通路调控:Wnt/β-catenin、PI3K/AKT等促癌通路被抑制,TGF-β1、NF-κB等炎症与免疫通路被激活,从转录层面重塑细胞功能,抑制肿瘤进展。
五、临床转化价值与展望
这项研究的创新之处,在于首次开发出PD-L1/VEGFR2双特异性胞内纳米抗体,为癌症联合治疗提供了全新技术路径,其核心转化价值体现在:
•治疗场景广泛:同时适用于实体瘤的原发灶控制与转移灶抑制,尤其对PD-L1与VEGFR2高表达的肺癌、宫颈癌等癌症具有针对性;
•联合治疗潜力:可与免疫检查点抑制剂、化疗药物或细胞治疗联合使用,进一步增强疗效,为难治性癌症提供个性化治疗方案;
•递送方式灵活:可通过质粒转染、纳米载体递送等方式实现胞内表达,未来可开发成基因治疗药物,精准靶向肿瘤细胞;
•低毒高效优势:生物相容性高、无明显副作用,解决传统联合疗法不良反应叠加的问题,提升患者耐受性。
目前,双特异性抗体已成为癌症免疫治疗的热门方向,但针对PD-L1与VEGFR2的胞内双特异性纳米抗体尚未进入临床。FAP1V2的成功研发,不仅验证了“免疫激活+抗转移”联合策略的可行性,更为纳米抗体在癌症治疗中的应用开辟了新场景。未来通过优化递送系统、提升体内表达稳定性,有望推动这类新型抗体进入临床,为癌症患者带来新的治疗选择。
文献参考
Zhang L, Lin Y, Hu L, et al. Transient intracellular expression of PD-L1 and VEGFR2 bispecific nanobody in cancer cells inspires long-term T cell activation and infiltration to combat tumor and inhibit cancer metastasis. Molecular Cancer. 2025;24:119.(DOI: 10.1186/s12943-025-02253-6)
参考文献下载链接:
网页链接{Transient intracellular expression of PD-L1 and VEGFR2 bispecific nanobody in cancer cells inspires long-term T cell activation and infiltration to combat tumor a.pdf}