再鼎医药的贝玛

9月3号由于贝玛妥珠单抗Fortitude 101”试验的最终分析显示,总生存期获益有所减弱,上市申请可能会出现延迟,第二天9月4号港股再鼎医药单日下跌了12%,惨不忍睹。
那我们静下心来分析一下贝玛在再鼎医药的权益区中国获批的情况,首先我们来看一下公告后再鼎医药总裁兼首席运营官乔希·斯迈利(Josh smiley)于9月4日参加Cantor全球医疗健康大会的访谈:
我们与安进公司(Amgen)合作开展了贝马托珠单抗(pembrolizumab)一线治疗胃癌的项目,该项目包含两项研究。其中一项是“贝马托珠单抗联合化疗”与“单纯化疗”的对照试验,即“达到了具有统计学意义和临床意义的获益终点”试验(试验名,暂译“坚韧 101”)。这项试验在中国意义重大,因为目前胃癌一线治疗的标准方案就是化疗。大约一个半月前,我们宣布该试验在预设的中期分析中,总生存期(OS)达到了具有统计学意义和临床意义的获益终点。
而在昨天的另一场会议上,安进公司披露,该试验的最终分析显示,总生存期获益有所减弱,并计划在今年晚些时候的大型医学会议上公布完整数据。
由于距离该医学会议时间较近,目前我们不便对数据过多置评,仍需等待会议公布结果。不过,基于这一新信息,我们将调整计划:等待第二项试验的结果——该试验是“巴玛联合化疗与 PD-1 抑制剂”对比“单纯化疗与 PD-1 抑制剂”,试验结果预计在今年年底或明年年初公布。待两项试验数据均出炉后,我们会综合分析所有信息,再推进后续的上市申请策略。因此,我无法对当前数据本身发表评论,但可以明确的是,我们已调整思路:不再基于“Fortitude 101”这一项试验单独提交申请,而是将两项试验数据整合后再制定下一步计划。
至少从目前来看,上市申请可能会出现延迟,预计延迟时间在 6 个月左右。当然,我们仍需进一步研究和理解完整数据。此外,投资者届时也将有机会看到“Fortitude 101”试验的相关数据——包括显示总生存期获益的中期主要分析数据,以及后续的 6 个月最终分析数据,这两组数据都将在即将召开的医学会议上公布。
即将召开的重大医学会议大概率指的就是ESMO会议,欧洲肿瘤内科学会年会(ESMO2025)将于2025年10月17日-21日在德国柏林举办。一个多月我们也就将知道101相关数据。
那么目前来看贝玛有几种情况:
1、101和102试验数据OS结果达到了具有统计学意义和临床意义的获益终点,获得FDA和CDE双重批准,完美结果。
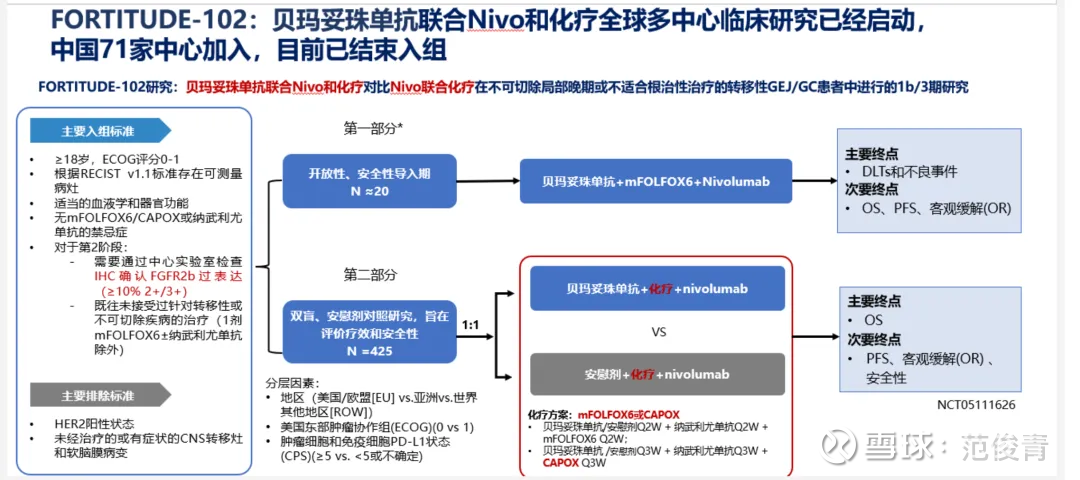
从目前101的试验来看,主要是后线干扰问题影响了OS,对照组化疗患者进展后一定会寻求免疫疗法作为后续治疗。现行的标准疗法是免疫加化疗,所以安进也提前考虑了这个问题,做了102试验,102试验组(贝玛妥珠单抗 + 化疗 + 纳武利尤单抗)对(化疗 + 纳武利尤单抗+安慰剂)基本就不受后线干扰,数据大概率是可以获得阳性结果的。
2、全球临床OS未取得统计学差异的阳性结果,但中国区数据支持CDE批准。
101入组了547例患者和102入组了528例患者,其中101中国患者占比40%约218人,102未披露占比,正常也应该占比40%左右,我们按低值来算也有35%约185人,这样大约有400位中国人群数据,其实中国部分数据应该是很好的,主持三期的PI李进教授当时差不多是明说了,当然当时李进说的时候安进还没有更新后面的衰减。如果数据和二期结果有一致性趋势的25-30个月的mOS,且相对于对照组显著获益,由于这是预后很差的晚期胃癌,又是中国多发病人的适应症,药在中国获批没有问题。这样万一总体数据不行,但中国仍然可以获批,那么再鼎医药整好是中国区权益。

3、中国区也未能获批。
这种情况是小概率事件,但仍然有可能发生。
如果是1和2的结果,其实对再鼎医药几乎没有影响,包括推迟6个月的时间。我们来看,原来计划今年末向CDE提交申请,那么现在这个申请最多可能被推迟六个月申请,也就是明年6月份前可以递交申请,由于获得FDA和CDE双重认证“突破性疗法”,加上现在CDE整体审批效率加速,那么仍然可以赶在27年6月30日前获批,不影响当年的医保谈判,28年进入医保,而原来的预期其实也是28年进入医保,由于进医保前的销量有限,所以如果是1和2的结果,贝玛在中国的销售基本不受影响。
如果是3的结果,那么我们要考虑再鼎去掉贝玛的价值如何呢,老范认为没有贝玛,对再鼎医药中期估值的影响是不小的,但仍然认为对于再鼎医药目前来说仍然还是低估的。
再鼎的核投资逻辑在于中国和海外双向飞轮转动,搭好框架后会一方面引入源源不断的药物,通过国内极少数能获得FDA认可的临床试验能力以及卓越的商业化能力,实现规模化的提升,提效提质,成为海外药企进入国内最优等级考虑的公司,另一方面自研含全球权益管线引进并走出海外的双轮驱动,所以未来看再鼎的核心在于还有没有更多的1310,还有没有更多的类似POVE、艾加莫德的引进,以及艾加莫德、pove更多新的适应症开展。
附上总裁Josh Smiley的简介:
Josh Smiley:总裁兼首席运营官
2022 年 8 月加入再鼎医药,在再鼎医药,Smiley 先生全面管理商业化、生产、业务拓展、财务、人力资源、信息技术、企业事务和战略各个方面的工作。加入再鼎之前,Smiley 先生在礼来公司担任首席财务官。他在礼来工作超过 25 年,担任过多个要职。在晋升为首席财务官之前,他担任高级副总裁,负责财务、企业内控和资金管理。他在礼来的工作经验还包括领导美国销售和市场工作(重点关注支付方和公共部门客户),以及业务拓展和并购。
$再鼎医药(09688)$ $云顶新耀(01952)$ $和铂医药-B(02142)$
文章同发于:网页链接