Genmab终止PD-L1/4-1BB双抗研发点评

$维立志博-B(09887)$ $Genmab(GMAB)$
2025年12月29日,Genmab宣布终止PD-L1/4-1BB双抗acasunlimab开发,将把资源集中在更具潜力的项目上,包括 CD3×CD20双特异性抗体epcoritamab、EGFR/LGR5双抗petosemtamab 和FRα ADC药物 rinatabart sesutecan。

1、PD-L1/4-1BB双抗acasunlimab开发进展
目前在3期临床,也是全球唯一一款在3期临床阶段的PD-L1/4-1BB双抗,3期适应症为联用K药治疗PD1/PD-L1抗体及铂类化疗经治的NSCLC二/三线。
2、acasunlimab 2期数据
其实2期数据就有点奇怪,在PD1/PD-L1抗体及铂类化疗经治的NSCLC二/三线患者中,arm B(acasunlimab 100 mg + pembro 200 mg Q3W)、arm C(acasunlimab 100 mg + pembro 400 mg Q6W)的mOS分别为8.6个月、17.5个月,Q3W给药的效果竟然不如Q6W...

安全性方面,4-1BB在肝毒性方面的问题也比较严重,单药组≥3级及以上AE发生率8.7%,联用K药组13.3%。

3、利好国内维立志博,但维立志博PD-L1/4-1BB双抗也有待更大样本量数据验证
维立志博PD-L1/4-1BB双抗LBL-024在结构设计上和Genmab的acasunlimab有比较大的差异,LBL-024是2+2的设计,acasunlimab是1+1的设计。
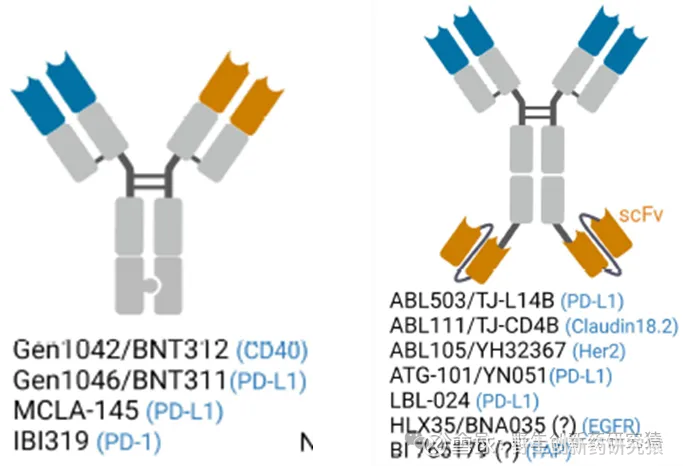
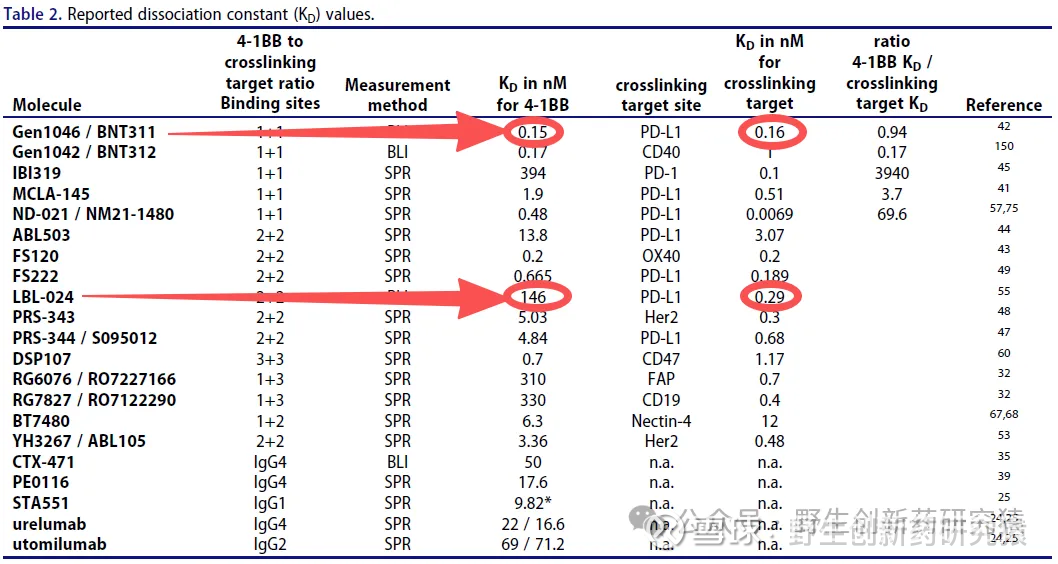
从亲和力的差异来看,LBL-024对于PD-L1的亲和力远远强于4-1BB,而acasunlimab对两者的亲和力类似;按照现有的理论,降低对4-1BB的亲和力、增强对PD-L1的亲和力有助于减少4-1BB带来的肝毒性问题。
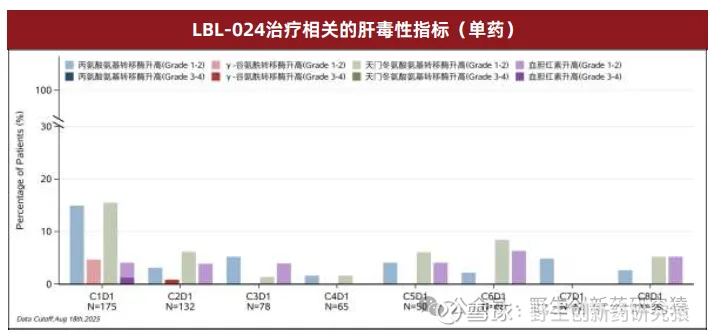
从维立志博研发日披露的LBL-024单药肝毒性数据来看,上述设计确实有用,治疗期间没有看到≥3级及以上肝毒AE。
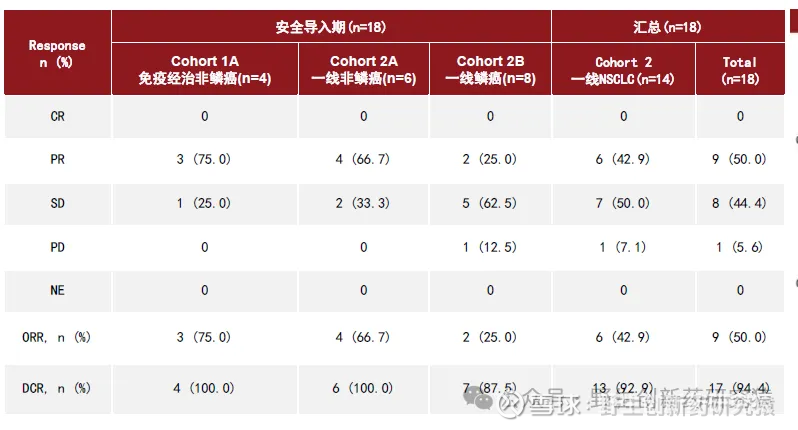
疗效数据上,LBL-024目前针对NSCLC的样本量较少,但早期拿到的ORR都还不错,未来需要更大样本量的数据验证。
总结下来就是,Genmab的acasunlimab停止开发后,在PD-L1/4-1BB双抗这赛道上维立志博LBL-024自动往前了一步。从现有数据来看,LBL-024可能解决了4-1BB靶点的肝毒性问题,早期疗效的ORR数据也不错,但还有待更多数据验证,值得持续跟踪。
(注:以上仅为行业观点分享,不涉及具体标的的投资建议)