首款!百济神州 HER2 双抗国内获批上市
百济神州(06160)
5 月 29 日,NMPA 官网显示,百济神州 HER2 双特异性抗体「注射用泽尼达妥单抗」获批上市,适用于既往接受过全身治疗的HER2高表达(IHC3+)的不可切除局部晚期或转移性胆道癌患者。
本次获批,泽尼达妥单抗成为了国内首款获批上市的 HER2 双抗药物,同时也是首款获批用于胆道癌的 HER2 靶向药物,为胆道癌患者带来了新的治疗选择。
截图来源:NMPA 官网
泽尼达妥单抗(ZW25,Zanidatamab)最初由 Zymeworks 公司开发,可同时结合两个非重叠的 HER2 表位(亚基 2 和亚基 4),即双互补位结合。这种独特的设计可形成多种作用机制,包括双重阻断 HER2 信号、增强结合并去除细胞表面的 HER2 蛋白、强有力的抗体效应子功能以增进在患者中的抗肿瘤活性。百济神州早在 2018 年度就与 Zymeworks 达成合作,以 4000 万美元首付款、最高 3.9 亿美元里程碑款获得了泽尼达妥单抗和另一款 HER2 双抗 ADC 管线 ZW49 在亚洲(除日本外)、澳大利亚和新西兰的独家开发和商业化权利。不过双方在 2023 年 11 月已经终止了 ZW49 的项目合作。
2022 年 10 月,Zymeworks 又与 Jazz 公司达成一项高达 17.6 亿美元的合作,将泽尼达妥单抗在美国、欧洲、加拿大、日本等地区的权益授予该公司。
 截图来自:Insight 数据库网页版
截图来自:Insight 数据库网页版在海外,泽尼达妥单抗曾获得 FDA 授予的突破性疗法认定、快速通道资格、优先审评资格、孤儿药资格等,并获得了 NMPA 授予的突破性疗法、优先审评。2024 年 11 月 20 日,泽尼达妥单抗已经率先在美国获 FDA 批准上市。
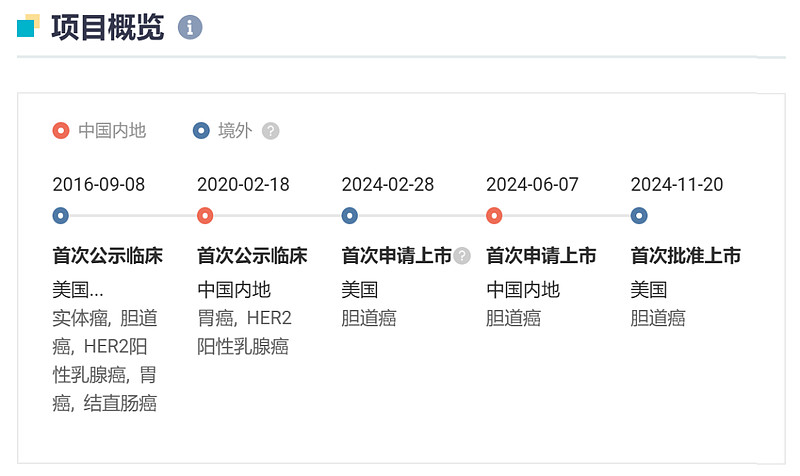 截图来自:Insight 数据库网页版
截图来自:Insight 数据库网页版泽尼达妥单抗的获批是基于临床 IIb 期试验 HERIZON-BTC-01 的数据。这项开放标签 IIb 期研究招募了 HER2 扩增、不可切除、局部晚期/转移性 BTC 且接受过 ≥ 1 次含吉西他滨全身性化疗的成人患者。主要终点为确认的客观缓解率(ORR)。
Insight 数据库显示,在 2023 ASCO 大会中 Zymeworks 首次公布了该项临床数据,2024 ASCO 大会上又公布了 OS 和长期随访数据;亚洲亚组的数据则在 2023 ESMO Asia 和 2024 ESMO Asia 中发布和更新。
2024 ASCO 上发布的数据显示,截至 2023 年 7 月 28 日,队列 1(HER2+,n=80)患者确认的客观缓解率(cORR)为 41.3%(33/80,95% CI:30.4-52.8),与此前截止 2022 年 10 月的初步分析结果一致,另增加一例完全缓解。
中位 DOR 为 14.9 个月(95% CI:7.4,未达到);中位 PFS 为 5.5 个月(95% CI:3.6,7.3);中位 OS 为 15.5 个月(95% CI:10.4,18.5)。
对不同 HER2 表达患者的亚组分析显示,IHC 3+ 患者 cORR 为 51.6%(95% CI:38.6-64.5),中位 PFS 为 7.2 个月(95% CI:5.4,9.4),中位 OS 为 18.1 个月(95% CI:12.2,23.2);IHC 2+ 患者 cORR 为 5.6%(95% CI:0.1-27.3),中位 PFS 为 1.7 个月(95% CI:1.0,3.3),中位 OS 为 5.2 个月(95% CI:3.1,10.2)。
亚洲亚组数据(N=50)显示,ORR 为 42%(95% CI:28-57),mDoR 为 11.2 个月(95% CI:3.9-NE),mOS 为 13.4 个月(95% CI:9.7,18.1),12 个月 OS 率为 54%(95% CI:38-67)。
截图来自:Insight 数据库网页版
除了二线胆道癌之外,泽尼达妥单抗仍在布局多个适应症,一线胆道癌(HERIZON-BTC-302)、二线及以上乳腺癌(EmpowHER-BC-303)、一线胃食管腺癌(HERIZON-GEA-01)都已经进入到 III 期临床研发中。本次获批之后,泽尼达妥单抗成功在胆道癌领域拔得头筹。不过值得一提的是,从适应症角度而论,第一三共/阿斯利康的明星药德曲妥珠单抗(Enhertu,DS-8201a)也启动了联用 PD-1/TIGIT 双抗 Rilvegostomig 一线治疗 HER2 阳性胆道癌的 网页链接{III 期临床} DESTINY-BTC01。从药物类型角度,康宁杰瑞与石药集团联合开发的 KN-026(Anbenitamab)同样是一款相似机制的 HER2 双抗,当前也已经在 III 期临床开发中。
来源:Insight数据库