全球首批!阿斯利康自免新药皮下剂型获批上市
来源:市场资讯
(来源:求实药社)
12月16日,阿斯利康宣布,其皮下注射生物制剂Saphnelo (Anifrolumab,阿伏利尤单抗皮下注射剂)已在欧盟获批,可作为预填充注射笔,用于系统性红斑狼疮(SLE)成年患者的皮下自行给药,作为标准疗法的补充。
新闻稿指出,便捷的皮下注射方式有望使更多患者获得与 Saphnelo 静脉输注相同的临床获益。

Saphnelo 是全球首个获批的靶向 Ⅰ 型干扰素通路的 SLE 治疗靶向药物,可与 I 型干扰素 (IFN) 受体亚基 1 结合,从而阻断 I 型干扰素的活性。I 型干扰素,例如 IFN-α、IFN-β 和 IFN-κ,是参与调节与 SLE 相关的炎症通路的细胞因子。
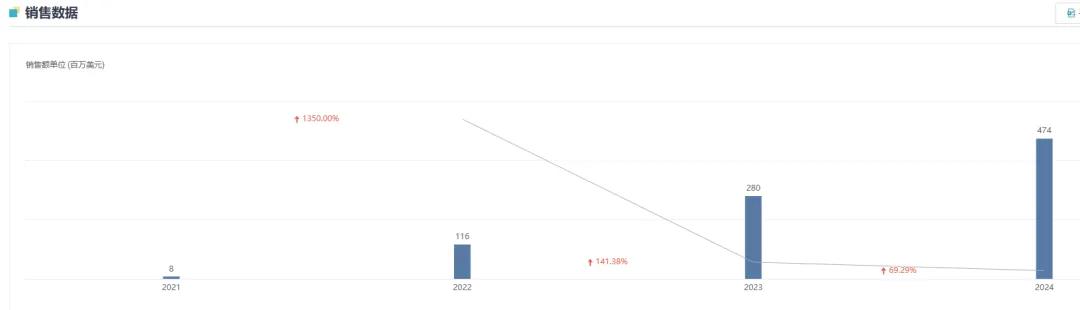
该药于 2021 年 7 月首次获得 FDA 批准,用于治疗中度至重度 SLE 成人患者,并于 2021 年 9 月、2022 年 2 月先后在日本和欧盟获批上市。自获批以来,阿伏利尤单抗销售额一路上涨,24 年全球销售额达 4.74 亿美元,同比大增 69.29%。2025 年前三季度斩获 4.83 亿美元,同比增长 47%。
本次是 Saphnelo 皮下制剂的全球首个批准。除了欧盟以外,Saphnelo 皮下注射剂正在包括美国和日本在内的多个国家接受监管审查。
今年 9 月,阿斯利康宣布 Saphnelo 皮下制剂针对 SLE患者 III 期 TULIP-SC 试验的预定中期分析达到主要终点。
TULIP-SC 是一项 3 期、多中心、跨国、随机、双盲、安慰剂对照研究,旨在评估在接受标准护理 (SOC) 治疗的中度至重度活动性自身抗体阳性 SLE 患者中,皮下注射 Saphnelo 与安慰剂的疗效和安全性。
结果显示,与安慰剂相比,Saphnelo 皮下注射疗法显著降低了疾病活动度,且具有临床意义。中期分析中观察到的安全性与 Saphnelo静脉输注的已知临床特征一致。
文章内容仅供参考,不构成投资建议。投资者据此操作,风险自担, 关于对文中陈述、观点判断保持中立,不对所包含内容的准确性、可靠性或完整性提供任何明示或暗示的保证。请读者仅作参考,并请自行承担全部。