NAMs非临床新航道:益诺思从细胞到类器官的体外心脏毒性评价平台
在药物研发的漫漫征程中,心脏毒性问题宛如一颗隐匿的“暗礁”,稍有不慎便可能引发药物研发的折戟沉沙。药源性心脏毒性,这一临床应用中发生率较高的不良反应,是众多药物上市后被迫撤市的罪魁祸首之一。据不完全统计,1950-2014年期间,全球共有462种药物因引发不良反应而撤市,其中63种药物因心脏毒性问题被强制下架,占比高达14%。
2013年7月,美国食品药品监督管理局(FDA)、心脏安全研究联合会(CSRC)、健康与环境科学研究所(HESI)联合提出了一种全新的TdP风险评价方式——综合性离体致心律失常风险评估(CiPA),离子通道和人诱导多能干细胞分化的心肌细胞(hiPSC-CMs)是其重要组成部分。2022年2月,ICH E14/S7BQ&A中针对hERG试验提出了“生理温度”和“最佳实践”,针对体外模型提出了可使用人源化细胞模型(如:类器官等)进行体外综合风险评估。2022年9月29日,美国参议院通过了《FDA现代化法案2.0》,该法案取消了新药临床试验申请(IND)中必须要进行动物实验的要求,允许通过体外实验或计算机模拟等替代方法获得FDA豁免。次年,FDA更新指南,鼓励药品开发商采用非动物实验测试方法(NAMs),例如细胞检测、器官类器官等,但仍要求提供与传统动物实验可比的相关数据。2025年4月10日,FDA宣布将逐步取消单克隆抗体和其他部分药物的动物试验要求,采用更有效、更贴近人体的实验方法,如细胞系和实验室环境下的类器官毒性测试。
在如此的前提背景下,益诺思深谙心脏毒性问题对药物研发的重大影响,凭借多年的技术沉淀与创新精神,精心打造了先进的体外心脏毒性平台,致力于为创新药物研发企业提供精准、高效、全面的心脏毒性评估服务,助力药物研发突破心脏毒性瓶颈,为患者带来更安全有效的治疗方案。
1
细胞→干细胞→类器官:
体外心脏毒解决方案"三级跳"
传统的体外hERG试验采用异源转染hERG钾通道的HEK293细胞,借助全细胞膜片钳技术,通过测定药物对hERG钾通道的阻滞作用,作为离子通道研究的“金标准”。益诺思体外心脏毒性评价平台始终紧贴技术前沿:2009年即率先引入自动化膜片钳,持续优化实验流程,形成标准化、高通量的hERG钾通道和Nav1.5钠通道检测体系。在CiPA的推动下,益诺思较早建立和验证了生理温度条件下hERG钾通道和Nav1.5钠通道评价方法,同时建立了满足ICH E14 / S7B Q&A中GLP条件下hERG钾通道试验的最佳实践条件,为药物早期筛选与优化提供可靠数据支撑。
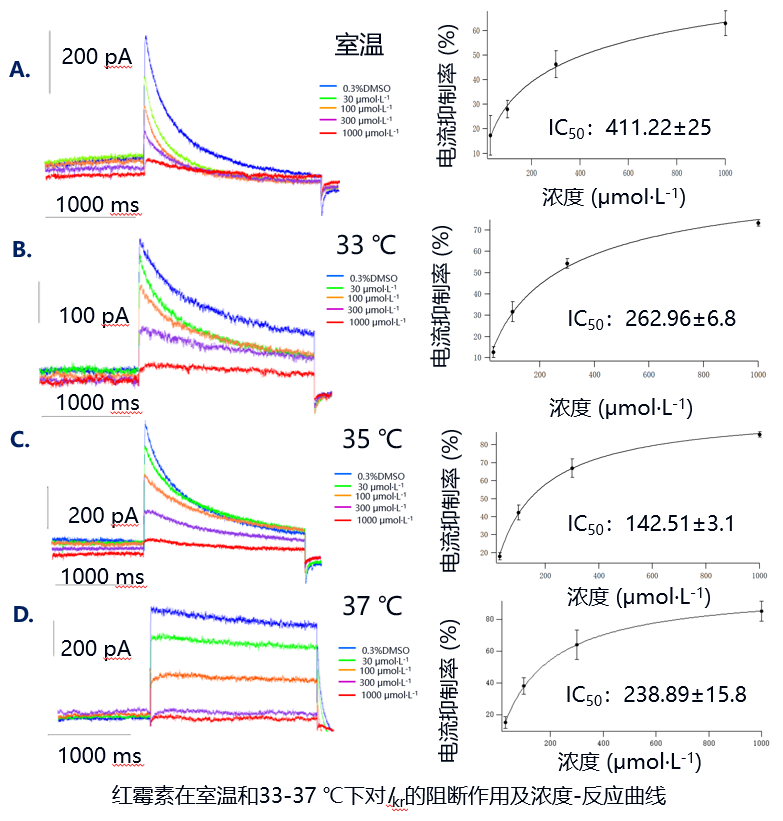
相较于转染单个离子通道的HEK293细胞模型,hiPSC-CMs具有与原生心肌细胞相似的电生理和药理学特性,能够模拟人类心脏组织的结构和功能特征,其离子通道表达丰富,包括INa、ICa-L、If、Ik1、Ito、Ikr、Iks等,均对动作电位持续时间有重要贡献,对肾上腺素和胆碱能的刺激也存在响应,接近成人心肌细胞的形态。益诺思采用健康人和长QT综合征患者来源的hiPSC-CMs模型,结合实时细胞分析技术(RTCA)监测hiPSC-CMs细胞的搏动频率、幅度和细胞活力,膜片钳技术监测离子通道电流变化,免疫荧光技术评估hiPSC-CMs的缝隙连接蛋白(CX-43)表达与分布,及Caspase-3/7活性检测评估细胞凋亡通路的激活情况,从结构到功能建立了基于hiPSC-CMs模型的心脏毒性评价方法,并采用多种阳性药物对所建立的方法进行了验证,为创新药物心脏毒性体外评价提供了一种新的解决方案。
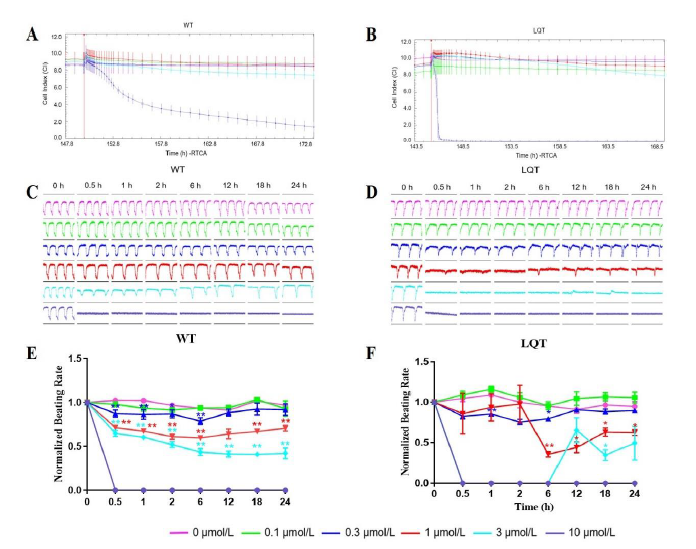
健康和疾病来源的hiPSC-CMs的生长曲线及搏动状态图
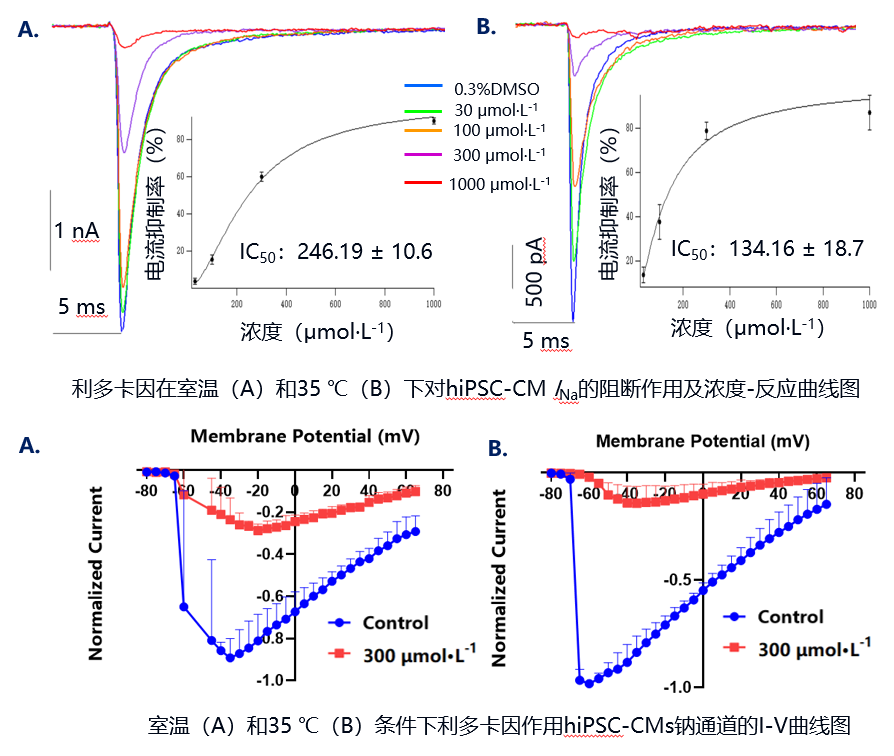
尽管hiPSC-CMs模型在心脏毒性评估中表现出色,但由于hiPSC-CMs缺乏内源性细胞外基质(ECM)和非心肌细胞的心脏细胞类型,在二维培养环境中还会逐渐失去细胞形态、诱导异常分裂、影响细胞分化表型,从而无法完全模拟心脏组织中细胞的功能和行为。心脏类器官是通过诱导hiPSCs在体外自组织形成的三维细胞结构,能够准确反映心脏的生理表型和药物诱导反应,更加真实地模拟人体内心脏电生理的复杂性。
1
益诺思心脏类器官模型
前沿探索
自组装心脏器官不仅能够生成多种细胞类型,包括心肌细胞、内皮细胞、成纤维细胞等,更接近天然心脏的细胞多样性,能够复制胚胎心脏发育过程中的细胞间相互作用和信号通路,对于心血管疾病的发病机制和治疗提供新的策略。与传统2D细胞模型相比,心脏类器官不仅能够模拟心脏发育过程中的细胞分化、组织形成和形态发成等过程,而且细胞类型组成多样,能够形成更接近人体内器官结构的复杂集群,表现出来的心肌细胞具有更 -高的成熟度,更接近人的电生理特性、收缩功能和细胞结构。
益诺思通过改进目前已有诱导分化方案,建立了一种生命周期长、形态更好、更适合药物毒性评价的心脏类器官培养方法。在此基础上,采用qPCR、免疫荧光、组织病理学、微电极阵列(MEA)及测序技术等多个手段和方法,对所构建的心脏类器官模型中搏动状态、形态和生物标志物、内部结构及电生理功能等在分化不同阶段时期的变化进行分析,对心脏类器官生命周期进行了探索,将心脏类器官分化与人胚胎时期心脏发育过程作对比;并对所构建的模型进行药物验证,为创新药物心脏毒性评价提供了一种新的选择,更贴近人体心脏生理和功能状态。
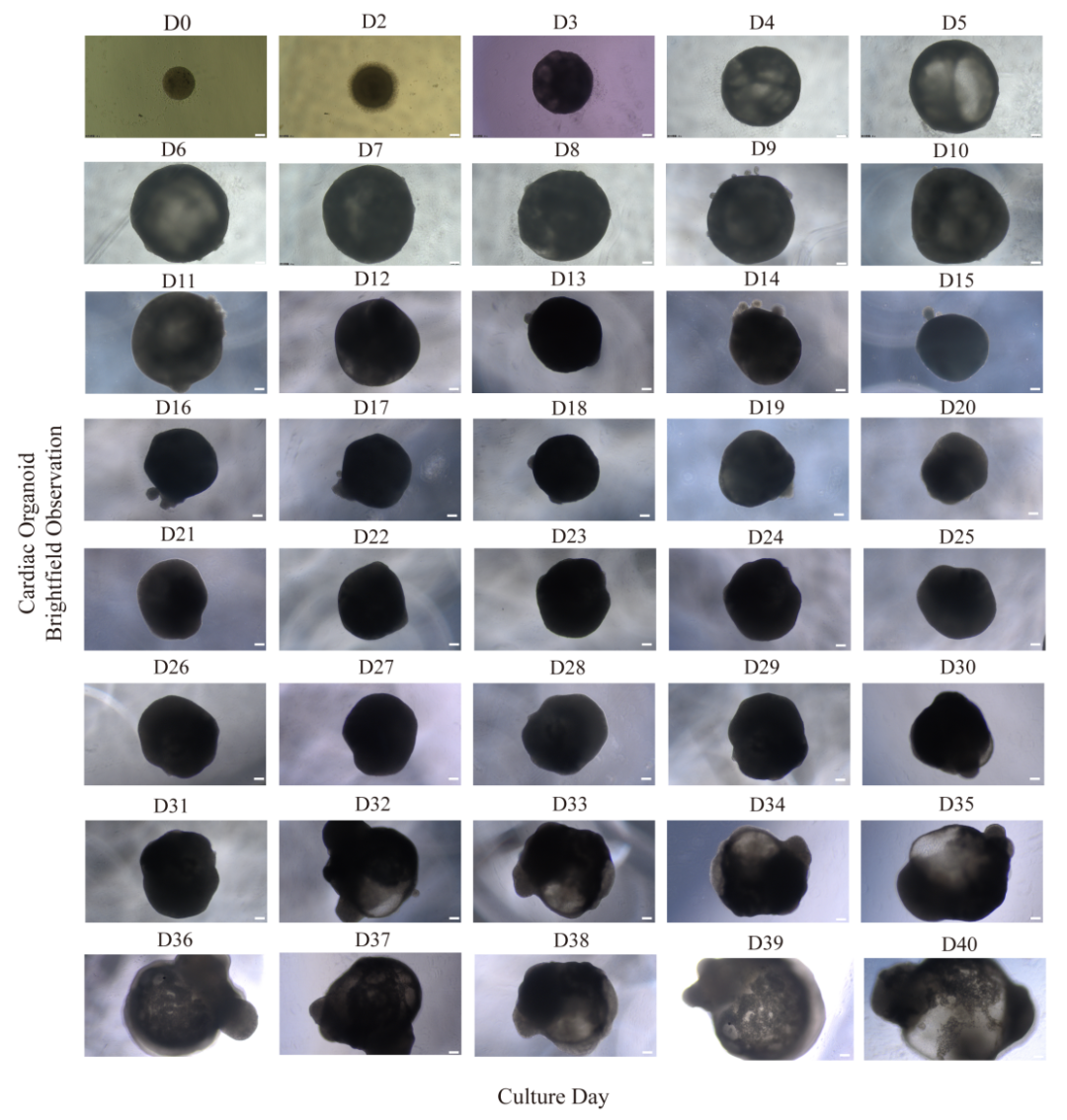
心脏类器官分化过程形态变化明场图
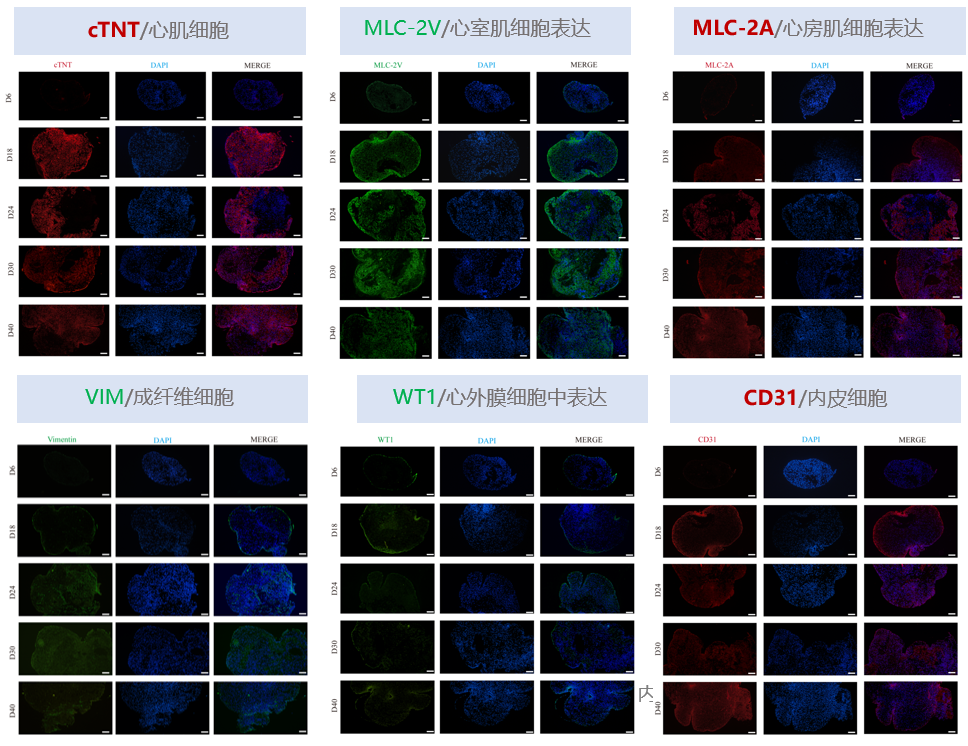
不同分化阶段心脏类器官不同细胞标志物的免疫荧光图
1
益诺思NAM探索
人源化技术路径转型
益诺思始终立于行业前沿,主动布局并深耕NAMs技术体系,将类器官、器官芯片、AI毒性预测等人源化模型与经典动物数据交叉验证,为每一款创新药量身定制“动物+NAMs”双轨并行的最优化方案,确保安全性评价既领先又可靠。
本文以心脏毒性的创新技术研究为例,从HEK293细胞模型到hiPSC-CMs模型再到心脏类器官模型,结合专业团队与优质服务,可为创新药物研发企业提供全面的心脏毒性体外评估解决方案。我们致力于帮助药物研发企业突破心脏毒性瓶颈,提高药物研发效率,降低研发成本,为患者带来更安全有效的治疗药物。